Dissertation Klaus Heitkamp 1999
Dissertation Klaus Heitkamp 1999 Dissertation Klaus Heitkamp 1999
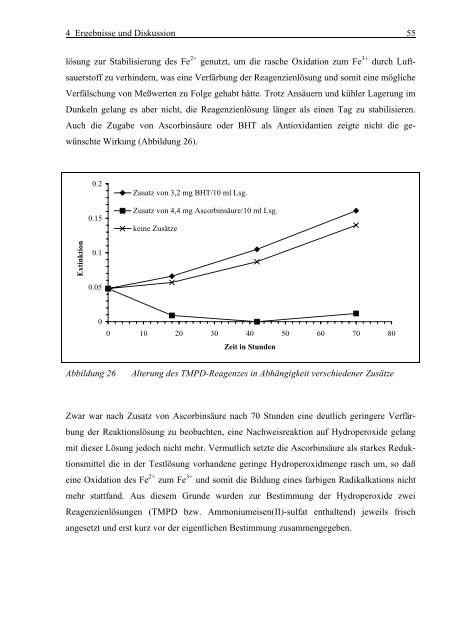
4 Ergebnisse und Diskussion 55lösung zur Stabilisierung des Fe 2+ genutzt, um die rasche Oxidation zum Fe 3+ durch Luftsauerstoffzu verhindern, was eine Verfärbung der Reagenzienlösung und somit eine möglicheVerfälschung von Meßwerten zu Folge gehabt hätte. Trotz Ansäuern und kühler Lagerung imDunkeln gelang es aber nicht, die Reagenzienlösung länger als einen Tag zu stabilisieren.Auch die Zugabe von Ascorbinsäure oder BHT als Antioxidantien zeigte nicht die gewünschteWirkung (Abbildung 26).Extinktion ...0.20.150.1Zusatz von 3,2 mg BHT/10 ml Lsg.Zusatz von 4,4 mg Ascorbinsäure/10 ml Lsg.keine Zusätze0.0500 10 20 30 40 50 60 70 80Zeit in StundenAbbildung 26Alterung des TMPD-Reagenzes in Abhängigkeit verschiedener ZusätzeZwar war nach Zusatz von Ascorbinsäure nach 70 Stunden eine deutlich geringere Verfärbungder Reaktionslösung zu beobachten, eine Nachweisreaktion auf Hydroperoxide gelangmit dieser Lösung jedoch nicht mehr. Vermutlich setzte die Ascorbinsäure als starkes Reduktionsmitteldie in der Testlösung vorhandene geringe Hydroperoxidmenge rasch um, so daßeine Oxidation des Fe 2+ zum Fe 3+ und somit die Bildung eines farbigen Radikalkations nichtmehr stattfand. Aus diesem Grunde wurden zur Bestimmung der Hydroperoxide zweiReagenzienlösungen (TMPD bzw. Ammoniumeisen(II)-sulfat enthaltend) jeweils frischangesetzt und erst kurz vor der eigentlichen Bestimmung zusammengegeben.
56 4 Ergebnisse und Diskussion4.2.2 Durchführung der MessungenZum Vergleich der verschiedenen photometrischen Bestimmungsmethoden wurden jeweilsVerdünnungsreihen von Wasserstoffperoxid, tert.-Butylhydroperoxid, 13S-Hydroperoxyoctadeca-9(Z),11(E)-diensäureund 13S-Hydroperoxyoctadeca-9(Z),11(E)-diensäuremethylesterangesetzt und diese entsprechend vermessen. Die Analyse der Lipidhydroperoxide erfolgte inmethanolischer Lösung. Wasserstoffperoxid und tert.-Butylhydroperoxide wurden in wäßrigerLösung vermessen. Die photometrische Auswertung erfolgte an einem Zeiss PM6 Photometer.Aus den erhaltenen Kalibriergeraden wurden Nachweis-, Erfassungs- und Bestimmungsgrenzein Anlehnung an die Norm DIN 32645 ermittelt. 135 Die einzelnen Arbeitsvorschriftensind nachstehend aufgeführt.4.2.2.1 Iodometrische TitrationZur iodometrischen Titration wurden in einem 100 ml Erlenmeyerkolben mit Schliffstopfenjeweils 10-15 mg Fettsäurehydroperoxid bzw. 10 ml einer ca. 0,2 %-igen wäßrigen Lösungvon Wasserstoffperoxid oder tert.-Butylperoxid mit 20 ml entgastem Eisessig versetzt. DerLösung wurde 1 ml einer wäßrigen, gesättigten Kaliumiodidlösung zugesetzt und der Kolbenanschließend mit Stickstoff ausgeblasen. Die Proben wurden für 30 Minuten an einen dunklenOrt gestellt und anschließend mit einer 0,05 molaren Natriumthiosulfatlösung unter Zusatzweniger Tropfen Stärkelösung bis zur Farblosigkeit titriert.4.2.2.2 TBA-Test335 mg Thiobarbitursäure (TBA) wurden unter leichtem Erwärmen in 5 ml Ethanol (enthielt6 mmol/l BHT) gelöst und diese Lösung dann mit Ethanol auf 50 ml aufgefüllt. Zur Messungwurden 700 µl der TBA-Lösung mit jeweils 150 µl der Probenlösung und einer 40 %-igenwäßrigen Trichloressigsäurelösung versetzt. Die Proben wurden 15 Minuten bei 80° C inkubiert.Ihre Extinktionen wurden anschließend bei 530 nm vermessen.
- Seite 17 und 18: 4 1 Einleitung - Vorkommen und Bede
- Seite 19 und 20: 6 3 Theoretischer Teil3 Theoretisch
- Seite 21 und 22: 8 3 Theoretischer TeilDer Radikalke
- Seite 23 und 24: 10 3 Theoretischer TeilDie Bildung
- Seite 25 und 26: 12 3 Theoretischer TeilHHR1R2R1R2(I
- Seite 27 und 28: 14 3 Theoretischer Teil3.2 Eigensch
- Seite 29 und 30: 16 3 Theoretischer TeilR1R2OOH R1 O
- Seite 31 und 32: 18 3 Theoretischer TeilDiese Method
- Seite 33 und 34: 20 3 Theoretischer TeilDamit ließ
- Seite 35 und 36: 22 3 Theoretischer TeilH 3CCNNR1H 3
- Seite 37 und 38: 24 3 Theoretischer TeilUeberreiter
- Seite 39 und 40: 26 3 Theoretischer TeilIn der Liter
- Seite 41 und 42: 28 3 Theoretischer TeilDie Methode
- Seite 43 und 44: 30 3 Theoretischer Teil3.3.3 GC-(MS
- Seite 45 und 46: 32 4 Ergebnisse und Diskussion4 Erg
- Seite 47 und 48: 34 4 Ergebnisse und DiskussionBezei
- Seite 49 und 50: 36 4 Ergebnisse und DiskussionProbe
- Seite 51 und 52: 38 4 Ergebnisse und Diskussionwurde
- Seite 53 und 54: 40 4 Ergebnisse und Diskussionwurde
- Seite 55 und 56: 42 4 Ergebnisse und Diskussion4.1.5
- Seite 57 und 58: 44 4 Ergebnisse und Diskussion4.1.5
- Seite 59 und 60: 46 4 Ergebnisse und DiskussionIm Ge
- Seite 61 und 62: 48 4 Ergebnisse und DiskussionIδ [
- Seite 63 und 64: 50 4 Ergebnisse und DiskussionSubst
- Seite 65 und 66: 52 4 Ergebnisse und Diskussion4.2 V
- Seite 67: 54 4 Ergebnisse und Diskussionentsp
- Seite 71 und 72: 58 4 Ergebnisse und Diskussiondient
- Seite 73 und 74: 60 4 Ergebnisse und DiskussionExtin
- Seite 75 und 76: 62 4 Ergebnisse und DiskussionMetho
- Seite 77 und 78: 64 4 Ergebnisse und Diskussion80706
- Seite 79 und 80: 66 4 Ergebnisse und DiskussionEine
- Seite 81 und 82: 68 4 Ergebnisse und Diskussion4.4 E
- Seite 83 und 84: 70 4 Ergebnisse und Diskussion501,1
- Seite 85 und 86: 72 4 Ergebnisse und DiskussionEinfl
- Seite 87 und 88: 74 4 Ergebnisse und DiskussionDie v
- Seite 89 und 90: 76 4 Ergebnisse und DiskussionLäng
- Seite 91 und 92: 78 4 Ergebnisse und DiskussionFür
- Seite 93 und 94: 80 4 Ergebnisse und DiskussionHydro
- Seite 95 und 96: 82 4 Ergebnisse und Diskussion4.5.1
- Seite 97 und 98: 84 4 Ergebnisse und DiskussionIm Fa
- Seite 99 und 100: 86 4 Ergebnisse und DiskussionDazu
- Seite 101 und 102: 88 4 Ergebnisse und Diskussion0,50,
- Seite 103 und 104: 90 4 Ergebnisse und Diskussionund a
- Seite 105 und 106: 92 4 Ergebnisse und DiskussionDas F
- Seite 107 und 108: 94 4 Ergebnisse und Diskussion1,0In
- Seite 109 und 110: 96 4 Ergebnisse und DiskussionReage
- Seite 111 und 112: 98 4 Ergebnisse und Diskussionblute
- Seite 113 und 114: 100 4 Ergebnisse und Diskussion1.8E
- Seite 115 und 116: 102 4 Ergebnisse und DiskussionReak
- Seite 117 und 118: 104 4 Ergebnisse und Diskussionbei
4 Ergebnisse und Diskussion 55lösung zur Stabilisierung des Fe 2+ genutzt, um die rasche Oxidation zum Fe 3+ durch Luftsauerstoffzu verhindern, was eine Verfärbung der Reagenzienlösung und somit eine möglicheVerfälschung von Meßwerten zu Folge gehabt hätte. Trotz Ansäuern und kühler Lagerung imDunkeln gelang es aber nicht, die Reagenzienlösung länger als einen Tag zu stabilisieren.Auch die Zugabe von Ascorbinsäure oder BHT als Antioxidantien zeigte nicht die gewünschteWirkung (Abbildung 26).Extinktion ...0.20.150.1Zusatz von 3,2 mg BHT/10 ml Lsg.Zusatz von 4,4 mg Ascorbinsäure/10 ml Lsg.keine Zusätze0.0500 10 20 30 40 50 60 70 80Zeit in StundenAbbildung 26Alterung des TMPD-Reagenzes in Abhängigkeit verschiedener ZusätzeZwar war nach Zusatz von Ascorbinsäure nach 70 Stunden eine deutlich geringere Verfärbungder Reaktionslösung zu beobachten, eine Nachweisreaktion auf Hydroperoxide gelangmit dieser Lösung jedoch nicht mehr. Vermutlich setzte die Ascorbinsäure als starkes Reduktionsmitteldie in der Testlösung vorhandene geringe Hydroperoxidmenge rasch um, so daßeine Oxidation des Fe 2+ zum Fe 3+ und somit die Bildung eines farbigen Radikalkations nichtmehr stattfand. Aus diesem Grunde wurden zur Bestimmung der Hydroperoxide zweiReagenzienlösungen (TMPD bzw. Ammoniumeisen(II)-sulfat enthaltend) jeweils frischangesetzt und erst kurz vor der eigentlichen Bestimmung zusammengegeben.