Angelika Semmler - KOPS - Universität Konstanz
Angelika Semmler - KOPS - Universität Konstanz
Angelika Semmler - KOPS - Universität Konstanz
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
4 Analytik<br />
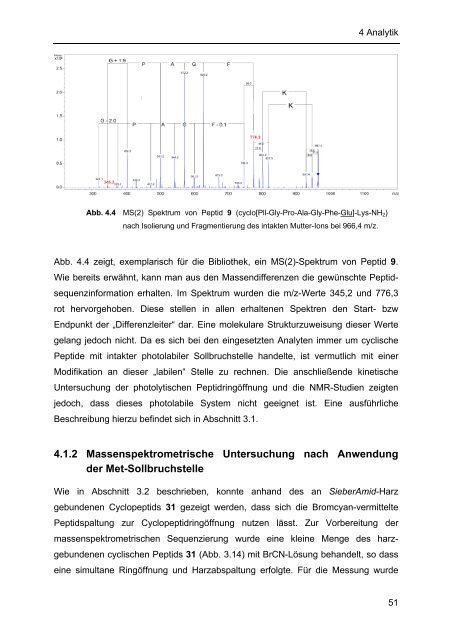
Abb. 4.4 MS(2) Spektrum von Peptid 9 (cyclo[Pll-Gly-Pro-Ala-Gly-Phe-Glu]-Lys-NH2)<br />
nach Isolierung und Fragmentierung des intakten Mutter-Ions bei 966,4 m/z.<br />
Abb. 4.4 zeigt, exemplarisch für die Bibliothek, ein MS(2)-Spektrum von Peptid 9.<br />
Wie bereits erwähnt, kann man aus den Massendifferenzen die gewünschte Peptid-<br />
sequenzinformation erhalten. Im Spektrum wurden die m/z-Werte 345,2 und 776,3<br />
rot hervorgehoben. Diese stellen in allen erhaltenen Spektren den Start- bzw<br />
Endpunkt der „Differenzleiter“ dar. Eine molekulare Strukturzuweisung dieser Werte<br />
gelang jedoch nicht. Da es sich bei den eingesetzten Analyten immer um cyclische<br />
Peptide mit intakter photolabiler Sollbruchstelle handelte, ist vermutlich mit einer<br />
Modifikation an dieser „labilen“ Stelle zu rechnen. Die anschließende kinetische<br />
Untersuchung der photolytischen Peptidringöffnung und die NMR-Studien zeigten<br />
jedoch, dass dieses photolabile System nicht geeignet ist. Eine ausführliche<br />
Beschreibung hierzu befindet sich in Abschnitt 3.1.<br />
4.1.2 Massenspektrometrische Untersuchung nach Anwendung<br />
der Met-Sollbruchstelle<br />
Wie in Abschnitt 3.2 beschrieben, konnte anhand des an SieberAmid-Harz<br />
gebundenen Cyclopeptids 31 gezeigt werden, dass sich die Bromcyan-vermittelte<br />
Peptidspaltung zur Cyclopeptidringöffnung nutzen lässt. Zur Vorbereitung der<br />
massenspektrometrischen Sequenzierung wurde eine kleine Menge des harz-<br />
gebundenen cyclischen Peptids 31 (Abb. 3.14) mit BrCN-Lösung behandelt, so dass<br />
eine simultane Ringöffnung und Harzabspaltung erfolgte. Für die Messung wurde<br />
51