HerzSupplement - Pentalong von Actavis
HerzSupplement - Pentalong von Actavis
HerzSupplement - Pentalong von Actavis
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
fokussiert. Wir konnten in älteren Arbeiten<br />
zeigen, dass die ALDH2 in isolierten Mitochondrien<br />
durch Nitroglyzerin oder mitochondriale<br />
reaktive Sauerstoff und Stickstoffspezies<br />
(e.g. Peroxynitrit und Superoxid)<br />
oxidativ inaktiviert wird [42]. Ellman’s Reagenz,<br />
eine Thiol oxidierende Substanz zur<br />
Quantifizierung <strong>von</strong> Thiolgruppen, bewirkte<br />
eine Inaktivierung des Enzyms – ein Hinweis<br />
auf die Beteiligung <strong>von</strong> Thiolgruppen am<br />
Katalysezyklus [42]. 2008 wurde erstmals an<br />
gereinigter, isolierter, rekombinanter, humaner<br />
ALDH2 gezeigt, dass dieses Enzym<br />
eindeutig eine Bioaktivierung <strong>von</strong> GTN katalysiert<br />
[43]. Die Autoren verwendeten als<br />
Nachweissystem für die direkte Bioaktivierung<br />
<strong>von</strong> GTN durch die ALDH2 die gereinigte<br />
lösliche Guanylatzyklase (sGC): Der<br />
durch die ALDH2 und GTN gebildete Vasodilatator<br />
(NO oder eine NOähnliche Spezies)<br />
aktiviert die sGC und damit die Bildung<br />
<strong>von</strong> cGMP – ein elegantes Testsystem. Hier<br />
wurde auch erstmals gezeigt, dass die gereinigte<br />
zytosolische ALDH1Isoform ebenfalls<br />
eine Bioaktivierung <strong>von</strong> GTN bewirkt,<br />
allerdings ist sie um den Faktor 33 weniger<br />
potent als ALDH2 (Abb. 5) [43].<br />
B<br />
ALDH2-Aktivität<br />
[µM 2-Hydroxy-3-Nitrobenzolsäure]<br />
80<br />
70<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
+ 0,1 mM LA<br />
Herz 35 · 2010 · Supplement II © Urban & Vogel<br />
*<br />
A<br />
A340 [a.u.]<br />
0,5<br />
0,4<br />
0,3<br />
0,2<br />
0,1<br />
Ethanol in vivo GTN in vivo<br />
Aus der gleichen Gruppe wurde vor<br />
Kurzem eine Arbeit publiziert, die zeigte,<br />
dass GTN eine teils irreversible Inaktivierung<br />
des isolierten ALDH2Enzyms be<br />
µmol cGMP × min –1 × mg –1<br />
ALDH<br />
7<br />
6<br />
5<br />
4<br />
3<br />
2<br />
1<br />
0<br />
GTN<br />
ALDH-1<br />
ALDH-2<br />
BSA<br />
DTT<br />
0<br />
0 400 800 1200 1600<br />
Zeit [s]<br />
C 120<br />
100<br />
80<br />
* #<br />
60<br />
*<br />
40<br />
20<br />
0<br />
+ 0,1 mM LA<br />
ALDH2-Aktivität<br />
[%]<br />
Kontrolle + 0<br />
Organische Nitrate<br />
10 –8 10 –7 10 –6 10 –5 10 –4 10 –3<br />
GTN [M]<br />
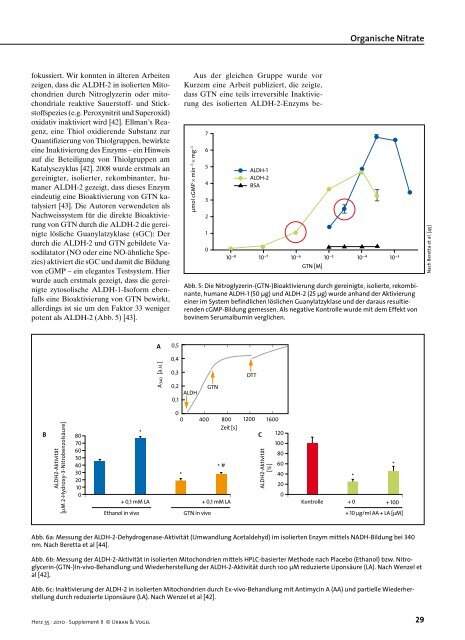
Abb. 5: Die Nitroglyzerin�(GTN�)Bioaktivierung durch gereinigte, isolierte, rekombi�<br />
nante, humane ALDH�1 (50 µg) und ALDH�2 (25 µg) wurde anhand der Aktivierung<br />
einer im System befindlichen löslichen Guanylatzyklase und der daraus resultie�<br />
renden cGMP�Bildung gemessen. Als negative Kontrolle wurde mit dem Effekt <strong>von</strong><br />
bovinem Serumalbumin verglichen.<br />
*<br />
*<br />
+ 100<br />
+ 10 µg/ml AA + LA [µM]<br />
Abb. 6a: Messung der ALDH�2�Dehydrogenase�Aktivität (Umwandlung Acetaldehyd) im isolierten Enzym mittels NADH�Bildung bei 340<br />
nm. Nach Beretta et al [44].<br />
Abb. 6b: Messung der ALDH�2�Aktivität in isolierten Mitochondrien mittels HPLC�basierter Methode nach Placebo (Ethanol) bzw. Nitro�<br />
glycerin�(GTN�)In�vivo�Behandlung und Wiederherstellung der ALDH�2�Aktivität durch 100 µM reduzierte Liponsäure (LA). Nach Wenzel et<br />
al [42].<br />
Abb. 6c: Inaktivierung der ALDH�2 in isolierten Mitochondrien durch Ex�vivo�Behandlung mit Antimycin A (AA) und partielle Wiederher�<br />
stellung durch reduzierte Liponsäure (LA). Nach Wenzel et al [42].<br />
29<br />
Nach Beretta et al. [45]