HerzSupplement - Pentalong von Actavis
HerzSupplement - Pentalong von Actavis HerzSupplement - Pentalong von Actavis
Herz Supplement Cardiovascular Diseases Vorrangig wurde das nitrooxylierte SimvastatinDerivat LE-CL10 synthetisiert, also ein SimvastationNODonorHybridmolekül. Das heißt, dem Statin wurde mit einem organischen Nitrat eine zweite bioaktive, die NO/sGC/cGMPSignaltransduktion regulierende Struktur im Molekül zur Seite gestellt. Erwartungsgemäß zeigte dieses Hybridmolekül einen vasodilatatorischen Effekt. An isolierten Pulmonalarterien des Schweins (Organbadexperimente) zeigten wir, dass die vasodilatatorische Wirkstärke des organischen Nitrates durch die Einführung des großen organischen Statingerüstes nicht gemindert wird. Die Nitratopivalinsäure allein und das SimvastatinNitratHybrid zeigen beide eine ähnliche, moderate vasodilatatorische Wirkung (Abb. 2). Eine ausgeprägte Inhibition der Amyloidaggregation konnten wir jedoch nicht feststellen. Fluoreszenzintensität [%] 35000 30000 25000 20000 15000 10000 5000 Obwohl für die Substanzklasse der Statine strukturell eher untypisch wurde dann eine Nitratoacylierung an der Hydroxygruppe des LovastatinLactonringes durchgeführt. Erfreulicher und überraschenderweise zeigte dieses StatinNitratHybrid LECL11 nun eine inhibitorische Wirkung von bemerkenswerten 65% auf die direkte AβAggregation über einen Zeitraum von über 96 h (Abb. 3). Die Kurvenscharen in Abbildung 3 demonstrieren die Qualität dieses Befundes eindrucksvoll. Dieses Ergebnis gab Anlass zur Synthese weiterer Statin und NitratoStatinDerivate der allgemeinen Formel (I) (Abb. 4). Alle weiteren nitratoacylierten Substanzen zeigten eine inhibitorische Wirkung auf die direkte AβAggregation, jedoch konnte keine der getesteten Substanzen in ihrer Wirksamkeit an die Verbindung LECL11 heranreichen (Abb. 5). Kontrolle 0 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 Zeit [h] Abb. 3: Gehemmte Aβ-Aggregation (rot) unter dem Einfluss von LE-CL11. O HO O O O HO COOH OH R1 O O O O O OH O Lovastatin (I) Abb. 4: Syntheseschema der acylierten und nitratoacylierten Statinderivate, wobei R1, bzw. R2 Acyl- und/oder Nitratoacyl-Reste sein können. 14 Herz 35 · 2010 · Supplement II © Urban & Vogel R2 O 2 N
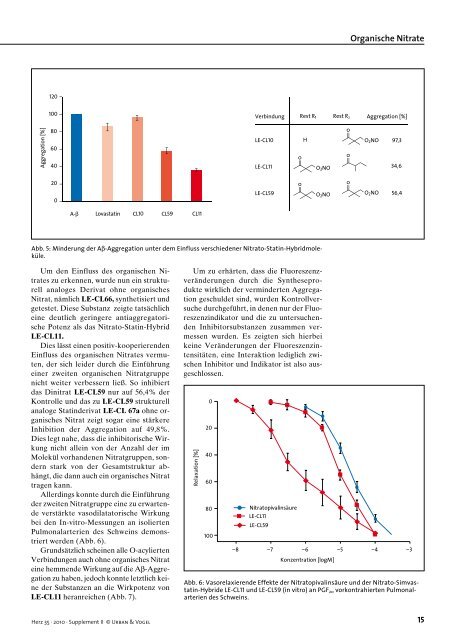
Aggregation [%] 120 100 80 60 40 20 0 A-β Lovastatin CL10 CL59 CL11 Um den Einfluss des organischen Nitrates zu erkennen, wurde nun ein strukturell analoges Derivat ohne organisches Nitrat, nämlich LE-CL66, synthetisiert und getestet. Diese Substanz zeigte tatsächlich eine deutlich geringere antiaggregatorische Potenz als das NitratoStatinHybrid LE-CL11. Dies lässt einen positivkooperierenden Einfluss des organischen Nitrates vermuten, der sich leider durch die Einführung einer zweiten organischen Nitratgruppe nicht weiter verbessern ließ. So inhibiert das Dinitrat LE-CL59 nur auf 56,4% der Kontrolle und das zu LE-CL59 strukturell analoge Statinderivat LE-CL 67a ohne organisches Nitrat zeigt sogar eine stärkere Inhibition der Aggregation auf 49,8%. Dies legt nahe, dass die inhibitorische Wirkung nicht allein von der Anzahl der im Molekül vorhandenen Nitratgruppen, sondern stark von der Gesamtstruktur abhängt, die dann auch ein organisches Nitrat tragen kann. Allerdings konnte durch die Einführung der zweiten Nitratgruppe eine zu erwartende verstärkte vasodilatatorische Wirkung bei den InvitroMessungen an isolierten Pulmonalarterien des Schweins demonstriert werden (Abb. 6). Grundsätzlich scheinen alle Oacylierten Verbindungen auch ohne organisches Nitrat eine hemmende Wirkung auf die AβAggregation zu haben, jedoch konnte letztlich keine der Substanzen an die Wirkpotenz von LE-CL11 heranreichen (Abb. 7). Herz 35 · 2010 · Supplement II © Urban & Vogel Um zu erhärten, dass die Fluoreszenzveränderungen durch die Syntheseprodukte wirklich der verminderten Aggregation geschuldet sind, wurden Kontrollversuche durchgeführt, in denen nur der Fluoreszenzindikator und die zu untersuchenden Inhibitorsubstanzen zusammen vermessen wurden. Es zeigten sich hierbei keine Veränderungen der Fluoreszenzintensitäten, eine Interaktion lediglich zwischen Inhibitor und Indikator ist also ausgeschlossen. Organische Nitrate Verbindung Rest R1 Rest R2 Aggregation [%] LE-CL10 LE-CL11 LE-CL59 Abb. 5: Minderung der Aβ-Aggregation unter dem Einfluss verschiedener Nitrato-Statin-Hybridmoleküle. Relaxation [%] 0 20 40 60 80 100 Nitratopivalinsäure LE-CL11 LE-CL59 0 0 H O2NO O2NO 0 0 0 O2NO O2NO 97,3 34,6 56,4 –8 –7 –6 Konzentration [logM] –5 –4 –3 Abb. 6: Vasorelaxierende Effekte der Nitratopivalinsäure und der Nitrato-Simvastatin-Hybride LE-CL11 und LE-CL59 (in vitro) an PGF2a vorkontrahierten Pulmonalarterien des Schweins. 15
- Seite 1 und 2: Herz Supplement Cardiovascular Dise
- Seite 3 und 4: Vorwort PETN- und PETN-Verwandtes I
- Seite 5 und 6: in A gehemmt wurden, dann fand kein
- Seite 7 und 8: Entwicklung einer LC-MS-Methode zur
- Seite 9 und 10: Bildung von FormiatAddukten zu ge
- Seite 11 und 12: Summary Pentaerythritol tetranitrat
- Seite 13: von Cholesterolsynthesehemmern (Sta
- Seite 17 und 18: Der durch Fluoreszenzmessungen erka
- Seite 19 und 20: eigene Klasse von Nitrovasodilatato
- Seite 21 und 22: tenverzweigung führte zu abgeschw
- Seite 23 und 24: nische Nitrate wirken, weil aus ihr
- Seite 25 und 26: mitierung der organischen Nitrate d
- Seite 27 und 28: A 5,5 p = 0,427 B C Durchmesser der
- Seite 29 und 30: fokussiert. Wir konnten in älteren
- Seite 31 und 32: Nach Daiber et al. In Vorbereitung
- Seite 33 und 34: L-012-Chemilumineszenz [min] 1,2 ×
- Seite 35 und 36: chondrial nitrite reduction coupled
- Seite 37 und 38: iosklerose verlangsamt werden könn
- Seite 39 und 40: L-NAME Puffer Nicht bestimmte Einhe
- Seite 41 und 42: Nach Schuhmacher et al. Hypertensio
- Seite 43 und 44: oxidativen Spektrums nicht nur auss
- Seite 45 und 46: Pulmonale Hypertonie - ein weiteres
- Seite 47 und 48: 2. Pulmonale Hypertonie - klinische
- Seite 49 und 50: Literatur 1. Schwemmer M, Bassenge
- Seite 51 und 52: Klinisch von Bedeutung sind vor all
- Seite 53 und 54: a 123-Rhodaminfluoreszenz ∆% zu u
- Seite 55 und 56: we speculate that GTN affects ROS f
- Seite 57 und 58: der Zellen exportiert werden. Auch
- Seite 59 und 60: A B NRF2 HuR-abhängige Stabilisier
- Seite 61 und 62: a Relative Luciferaseaktivität [%
- Seite 63 und 64: die nach Literaturangaben (siehe [1
Aggregation [%]<br />
120<br />
100<br />
80<br />
60<br />
40<br />
20<br />
0<br />
A-β Lovastatin CL10 CL59 CL11<br />
Um den Einfluss des organischen Nitrates<br />
zu erkennen, wurde nun ein strukturell<br />
analoges Derivat ohne organisches<br />
Nitrat, nämlich LE-CL66, synthetisiert und<br />
getestet. Diese Substanz zeigte tatsächlich<br />
eine deutlich geringere antiaggregatorische<br />
Potenz als das NitratoStatinHybrid<br />
LE-CL11.<br />
Dies lässt einen positivkooperierenden<br />
Einfluss des organischen Nitrates vermuten,<br />
der sich leider durch die Einführung<br />
einer zweiten organischen Nitratgruppe<br />
nicht weiter verbessern ließ. So inhibiert<br />
das Dinitrat LE-CL59 nur auf 56,4% der<br />
Kontrolle und das zu LE-CL59 strukturell<br />
analoge Statinderivat LE-CL 67a ohne organisches<br />
Nitrat zeigt sogar eine stärkere<br />
Inhibition der Aggregation auf 49,8%.<br />
Dies legt nahe, dass die inhibitorische Wirkung<br />
nicht allein <strong>von</strong> der Anzahl der im<br />
Molekül vorhandenen Nitratgruppen, sondern<br />
stark <strong>von</strong> der Gesamtstruktur abhängt,<br />
die dann auch ein organisches Nitrat<br />
tragen kann.<br />
Allerdings konnte durch die Einführung<br />
der zweiten Nitratgruppe eine zu erwartende<br />
verstärkte vasodilatatorische Wirkung<br />
bei den InvitroMessungen an isolierten<br />
Pulmonalarterien des Schweins demonstriert<br />
werden (Abb. 6).<br />
Grundsätzlich scheinen alle Oacylierten<br />
Verbindungen auch ohne organisches Nitrat<br />
eine hemmende Wirkung auf die AβAggregation<br />
zu haben, jedoch konnte letztlich keine<br />
der Substanzen an die Wirkpotenz <strong>von</strong><br />
LE-CL11 heranreichen (Abb. 7).<br />
Herz 35 · 2010 · Supplement II © Urban & Vogel<br />
Um zu erhärten, dass die Fluoreszenzveränderungen<br />
durch die Syntheseprodukte<br />
wirklich der verminderten Aggregation<br />
geschuldet sind, wurden Kontrollversuche<br />
durchgeführt, in denen nur der Fluoreszenzindikator<br />
und die zu untersuchenden<br />
Inhibitorsubstanzen zusammen vermessen<br />
wurden. Es zeigten sich hierbei<br />
keine Veränderungen der Fluoreszenzintensitäten,<br />
eine Interaktion lediglich zwischen<br />
Inhibitor und Indikator ist also ausgeschlossen.<br />
Organische Nitrate<br />
Verbindung Rest R1 Rest R2 Aggregation [%]<br />
LE-CL10<br />
LE-CL11<br />
LE-CL59<br />
Abb. 5: Minderung der Aβ-Aggregation unter dem Einfluss verschiedener Nitrato-Statin-Hybridmoleküle.<br />
Relaxation [%]<br />
0<br />
20<br />
40<br />
60<br />
80<br />
100<br />
Nitratopivalinsäure<br />
LE-CL11<br />
LE-CL59<br />
0<br />
0<br />
H<br />
O2NO<br />
O2NO<br />
0<br />
0<br />
0<br />
O2NO<br />
O2NO<br />
97,3<br />
34,6<br />
56,4<br />
–8 –7 –6<br />
Konzentration [logM]<br />
–5 –4 –3<br />
Abb. 6: Vasorelaxierende Effekte der Nitratopivalinsäure und der Nitrato-Simvastatin-Hybride<br />
LE-CL11 und LE-CL59 (in vitro) an PGF2a vorkontrahierten Pulmonalarterien<br />
des Schweins.<br />
15