SEW - lern-soft-projekt
SEW - lern-soft-projekt SEW - lern-soft-projekt
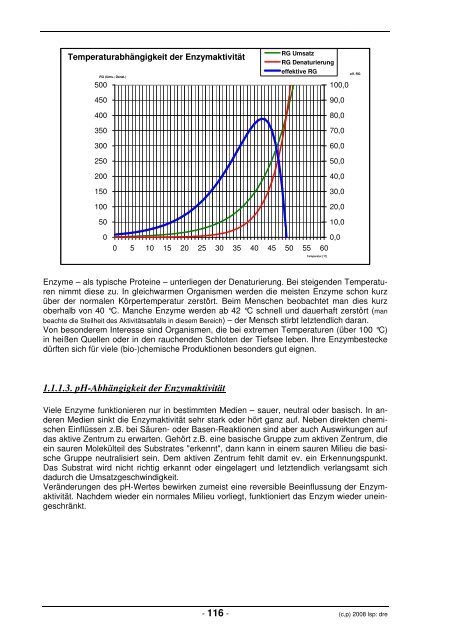
1.1.1.2. Temperaturabhängigkeit der Enzymaktivität Aus der Chemie kennen wir die RGT-Regel (Reaktionsgeschwindigkeits-Temperatur-Regel). Sie besagt, dass bei einer Erhöhung der Temperatur um 10 Grad (bzw. K) die Reaktionsgeschwindigkeit um das 2- bis 3-fache steigt. Selten kann es aber auch das 10-fache sein. Graphisch dargestellt ergibt sich für jede chemische Reaktion eine expotentielle Kurve für die Abhängigkeit der Reaktionsgeschwindigkeit von der Temperatur. 0,0 10,0 20,0 30,0 40,0 50,0 60,0 Temperatur Untersucht man nun die Temperaturabhängigkeit der Enzymaktivität, dann erhält man eine stark abweichende Kurve. Im ersten Abschnitt stimmt die Kurvenform mit der "normalen" chemischen Reaktion überein. Ab einer bestimmten Temperatur wird der Anstieg geringer und nimmt nach dem Erreichen eines Maximalwertes für die Enzymaktivität ab. Wie kann diese Kurve interpretiert werden Prinzipiell muss ja die RGT-Regel 0,0 10,0 20,0 30,0 40,0 50,0 60,0 auch für Enzyme gelten. Schließlich sind es ja auch nur einfache Temperatur chemische Reaktionen. Und es ist auch so, die RGT-Regel gilt auch hier. Bei Enzymen kommt zu der reinen Umsatzreaktion eine zweite Reaktion dazu, die mit betrachtet werden muss – die Zerstörungsreaktion (Denaturierung) des Enzyms selbst. Beide Reaktionen zusammen ergeben die effektive Reaktionsgeschwindigkeit des Enzyms, die wir in Experimenten normalerweise messen. ! ! ":4 / *%;! ;! :%* ! ! ,%'"9"& , 0 ! ! " :4 / *% ()! % ! ! &
Temperaturabhängigkeit der Enzymaktivität RG (Ums.; Denat.) 500 450 400 350 300 250 200 150 100 50 RG Umsatz RG Denaturierung effektive RG 100,0 90,0 80,0 70,0 60,0 50,0 40,0 30,0 20,0 10,0 eff. RG 0 0,0 0 5 10 15 20 25 30 35 40 45 50 55 60 Temperatur [°C] Enzyme – als typische Proteine – unterliegen der Denaturierung. Bei steigenden Temperaturen nimmt diese zu. In gleichwarmen Organismen werden die meisten Enzyme schon kurz über der normalen Körpertemperatur zerstört. Beim Menschen beobachtet man dies kurz oberhalb von 40 °C. Manche Enzyme werden ab 42 °C schnell und dauerhaft zerstört (man beachte die Steilheit des Aktivitätsabfalls in diesem Bereich) – der Mensch stirbt letztendlich daran. Von besonderem Interesse sind Organismen, die bei extremen Temperaturen (über 100 °C) in heißen Quellen oder in den rauchenden Schloten der Tiefsee leben. Ihre Enzymbestecke dürften sich für viele (bio-)chemische Produktionen besonders gut eignen. 1.1.1.3. pH-Abhängigkeit der Enzymaktivität Viele Enzyme funktionieren nur in bestimmten Medien – sauer, neutral oder basisch. In anderen Medien sinkt die Enzymaktivität sehr stark oder hört ganz auf. Neben direkten chemischen Einflüssen z.B. bei Säuren- oder Basen-Reaktionen sind aber auch Auswirkungen auf das aktive Zentrum zu erwarten. Gehört z.B. eine basische Gruppe zum aktiven Zentrum, die ein sauren Molekülteil des Substrates "erkennt", dann kann in einem sauren Milieu die basische Gruppe neutralisiert sein. Dem aktiven Zentrum fehlt damit ev. ein Erkennungspunkt. Das Substrat wird nicht richtig erkannt oder eingelagert und letztendlich verlangsamt sich dadurch die Umsatzgeschwindigkeit. Veränderungen des pH-Wertes bewirken zumeist eine reversible Beeinflussung der Enzymaktivität. Nachdem wieder ein normales Milieu vorliegt, funktioniert das Enzym wieder uneingeschränkt. - 116 - (c,p) 2008 lsp: dre
- Seite 1 und 2: Teil: A B E C D 1 2 3 (c,p)'9
- Seite 3 und 4: Inhaltsverzeichnis: Seite [ ! ] Vor
- Seite 5 und 6: [ I ] Entwicklung der Organismen (V
- Seite 7 und 8: Exkurs: moderne systhemische Betrac
- Seite 9 und 10: Aus evolutionärer Sicht ist der St
- Seite 11 und 12: 1.1. Enzyme und enzymatische Reakti
- Seite 13 und 14: Exkurs: Katalyse Betrachten wir zue
- Seite 15 und 16: Manchmal passen andere Substrate do
- Seite 17 und 18: 1.1.1. Abhängigkeit der Enzymaktiv
- Seite 19: ! ! "# $! %&'()! ! ! ! ! * + , "
- Seite 23 und 24: über eine Neuproduktion des Enzyms
- Seite 25 und 26: Von MONOD (1910 - 1976) et. al. sta
- Seite 27 und 28: 1.2. Transport von Energie und Redu
- Seite 29 und 30: Verhindert man z.B. bei einer chemi
- Seite 31 und 32: Das ATP-System Adenosintriphosphat
- Seite 33 und 34: Das NADP + nimmt zwei Elektronen un
- Seite 35 und 36: - 130 - (c,p) 2008 lsp: dre
- Seite 37 und 38: 2.1. anaerobe Dissimilation (Gärun
- Seite 39 und 40: Umwandlung der Glucose in Fructose
- Seite 41 und 42: Umwandlung des Reaktionsproduktes (
- Seite 43 und 44: '" "! A( 4 )), Q: de.wikipedia.org
- Seite 45 und 46: 2.1.2.1. alkoholischen Gärung In d
- Seite 47 und 48: 2.1.2.2. Milchsäure-Gärung Zu die
- Seite 49 und 50: 2.1.2.8. weitere Gärungen Bei den
- Seite 51 und 52: 2.2.1. Zitrat-Zyklus Der Zitrat-Zyk
- Seite 53 und 54: Oxidation und Decarboxylierung (Ene
- Seite 55 und 56: Abschlussübersicht Betrachtet man
- Seite 57 und 58: Ablauf der Atmungskette Glycolyse u
- Seite 59 und 60: ' " * ! %! * "! , 0 " * 9 &
- Seite 61 und 62: 3. Assimilations-Vorgänge Assimila
- Seite 63 und 64: 3.1.1. heterotrophe Assimilation (a
- Seite 65 und 66: 3.1.2.1. das Verdauungssystem des M
- Seite 67 und 68: Die Bauchspeicheldrüse (Pankreas)
- Seite 69 und 70: Exkurs: Parasiten im Verdauungstrak
Temperaturabhängigkeit der Enzymaktivität<br />
RG (Ums.; Denat.)<br />
500<br />
450<br />
400<br />
350<br />
300<br />
250<br />
200<br />
150<br />
100<br />
50<br />
RG Umsatz<br />
RG Denaturierung<br />
effektive RG<br />
100,0<br />
90,0<br />
80,0<br />
70,0<br />
60,0<br />
50,0<br />
40,0<br />
30,0<br />
20,0<br />
10,0<br />
eff. RG<br />
0<br />
0,0<br />
0 5 10 15 20 25 30 35 40 45 50 55 60<br />
Temperatur [°C]<br />
Enzyme – als typische Proteine – unterliegen der Denaturierung. Bei steigenden Temperaturen<br />
nimmt diese zu. In gleichwarmen Organismen werden die meisten Enzyme schon kurz<br />
über der normalen Körpertemperatur zerstört. Beim Menschen beobachtet man dies kurz<br />
oberhalb von 40 °C. Manche Enzyme werden ab 42 °C schnell und dauerhaft zerstört (man<br />
beachte die Steilheit des Aktivitätsabfalls in diesem Bereich) – der Mensch stirbt letztendlich daran.<br />
Von besonderem Interesse sind Organismen, die bei extremen Temperaturen (über 100 °C)<br />
in heißen Quellen oder in den rauchenden Schloten der Tiefsee leben. Ihre Enzymbestecke<br />
dürften sich für viele (bio-)chemische Produktionen besonders gut eignen.<br />
1.1.1.3. pH-Abhängigkeit der Enzymaktivität<br />
Viele Enzyme funktionieren nur in bestimmten Medien – sauer, neutral oder basisch. In anderen<br />
Medien sinkt die Enzymaktivität sehr stark oder hört ganz auf. Neben direkten chemischen<br />
Einflüssen z.B. bei Säuren- oder Basen-Reaktionen sind aber auch Auswirkungen auf<br />
das aktive Zentrum zu erwarten. Gehört z.B. eine basische Gruppe zum aktiven Zentrum, die<br />
ein sauren Molekülteil des Substrates "erkennt", dann kann in einem sauren Milieu die basische<br />
Gruppe neutralisiert sein. Dem aktiven Zentrum fehlt damit ev. ein Erkennungspunkt.<br />
Das Substrat wird nicht richtig erkannt oder eingelagert und letztendlich verlangsamt sich<br />
dadurch die Umsatzgeschwindigkeit.<br />
Veränderungen des pH-Wertes bewirken zumeist eine reversible Beeinflussung der Enzymaktivität.<br />
Nachdem wieder ein normales Milieu vorliegt, funktioniert das Enzym wieder uneingeschränkt.<br />
- 116 - (c,p) 2008 lsp: dre