Erlebnisgastronomie 300 m untertage – das ... - RDB eV
Erlebnisgastronomie 300 m untertage – das ... - RDB eV
Erlebnisgastronomie 300 m untertage – das ... - RDB eV
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
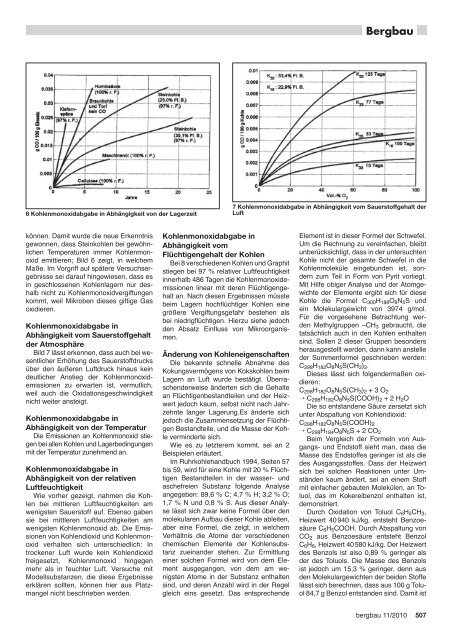
6 Kohlenmonoxidabgabe in Abhängigkeit von der Lagerzeit<br />
können. Damit wurde die neue Erkenntnis<br />
gewonnen, <strong>das</strong>s Steinkohlen bei gewöhnlichen<br />
Temperaturen immer Kohlenmonoxid<br />
emittieren; Bild 6 zeigt, in welchem<br />
Maße. Im Vorgriff auf spätere Versuchsergebnisse<br />
sei darauf hingewiesen, <strong>das</strong>s es<br />
in geschlossenen Kohlenlagern nur deshalb<br />
nicht zu Kohlenmonoxidvergiftungen<br />
kommt, weil Mikroben dieses giftige Gas<br />
oxidieren.<br />
Kohlenmonoxidabgabe in<br />
Abhängigkeit vom Sauerstoffgehalt<br />
der Atmosphäre<br />
Bild 7 lässt erkennen, <strong>das</strong>s auch bei wesentlicher<br />
Erhöhung des Sauerstoffdrucks<br />
über den äußeren Luftdruck hinaus kein<br />
deutlicher Anstieg der Kohlenmonoxidemissionen<br />
zu erwarten ist, vermutlich,<br />
weil auch die Oxidationsgeschwindig keit<br />
nicht weiter ansteigt.<br />
Kohlenmonoxidabgabe in<br />
Abhängigkeit von der Temperatur<br />
Die Emissionen an Kohlenmonoxid stiegen<br />
bei allen Kohlen und Lagerbedin gungen<br />
mit der Temperatur zunehmend an.<br />
Kohlenmonoxidabgabe in<br />
Abhängigkeit von der relativen<br />
Luftfeuchtigkeit<br />
Wie vorher gezeigt, nahmen die Kohlen<br />
bei mittleren Luftfeuchtigkeiten am<br />
wenigsten Sauerstoff auf. Ebenso gaben<br />
sie bei mittleren Luftfeuchtigkeiten am<br />
wenigsten Kohlenmonoxid ab. Die Emissionen<br />
von Kohlendioxid und Kohlenmonoxid<br />
verhalten sich unterschiedlich: In<br />
trockener Luft wurde kein Kohlendioxid<br />
freigesetzt, Kohlenmonoxid hingegen<br />
mehr als in feuchter Luft. Versuche mit<br />
Modellsubstanzen, die diese Ergebnisse<br />
erklären sollten, können hier aus Platzmangel<br />
nicht beschrieben werden.<br />
Kohlenmonoxidabgabe in<br />
Abhängigkeit vom<br />
Flüchtigengehalt der Kohlen<br />
Bei 8 verschiedenen Kohlen und Graphit<br />
stiegen bei 97 % relativer Luftfeuchtig keit<br />
innerhalb 486 Tagen die Kohlenmonoxidemissionen<br />
linear mit deren Flüchtigengehalt<br />
an. Nach diesen Ergebnissen müsste<br />
beim Lagern hochflüchtiger Kohlen eine<br />
größere Vergiftungsgefahr bestehen als<br />
bei niedrigflüchtigen. Hierzu siehe jedoch<br />
den Absatz Einfluss von Mikroorganismen.<br />
Änderung von Kohleneigenschaften<br />
Die bekannte schnelle Abnahme des<br />
Kokungsvermögens von Kokskohlen beim<br />
Lagern an Luft wurde bestätigt. Überraschenderweise<br />
änderten sich die Gehalte<br />
an Flüchtigenbestandteilen und der Heizwert<br />
jedoch kaum, selbst nicht nach Jahrzehnte<br />
langer Lagerung.Es änderte sich<br />
jedoch die Zusammensetzung der Flüchtigen<br />
Bestandteile, und die Masse der Kohle<br />
verminderte sich.<br />
Wie es zu letzterem kommt, sei an 2<br />
Beispielen erläutert.<br />
Im Ruhrkohlehandbuch 1994, Seiten 57<br />
bis 59, wird für eine Kohle mit 20 % Flüchtigen<br />
Bestandteilen in der wasser- und<br />
aschefreien Substanz folgende Analyse<br />
angegeben: 89,6 % C; 4,7 % H; 3,2 % O;<br />
1,7 % N und 0,8 % S. Aus dieser Analyse<br />
lässt sich zwar keine Formel über den<br />
molekularen Aufbau dieser Kohle ableiten,<br />
aber eine Formel, die zeigt, in welchem<br />
Verhältnis die Atome der verschiedenen<br />
chemischen Elemente der Kohlensubstanz<br />
zueinander stehen. Zur Ermittlung<br />
einer solchen Formel wird von dem Element<br />
ausgegangen, von dem am wenigsten<br />
Atome in der Substanz enthalten<br />
sind, und deren Anzahl wird in der Regel<br />
gleich eins gesetzt. Das entsprechende<br />
Bergbau<br />
7 Kohlenmonoxidabgabe in Abhängigkeit vom Sauerstoffgehalt der<br />
Luft<br />
Element ist in dieser Formel der Schwefel.<br />
Um die Rechnung zu vereinfachen, bleibt<br />
unberücksichtigt, <strong>das</strong>s in der untersuchten<br />
Kohle nicht der gesamte Schwefel in die<br />
Kohlenmoleküle eingebunden ist, sondern<br />
zum Teil in Form von Pyrit vorliegt.<br />
Mit Hilfe obiger Analyse und der Atomgewichte<br />
der Elemente ergibt sich für diese<br />
Kohle die Formel C<strong>300</strong>H188O8N5S und<br />
ein Molekulargewicht von 3974 g/mol.<br />
Für die vorgesehene Betrachtung werden<br />
Methylgruppen –CH3 gebraucht, die<br />
tatsächlich auch in den Kohlen enthalten<br />
sind. Sollen 2 dieser Gruppen besonders<br />
herausgestellt werden, dann kann anstelle<br />
der Summenformel geschrieben werden:<br />
C298H182O8N5S(CH3)2.<br />
Dieses lässt sich folgendermaßen oxidieren:<br />
C298H182O8N5S(CH3)2 + 3 O2<br />
→ C298H182O8N5S(COOH)2 + 2 H2O<br />
Die so entstandene Säure zersetzt sich<br />
unter Abspaltung von Kohlendioxid:<br />
C298H182O8N5S(COOH)2<br />
→ C298H184O8N5S + 2 CO2<br />
Beim Vergleich der Formeln von Ausgangs-<br />
und Endstoff sieht man, <strong>das</strong>s die<br />
Masse des Endstoffes geringer ist als die<br />
des Ausgangsstoffes. Dass der Heizwert<br />
sich bei solchen Reaktionen unter Umständen<br />
kaum ändert, sei an einem Stoff<br />
mit einfacher gebauten Molekülen, an Toluol,<br />
<strong>das</strong> im Kokereibenzol enthalten ist,<br />
demonstriert.<br />
Durch Oxidation von Toluol C6H5CH3,<br />
Heizwert 40 940 kJ/kg, entsteht Benzoesäure<br />
C6H5COOH. Durch Abspaltung von<br />
CO2 aus Benzoesäure entsteht Benzol<br />
C6H6, Heizwert 40 580 kJ/kg. Der Heizwert<br />
des Benzols ist also 0,89 % geringer als<br />
der des Toluols. Die Masse des Benzols<br />
ist jedoch um 15,3 % geringer, denn aus<br />
den Molekulargewichten der beiden Stoffe<br />
lässt sich berechnen, <strong>das</strong>s aus 100 g Toluol<br />
84,7 g Benzol entstanden sind. Damit ist<br />
bergbau 11/2010 507