Der Joule-Thomson-Effekt - Physikalische und Theoretische Chemie
Der Joule-Thomson-Effekt - Physikalische und Theoretische Chemie
Der Joule-Thomson-Effekt - Physikalische und Theoretische Chemie
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
p [MPa]<br />
<strong>Joule</strong>-<strong>Thomson</strong>-<strong>Effekt</strong> 6<br />
<strong>Der</strong> Term in dem das Produkt ab auftritt ist sehr klein, da zum Einen a <strong>und</strong> b klein sind <strong>und</strong><br />
zum Anderen V m groß ist. Außerdem kann näherungsweise pV m durch RT in den Korrekturgliedern<br />
ersetzt werden.<br />
pV<br />
m<br />
1 a <br />
1 b RT<br />
Vm<br />
RT <br />
<br />
(20)<br />
<br />
Ausmultiplizieren <strong>und</strong> erneutes Substituieren von pV m durch RT ergibt:<br />
20<br />
18<br />
16<br />
14<br />
12<br />
10<br />
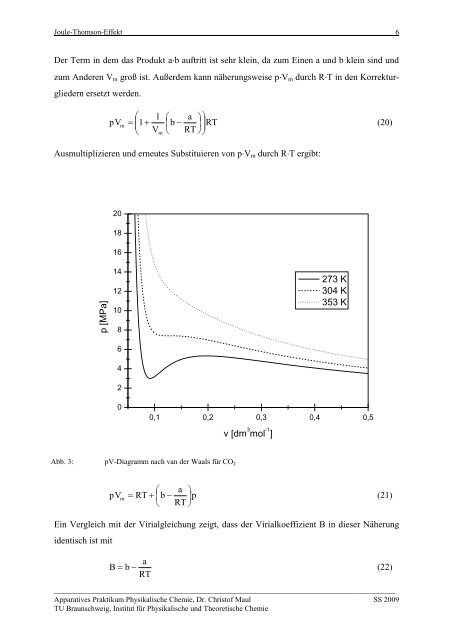
273 K<br />
304 K<br />
353 K<br />
8<br />
6<br />
4<br />
2<br />
0<br />
0,1 0,2 0,3 0,4 0,5<br />
v [dm 3 mol -1 ]<br />
Abb. 3: pV-Diagramm nach van der Waals für CO 2<br />
pV m<br />
a <br />
RT b<br />
p<br />
(21)<br />
RT <br />
Ein Vergleich mit der Virialgleichung zeigt, dass der Virialkoeffizient B in dieser Näherung<br />
identisch ist mit<br />
a<br />
B b <br />
(22)<br />
RT<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> <strong>Chemie</strong>, Dr. Christof Maul SS 2009<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> <strong>und</strong> <strong>Theoretische</strong> <strong>Chemie</strong>