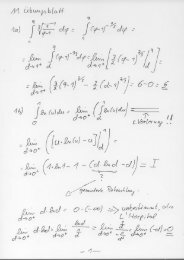Hydrolyse von Harnstoff / Michaelis-Menten-Kinetik - Physikalische ...
Hydrolyse von Harnstoff / Michaelis-Menten-Kinetik - Physikalische ...
Hydrolyse von Harnstoff / Michaelis-Menten-Kinetik - Physikalische ...
- Keine Tags gefunden...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 1<br />
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong><br />
Das Ziel dieses Versuches ist es, die mit dem <strong>Michaelis</strong>-<strong>Menten</strong>-Mechanismus verbundene<br />
<strong>Kinetik</strong> sowie eine Methode zur Bestimmung der Enzymaktivität zu erlernen. Dies soll anhand<br />
der <strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> unter Katalyse durch das Enzym Urease geschehen. Über<br />
die einfache <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> hinaus sollen außerdem der Einfluss einer Produkthemmung<br />
und des pH-Wertes kennen gelernt werden. Hierbei sind nicht die mathematischen<br />
Einzelheiten der im Anhang aufgeführten Herleitungen (sie sind nur der Vollständigkeit halber<br />
angegeben), sondern die Methodik, mit der aus komplexen Mechanismen Geschwindigkeitsgesetze<br />
abgeleitet werden (Bodensteinsches Quasistationaritätsprinzip) und theoretische<br />
Modelle ausgehend <strong>von</strong> der einfachsten Annahme durch Verfeinerung mit der Realität abgeglichen<br />
werden.<br />
Stichworte<br />
<strong>Kinetik</strong>, Reaktionsordnung, Geschwindigkeitskonstante, Reaktionsgeschwindigkeit, Gleichgewichtskonstante,<br />
pH-Wert, Enzym, Enzymaktivität, Leitfähigkeit<br />
<strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong><br />
L. Pasteur zitierte in einem Vortrag im April 1864 an der Sorbonne folgenden Ausspruch des<br />
Mediziners und Alchemisten J.B. van Helmont (1577/9 - 1644): "Das reinste Quellwasser<br />
verschimmelt und produziert Würmer, wenn sein Behälter mit dem Duft eines Fermentes imprägniert<br />
wird. Die Gerüche, die aus der Tiefe eines Sumpfes aufsteigen, produzieren Frösche,<br />
Schnecken, Blutegel, Pflanzen usw. Graben sie ein Loch in einen Ziegel, legen sie in<br />
das Loch Königskraut, decken das Loch mit einem zweiten Ziegel zu, lassen sie die zwei Ziegel<br />
an der Sonne! In einigen Tagen erscheint der Geruch des Königskrautes, der, als Ferment<br />
wirkend, die Pflanze in Skorpione verwandelt." Nach dieser mystischen und lückenhaften<br />
Versuchsanleitung ist offenbar die Funktion des Fermentes, die Lebensprozesse in Gang zu<br />
setzen, die zur Bildung der "Skorpione" führen (in der Alchemie steht der Begriff Skorpione<br />
für den Vorgang, wenn aus absterbendem, faulendem Material wieder neues Leben entsteht).<br />
Mit fortschreitender Erforschung der Lebensprozesse wurde der Begriff enger gefasst und<br />
heute ist er synonym mit "Enzym".<br />
Dies sind bestimmte Proteine, deren Aufgabe es ist, spezifische, biochemische Reaktionen zu<br />
katalysieren, was in der Regel unter sehr hoher Substrat- und Produktspezifität geschieht, d.h.,<br />
dass nur ausgewählte Edukte zu ganz bestimmten Produkten umgesetzt werden. Auf diese<br />
Weise vollzieht sich also die geheimnisvolle Steuerung der Lebensvorgänge: durch spezifische<br />
Katalyse. Der entscheidende Schritt ist dabei die Wechselwirkung des Substrats mit dem<br />
so genannten "aktiven Zentrum" des Enzyms, die dafür sorgt, dass die Energie des Über-<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 2<br />
gangszustands, der zu den gewünschten Produkten führt, erniedrigt wird (d.h. nur ein bestimmter<br />
Reaktionsweg wird eingeschlagen).<br />
Die in diesem Versuch untersuchte Reaktion ist die <strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong>,<br />
O<br />
N H 2<br />
NH 2<br />
Urease<br />
+<br />
+ 2 H 2 O<br />
2 NH 4 +<br />
O<br />
O -<br />
O -<br />
(1)<br />
die durch das Enzym Urease katalysiert wird. Zwar taucht das Enzym Urease in obiger Bruttogleichung<br />
nicht auf (hat also keinen Einfluss auf das Gleichgewicht!), dennoch hängt die<br />
Reaktionsgeschwindigkeit entscheidend <strong>von</strong> der Enzymkonzentration ab. Ein plausibler Mechanismus,<br />
mit der sich die beobachtete <strong>Kinetik</strong> beschreiben lässt, ist der <strong>Michaelis</strong>-<strong>Menten</strong>-<br />
Mechanismus, der sich in seiner einfachsten Form wie folgt darstellt:<br />
U + S<br />
k 1 k 2<br />
US<br />
U + P (2)<br />
k -1<br />
S steht hier für das Substrat, U für Urease und P für die Produkte. Im ersten Schritt wird also<br />
der Enzymsubstratkomplex US mit der Geschwindigkeitskonstanten k 1 gebildet, bzw. zerfällt<br />
mit der Geschwindigkeitskonstanten k -1 wieder in die Edukte. Im zweiten Schritt werden die<br />
Produkte in einer irreversiblen Reaktion <strong>von</strong> US und Wasser mit der Geschwindigkeitskonstanten<br />
k 2 gebildet (die Konzentration <strong>von</strong> Wasser bleibt konstant Reaktion pseudo-erster<br />
Ordnung, k 2 =k' 2 [H 2 O] 2 ).<br />
Die entsprechenden Bildungsgeschwindigkeiten der für die Herleitung des Geschwindigkeitsgesetzes<br />
interessanten Spezies ergeben sich dann wie folgt: 1<br />
d[US]<br />
= k1[S][U]<br />
− k<br />
− 1[US]<br />
− k<br />
2[US]<br />
(3)<br />
dt<br />
d[P]<br />
= k<br />
2[US]<br />
(4)<br />
dt<br />
Die Ureasekonzentration lässt sich hierbei nicht einfach aus der einfachen Bedingung<br />
m U /(M U·V) berechnen, da das Enzym je nach Qualität unterschiedlich viele aktive Zentren pro<br />
Molekül besitzt. Die Enzymqualität wird daher umgekehrt durch die mit einer bestimmten<br />
Enzymeinwaage erreichbaren Reaktionsgeschwindigkeit charakterisiert werden.<br />
Die Bildungsgeschwindigkeit v = d[P]/dt der Produkte kann durch Ermittlung <strong>von</strong> [US] unter<br />
Annahme des Bodensteinschen Stationaritätsprinzips – hierunter versteht man die Annahme,<br />
dass pro Zeiteinheit genauso viel Zwischenprodukt [US] gebildet wird, wie abgebaut wird,<br />
wodurch d[US]/dt gleich 0 wird - und der Substitution<br />
1 zur Aufstellung <strong>von</strong> Geschwindigkeitsgesetzen für einzelne Elementarschritte chemischer Reaktionen s. Lehrbücher<br />
der <strong>Physikalische</strong>n Chemie, z.B. P.W. Atkins, <strong>Physikalische</strong> Chemie, 2. Aufl. Weinheim 1996, Kap. 25<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 3<br />
bestimmt werden.<br />
[ U] = [U] − 0<br />
[US] (5)<br />
d[US]<br />
= k1 [U][S] − k<br />
− 1[US]<br />
− k<br />
2[US]<br />
= 0<br />
(6a)<br />
dt<br />
[US]<br />
k<br />
[U][S]<br />
k<br />
([U]<br />
− [US])<br />
[S]<br />
1<br />
1 0<br />
= =<br />
(6b)<br />
k<br />
2<br />
+ k<br />
− 1<br />
k<br />
2<br />
+ k<br />
−1<br />
Auflösen <strong>von</strong> Gl. 6b nach [US] und Einsetzen in Gl. 4 ergibt für die Reaktionsgeschwindigkeit<br />
v:<br />
v =<br />
d[P] k<br />
2<br />
⋅[U]<br />
0<br />
⋅[S]<br />
=<br />
dt k<br />
−1<br />
+ k<br />
2<br />
[S] +<br />
k<br />
1<br />
Gl. 7 ist als <strong>Michaelis</strong>-<strong>Menten</strong>-Gleichung bekannt und beschreibt die Bildungsgeschwindigkeit<br />
der Produkte in Abhängigkeit der momentanen <strong>Harnstoff</strong>konzentration und der eingesetzten<br />
Konzentration des Enzyms. Die Größe ( k -1 +k 2 )/k 1 wird zu einer Konstanten, der <strong>Michaelis</strong>-<strong>Menten</strong>-Konstante<br />
K M zusammengezogen.<br />
K<br />
k<br />
+ k<br />
1 2<br />
M<br />
= − (8)<br />
k1<br />
Da die Konzentration [S] zum Zeitpunkt t=0 durch die Einwaage an <strong>Harnstoff</strong> festgelegt ist,<br />
können die Konstanten K M und k 2 durch Messung der Anfangsgeschwindigkeit v 0 ermittelt<br />
werden.<br />
v<br />
0<br />
⎛ d[P] ⎞<br />
= ⎜ ⎟<br />
⎝ dt ⎠<br />
t = 0<br />
k<br />
2[U]<br />
0[S]<br />
=<br />
[S] + K<br />
0<br />
M<br />
0<br />
In Abb.1 sind nach Gl. 7 berechnete Werte (Einheiten willkürlich, K M /(k 2 [U] 0 ) = 13,33) für<br />
die Reaktionsgeschwindigkeit in Abhängigkeit <strong>von</strong> der Substratkonzentration aufgetragen.<br />
Betrachtet man den Grenzwert<br />
⎛ d[P] ⎞<br />
lim ⎜ ⎟ = k<br />
2[U]<br />
0<br />
= v<br />
[S] →∞⎝<br />
dt ⎠<br />
max<br />
so sieht man, dass durch für eine Substratkonzentration [S] = K M in Gl. 9 v = d[P]/dt den Wert<br />
v max /2 annimmt.<br />
Das Geschwindigkeitsgesetz (7), das zu dem <strong>Michaelis</strong>-<strong>Menten</strong>-Mechanismus gehört, stellt<br />
einen fließenden Übergang <strong>von</strong> einer <strong>Kinetik</strong> erster Ordnung zu einer <strong>Kinetik</strong> nullter Ordnung<br />
dar. Anschaulich lässt sich dies wie folgt erklären:<br />
I) Ist im Verhältnis zum Substrat sehr viel Enzym vorhanden, so wird die Enzymkonzentration<br />
kaum durch die Bildung des Substratkomplexes verringert. In der Folge<br />
(7)<br />
(9)<br />
(10)<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 4<br />
nimmt auch die Bildungsgeschwindigkeit <strong>von</strong> P zu, die linear <strong>von</strong> der Konzentration<br />
[US] abhängt.<br />
II)<br />
Wenn allerdings die Substratkonzentration so hoch wird, dass wenig freies Enzym<br />
übrig ist, so hängt die Reaktionsgeschwindigkeit nur noch <strong>von</strong> der Menge des eingesetzten<br />
Enzyms ab und nicht mehr <strong>von</strong> der Substratkonzentration. Das ist genauso, wie<br />
an der Supermarktkasse, wenn alle Kassen besetzt sind. Dann kommt es auch nur auf<br />
die Arbeitsgeschwindigkeit oder „Turn-Over-Frequenz“ der Kassiererinnen an, wie<br />
viele Leute pro Zeiteinheit durchgeschleust werden können.<br />
Abbildung 1:<br />
Darstellung der <strong>Michaelis</strong>-<strong>Menten</strong>-Gleichung (Gl. 7): Abhängigkeit der Produktbildungsgeschwindigkeit<br />
v <strong>von</strong> der Substratkonzentration<br />
Die durch Gl. 10 definierte Maximalgeschwindigkeit kann als Maß für die katalytische Aktivität<br />
A der Urease verwendet werden. Diese ist definiert als die Menge an Ammoniak in mol,<br />
die pro mg Enzym bei einer bestimmten Temperatur (oft 25 oder 30°C) und einem bestimmten<br />
pH (pH6,1 oder pH7) maximal pro Minute gebildet wird (Angabe in U mg -1 : ein U entspricht<br />
1µmol NH 3 pro Minute).<br />
v<br />
max<br />
⋅ VLösung<br />
A = (11)<br />
m<br />
Enzym<br />
Im Hauptteil des Versuchs wird die Anfangsgeschwindigkeit der Reaktion (diese ist nicht<br />
durch die nicht-kompetitive Produkthemmung beeinflusst, s.u.) dazu verwendet, um die Parameter<br />
K M und v max zu ermitteln. Hierzu ist es hilfreich, die reziproke Form <strong>von</strong> Gl. 9 zu<br />
verwenden<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 5<br />
1<br />
v<br />
1 K 1<br />
= + ⋅<br />
(12)<br />
M<br />
0<br />
v<br />
max<br />
v<br />
max<br />
[S]<br />
0<br />
und dementsprechend 1/v 0 gegen 1/[S] 0 aufzutragen (so genannter Lineweaver-Burk-Plot).<br />
Aus dem Achsenabschnitt erhält man v max , mit dessen Hilfe man dann K M aus der Steigung<br />
der Ausgleichsgeraden ermitteln kann.<br />
pH-Abhängigkeit der <strong>Harnstoff</strong>hydrolyse<br />
Ein wichtiger Punkt bei der <strong>Harnstoff</strong>hydrolyse ist der pH-Wert der Lösung. Führt man die<br />
Experimente in einer ungepufferten Lösung aus, so stellt sich nach einiger Zeit der pH-Wert<br />
für den Ammoniumcarbonat-Puffer ein. Die Aktivität der Urease hängt aber entscheidend<br />
vom pH-Wert ab. Optimal wäre ein pH <strong>von</strong> 7,01 [1] (s.u.). Die Beeinträchtigung der Aktivität<br />
lässt sich mit folgendem Mechanismus beschreiben: [2]<br />
UH 2<br />
UH 2<br />
S<br />
K E,1<br />
k 1 k<br />
UH - + S UHS - 2<br />
UH - + P<br />
K<br />
k -1 E,2<br />
U 2-<br />
K ES,2<br />
US 2- K ES,1<br />
Abbildung 2: Mechanismus der pH-abhängigen <strong>Harnstoff</strong>hydrolyse nach Trypton und Dixon [2]<br />
Die aktive Spezies des Enzyms ist damit das amphotere Anion einer zweibasigen Säure. Die<br />
Behandlung dieses Mechanismus unter der Bedingung eines stabilen Zwischenzustandes für<br />
UHS - liefert für die Größen v max und K M in Abhängigkeit der Gleichgewichtskonstanten<br />
(Herleitung siehe Anhang):<br />
*<br />
*<br />
k<br />
2[U]<br />
0<br />
v<br />
max<br />
v<br />
max<br />
= k<br />
2[U]<br />
0<br />
=<br />
=<br />
(13)<br />
+<br />
[H ] K<br />
ES,2 f ( pH)<br />
1+<br />
+<br />
+<br />
K [H ]<br />
ES,1<br />
K<br />
M<br />
+<br />
[H ] K<br />
E,2<br />
1+<br />
+<br />
+<br />
K<br />
*<br />
E,1 [H ]<br />
= K<br />
M<br />
(14)<br />
+<br />
[H ] K<br />
ES,2<br />
1+<br />
+<br />
+<br />
K [H ]<br />
ES,1<br />
v* max ist die (hypothetische) Maximalgeschwindigkeit für den Fall, dass alle Enzymmoleküle<br />
in der einfach protonierten Form vorliegen würden, während v max die im Experiment erzielbare<br />
Maximalgeschwindigkeit für einen gegebenen pH-Wert darstellt.<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 6<br />
Es wird gefunden, dass die jeweiligen Konstanten K E und K ES gleich sind, was bedeutet, dass<br />
die Anbindung des Substrates keinen Einfluss auf die Säure-Base Eigenschaften des Enzyms<br />
hat. Dies hat ebenfalls zur Folge, dass sich K M nicht mit dem pH ändert. Fidaleo und Lavecchia<br />
geben die Werte mit pK 1 =6,12 und pK 2 =7.9 an. (Warum ist dann ein pH-Wert <strong>von</strong> 7.01<br />
optimal für die <strong>Harnstoff</strong>hydrolyse?) Die Werte können benutzt werden, um z.B. die Aktivität<br />
bei einem beliebigen pH zu berechnen, da die Experimente in ungepufferter Lösung durchgeführt<br />
werden.<br />
Produkthemmung<br />
Verwendet man die aus den gemessenen Anfangsgeschwindigkeiten ermittelten Parameter des<br />
<strong>Michaelis</strong>-<strong>Menten</strong>-Mechanismus und versucht damit den Konzentrationsverlauf über die Zeit<br />
zu beschreiben, so tritt ein weiterer Gesichtspunkt des eigentlichen Mechanismus zu Tage.<br />
Hierzu wird zunächst die <strong>Michaelis</strong>-<strong>Menten</strong>-Gleichung mit der Anfangsbedingung<br />
t=0[S]=[S] 0 integriert (Herleitung siehe Anhang).<br />
[P]<br />
() t<br />
= [S]<br />
0<br />
− K<br />
M<br />
⎛<br />
⎜ e<br />
⎜<br />
⋅ W⎜<br />
⎜<br />
⎜<br />
⎝<br />
vmaxt<br />
−<br />
K M<br />
⎛<br />
+ ln⎜<br />
⎜<br />
⎝<br />
K<br />
[] S<br />
M<br />
0<br />
e<br />
[S] 0<br />
KM<br />
⎞ ⎞<br />
⎟ ⎟<br />
⎟ ⎟<br />
⎠ ⎟<br />
(15)<br />
⎟<br />
⎟<br />
⎠<br />
Die Funktion W ist dabei die Lambert-Funktion, die als Umkehrfunktion der Beziehung<br />
f<br />
( W) W ⋅ e<br />
W<br />
= (16)<br />
definiert und z.B. als Funktion ProductLog im Programmpaket Mathematica ® integriert ist<br />
Ein Nachteil der Methode der Anfangsgeschwindigkeit zur Aufklärung der <strong>Kinetik</strong> bzw. des<br />
Mechanismus ist die Tatsache, dass der Einfluss der Produktkonzentration auf die Reaktionsgeschwindigkeit<br />
nicht berücksichtigt wird, da diese ja am Anfang sehr klein ist. Es gibt mehrere<br />
mögliche Mechanismen für die Produkthemmung. Der für die <strong>Harnstoff</strong>hydrolyse durch<br />
Urease relevante Mechanismus ist der so genannte nicht-kompetitive Mechanismus (s.<br />
Abb.3).<br />
Sowohl das freie Enzym, wie auch der Enzym-Substrat-Komplex reagieren mit dem Produkt<br />
zu einem inaktiven Komplex. Das Substrat konkurriert nicht mit dem Produkt um freie Bindungsstellen,<br />
sondern P reagiert mit jeder Form des Enzyms in gleichem Maße und deaktiviert<br />
dieses. Die Gleichgewichtsbedingungen werden durch eine gemeinsame Dissoziationskonstante<br />
K p beschrieben, in der alle Formen <strong>von</strong> U vorkommen:<br />
([U]<br />
+ [US])<br />
[P]<br />
K P<br />
= (17)<br />
[UP] + [UPS]<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 7<br />
k 1<br />
k 2<br />
U + S US U + P<br />
k -1<br />
P<br />
P<br />
UP<br />
UPS<br />
Abbildung 3:<br />
Nicht-kompetitive Produkthemmung<br />
Das Geschwindigkeitsgesetz für diesen Mechanismus lässt sich durch Gl. 18 angeben (wiederum<br />
wird ein stationärer Zwischenzustand angenommen, Herleitung siehe Anhang).<br />
d[P]<br />
dt<br />
=<br />
v<br />
max<br />
[S]<br />
⎛ [P] ⎞<br />
+<br />
( K ) ⎜<br />
⎟ M + [S] 1<br />
⎝ K<br />
p ⎠<br />
Für kleine Produktkonzentrationen geht Gl. 18 in Gl. 7 über. Eine Methode, die Produkthemmung<br />
zu studieren, wäre zum Beispiel der Zusatz einer bestimmten Menge an Produkt, um<br />
den Effekt zu untersuchen, den die auf die Anfangsgeschwindigkeit hat. Sind die Parameter<br />
K M und v max schon bekannt, so kann K p (1,22±0,11 10 -2 mol/l) auch mit der Methode der Anfangsgeschwindigkeiten<br />
durch eine solche Messreihe bestimmt werden. Aus Zeitgründen soll<br />
hier aber ein anderer Weg eingeschlagen werden, der sich der integralen Konzentrations-Zeit-<br />
Kurve bedient. Der Einfluss der Produktkonzentration wird dabei halbquantitativ bestimmt.<br />
Hierzu werden jetzt zwei Gleichungen benötigt, da die Produktbildung und die Eduktabnahme<br />
miteinander gekoppelt sind (auftauchen <strong>von</strong> [P] in Gl. 18). Die zweite Gleichung ergibt sich<br />
wiederum aus dem Bodensteinschen Stationaritätsprinzip, da ja dann gerade soviel Produkt<br />
gebildet wird, wie Edukt verbraucht wird. Das Differentialgleichungssystem ist dann einfach<br />
durch (19) gegeben und lässt sich numerisch lösen.<br />
d[P] d[S]<br />
= −<br />
(19)<br />
dt dt<br />
Im konkreten Fall muss man noch die stöchiometrischen Verhältnisse berücksichtigen. Es<br />
werden zum Beispiel zwei Einheiten Ammoniak und eine Einheit CO 2 pro Formelumsatz gebildet.<br />
Betrachtet man Ammoniumcarbonat allerdings als das eigentliche Produkt, so liegen<br />
die Verhältnisse wieder 1:1 und Gl. 19 enthält automatisch den richtigen stöchiometrischen<br />
Koeffizienten.<br />
(18)<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 8<br />
Leitfähigkeit <strong>von</strong> Elektrolyten<br />
Die Konzentrationsmessungen erfolgen indirekt durch Messung der spezifischen Leitfähigkeit<br />
der Lösung. Die ionische Leitfähigkeit der Elektrolyte unterscheidet sich wesentlich <strong>von</strong> der<br />
elektronischen Leitfähigkeit der Metalle. Für den reinen Ladungstransport, der in Elektrolyten<br />
durch positive und negative Ionen bzw. in Metallen durch Elektronen getragen wird, lassen<br />
sich jedoch gleiche elektrische Grundgrößen definieren. Ist L die Länge und F der Querschnitt<br />
eines Elektrodengefäßes, so liefert das Ohmsche Gesetz für den Widerstand R dieses Leiters,<br />
wenn U die angelegte Spannung und I den sich einstellenden Strom bedeuten:<br />
R = U/I = L / (κF) (20)<br />
Im Gegensatz zu metallischen Leitern gilt Gl. 20 in Elektrolytlösungen nur für hochfrequenten<br />
Wechselstrom (mit Frequenzen ≥ 1 kHz), da sonst Elektrolyse- und Polarisationseffekte<br />
an den Elektroden auftreten. Die Größe L/F ist die Zellkonstante und wird meist in cm -1 angegeben.<br />
κ ist die spezifische Leitfähigkeit mit der SI-Einheit S/m = (Ωm) −1 . Die molare Leitfähigkeit<br />
(molar conductivity) Λ m ist die auf die Konzentration c bezogene spezifische Leitfähigkeit<br />
Λ m = κ/c (21)<br />
Ein Elektrolyt, der in zwei Ionensorten zerfällt, und zwar in ν + Kationen der Ladungszahl z +<br />
und ν − Anionen der Ladungszahl z − , besitzt die elektrochemische Wertigkeit ν = ν + z + = ν − z − ,<br />
die die molare Leitfähigkeit Λ m mit der Äquivalentleitfähigkeit Λ eq verknüpft:<br />
Λ eq = Λ m /ν = κ/(νc) (22)<br />
Anhand der molaren Leitfähigkeit ihrer Lösungen werden Elektrolyte als stark oder schwach<br />
klassifiziert: Ein starker Elektrolyt ist eine Substanz, deren molare Leitfähigkeit in Lösung nur<br />
wenig <strong>von</strong> der Konzentration abhängt. Ein schwacher Elektrolyt besitzt bei sehr niedrigen<br />
Konzentrationen eine ähnliche molare Leitfähigkeit wie ein starker Elektrolyt, die jedoch für<br />
zunehmende Konzentrationen sehr schnell auf kleine Werte abfällt. Das Verhalten schwacher<br />
Elektrolyte lässt sich auf der Basis des Gleichgewichts zwischen der Substanz und ihren Ionen<br />
in Lösung erklären: Der Dissoziationsgrad α, der den in Lösung dissoziiert vorliegenden Anteil<br />
einer Substanz angibt, nimmt zu, wenn die Konzentration verringert wird. Starke Elektrolyten<br />
dagegen liegen in Lösung immer vollständig dissoziiert vor (α = 1).<br />
Da die molare Leitfähigkeit Λ m = Λ m (c) selbst konzentrationsabhängig ist, findet man keine<br />
Proportionalität zwischen κ und c, wie Gleichung (21) nahe legt. Lediglich für den Grenzfall<br />
der unendlich verdünnten Lösung strebt Λ m einem festen Grenzwert zu. Man bezeichnet diesen<br />
Wert als molare Grenzleitfähigkeit (limiting molar conductivity) Λ 0 m bei unendlicher<br />
Verdünnung. Er beinhaltet keine interionischen Wechselwirkungen mehr. Für starke Elektrolyten<br />
sind Λ m und c im Bereich kleiner Konzentrationen c nach experimentellen Ergebnissen<br />
<strong>von</strong> Kohlrausch durch ein Quadratwurzelgesetz miteinander verknüpft:<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 9<br />
Λ m = Λ 0 m - A c ½ (23)<br />
Durch die Auftragung <strong>von</strong> Λ m gegen c ½ erhält man Λ 0 m aus dem Ordinatenabschnitt und A<br />
aus der Steigung der Geraden. Beziehung (23) ergibt sich auch aus der Debye-Hückel-Theorie<br />
der Ionenwanderung, die auf einer Modellvorstellung für ionische Lösungen beruht, nach der<br />
jedes Ion <strong>von</strong> einer entgegengesetzt geladenen Ionenwolke umgeben ist, die sich aus dem<br />
Wechselspiel zwischen der anziehenden Wirkung der Ladung des Zentralions und der für die<br />
Lösung charakteristischen thermischen Bewegung ergibt (s. Skript zur Elektrochemie). Die<br />
Abnahme der molaren Leitfähigkeit mit erhöhter Konzentration ist 1) auf eine asymmetrische<br />
Verzerrung der Ionenwolke bei der Wanderung mit einhergehender Verschiebung der Ladungsschwerpunkte<br />
vom Ionenwolke und Zentralion (Asymmetrieeffekt) und 2) auf die erhöhte<br />
Viskosität durch die entgegengesetzten Bewegungsrichtungen <strong>von</strong> Zentralion und Ionenwolke<br />
(elektrophoretischer Effekt) zurückzuführen.<br />
Nach dem Gesetz der unabhängigen Ionenwanderung ergibt sich die molare Grenzleitfähigkeit<br />
Λ 0 m bei unendlicher Verdünnung aus der Summe der Ionenleitfähigkeiten Λ, d.h. der mit<br />
den stöchiometrischen Faktoren ν gewichteten molaren Grenzionenleitfähigkeiten λ<br />
Λ 0 m = Λ + + Λ − = ν + λ + + ν − λ − (24)<br />
Diese sind wie Λ m und κ relativ stark temperaturabhängig, so dass es erforderlich ist, während<br />
der Messung für Temperaturkonstanz zu sorgen. Das Gesetz der unabhängigen Ionenwanderung<br />
ermöglicht es, für einen beliebigen Elektrolyten (zumindest bei unendlicher Verdünnung)<br />
die molare Leitfähigkeit Λ m aus den bekannten Ionenleitfähigkeiten λ zu berechnen.<br />
Insbesondere können Grenzleitfähigkeiten schwacher Elektrolyte, die einer direkten Messung<br />
nicht zugänglich sind, aus den Grenzleitfähigkeiten starker Elektrolyte berechnet werden. Für<br />
die Grenzleitfähigkeit <strong>von</strong> Essigsäure ergibt sich beispielsweise:<br />
Λ 0 m (CH 3 COOH) = Λ 0 m (CH 3 COONa) + Λ 0 m (HCl) − Λ 0 m (NaCl)<br />
Das Quadratwurzelgesetz (23) versagt für schwache Elektrolyte, weil diese nur teilweise dissoziieren<br />
(α < 1). Vernachlässigt man interionische Wechselwirkungen (für kleine Werte <strong>von</strong><br />
α zulässig), so bestimmt der Dissoziationsgrad alleine die Abnahme der molaren Leitfähigkeit:<br />
Λ m = αΛ m<br />
0<br />
(25)<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 10<br />
1) Bereitstellung der Lösungen<br />
a) Ammoniumcarbonat<br />
Aufgabenstellung<br />
Stellen Sie zunächst 100ml einer 0,01 M <strong>Harnstoff</strong>lösung her und versetzen Sie sie<br />
mit 50 mg Urease. Überlassen Sie die Lösung auf einem Magnetrührer bis zum<br />
Ende des Messtages sich selbst.<br />
b) Herstellung der Verdünnungsreihe einer <strong>Harnstoff</strong>lösung/Ureaselösung<br />
2) Messungen<br />
Stellen Sie ausgehend <strong>von</strong> 250 ml einer 0,1 M <strong>Harnstoff</strong>lösung eine Verdünnungsreihe<br />
mit je 100ml der Konzentrationen {0.5·10 -3 , 1·10 -3 , 1.5·10 -3 , 2·10 -3 , 3·10 -3 ,<br />
4·10 -3 , 6·10 -3 , 8·10 -3 , 1·10 -2 , 1.2·10 -2 } mol/l her. Die Konzentration 1·10 -2 mol/l soll<br />
zweimal hergestellt werden. Wiegen Sie 150 mg Urease ab und lösen Sie sie in<br />
150 ml Wasser.<br />
Die Messgröße, mit der die Ammoniumcarbonatkonzentration zeitaufgelöst gemessen<br />
wird, ist die Leitfähigkeit der Lösung. Diese ist im betreffenden Konzentrationsbereich<br />
in sehr guter Näherung proportional zur Ionenkonzentration (im Allgemeinen ist sie dies<br />
natürlich nicht, da die molare Leitfähigkeit mit der Wurzel der Konzentration abnimmt:<br />
Kohlrausch’sches Quadratwurzelgesetz!).<br />
a) Nehmen Sie am Schreiber folgende Einstellungen vor: 6 Skalenteile(Skt.)/min,<br />
100 mV/Skt. Füllen Sie jeweils 100 ml der <strong>Harnstoff</strong>lösungen in das temperierte<br />
(25°C) Reaktionsgefäß und hängen Sie die pH- und die Leitfähigkeitselektrode<br />
hinein. Achten Sie hierbei darauf, dass die Leitfähigkeitselektrode am Rand des<br />
Gefäßes hängt und so tief wie möglich in die Lösung eintaucht.<br />
Schalten Sie den Schreiber ein und fügen Sie unter Rühren 10 ml der Ureaselösung<br />
hinzu, um die Reaktion zu starten. Nehmen Sie die Spannungskurve für ca. 60 s<br />
auf und notieren Sie den pH-Wert simultan (am besten direkt an die Kurve schreiben).<br />
Am Ende einer Messung sollten Reaktionsgefäß, Elektroden und Rührer gut<br />
gespült werden.<br />
b) Füllen Sie die (zweite) Lösung mit 1·10 -2 mol/l <strong>Harnstoff</strong> in das Reaktionsgefäß<br />
und nehmen Sie die Spannungskurve etwa 80-90 Minuten lang auf. Ändern Sie die<br />
Schreibereinstellungen auf 1V/Skt. bzw. 1 Skt./min. Notieren Sie ebenfalls den<br />
pH-Wert in regelmäßigen Abständen.<br />
c) Zur Kalibrierung: Messen Sie die Leitfähigkeit bzw. den Schreiberausschlag der<br />
unter 1a) bereiteten Ammoniumcarbonatlösung, indem Sie ausgehend <strong>von</strong> 100 ml<br />
destilliertem Wasser in mehreren Schritten je 2 ml zugeben und den Schreiberaus-<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 11<br />
schlag nach Einstellen eines konstanten Leitfähigkeitswertes dokumentieren. Hierbei<br />
bietet sich auch die Möglichkeit die Mischzeit abzuschätzen, vor deren Ablauf<br />
die Auswertung der Steigung der unter a) aufgenommenen Kurven in jedem Falle<br />
nicht ratsam ist.<br />
3) Auswertung<br />
a) Tragen Sie die vom Schreiber unter 2c) angezeigten Spannungswerte in einem<br />
Diagramm gegen die jeweilige Konzentration der Lösung auf und ermitteln Sie<br />
den Kalibrierfaktor mittels linearer Regression.<br />
b) Bestimmen sie die Konstanten v max , K M , k 2 und die Aktivität des Enzyms sowie die<br />
jeweils dazugehörigen Fehler aus den Anfangssteigungen v 0 und der zugehörigen<br />
<strong>Harnstoff</strong>konzentration [S] 0 der unter 2a) aufgenommen Kurven zunächst ohne<br />
den pH-Wert zu berücksichtigen (Lineweaver-Burk-Plot, Gl. 12). Zur Ermittlung<br />
der Anfangssteigung verwerfen sie etwa die ersten 20 Sekunden, da so lange etwa<br />
die Mischzeit beträgt!<br />
c) Ermitteln Sie mit einem geeigneten Mittelwert des pH-Wertes die Konstanten<br />
v max * und k 2 *, indem Sie die ermittelten Konstanten v max und k 2 um den Faktor<br />
f(pH) korrigieren (Gl. 13). Berechnen sie die Aktivität des Enzyms (in U/mg) unter<br />
den Bedingungen (pH, Temperatur), die auf der Flasche angegeben sind (bei<br />
30°C ist die Reaktion ca. um den Faktor 1,25 schneller als bei 25°C). Beachten sie,<br />
dass sie eventuell v max * noch durch den entsprechenden pH-Faktor für die Angabe<br />
auf der Flasche teilen müssen. Ermitteln Sie auch hier den Fehler und vergleichen<br />
Sie die Ergebnisse mit der Angabe auf der Flasche!<br />
d) In diesem Teil der Auswertung geht es darum, die aufgenommene Konzentrations-<br />
Zeit-Kurve mit Daten zu vergleichen, die nach den im Theorieteil vorgestellten<br />
Modellen berechnet werden. Dies geschieht mit dem Programm Mathematica ® ,<br />
das auf den Auswerterechnern im Praktikum installiert ist. Ein vorgefertigtes Sheet<br />
liegt auf dem Desktop und man braucht nur noch einzelne Werte einzufügen (siehe<br />
Anleitung in Anhang 4).<br />
Übertragen sie zunächst die unter 2b) aufgenommene Spannungskurve in eine<br />
Konzentrations-Zeit-Kurve (Intervall <strong>von</strong> 2 Minuten) und erstellen sie hieraus eine<br />
ASCII-Datei mit dem Namen Daten1.DAT. Hierzu kann man einfach in Origin ®<br />
die betreffenden Spalten auswählen und die Datei mit DateiExportierenASCII<br />
erstellen, oder in Excel ® DateiSpeichern unter Dateityp (Unicode) .txt. Das<br />
Dezimaltrennzeichen muss der Punkt sein. Dies geht am einfachsten, wenn man<br />
die ASCII-Datei mit WordPad öffnet und unter BearbeitenErsetzen die gewünschte<br />
Änderung vornimmt.<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 12<br />
Auf den Auswerterechnern im Praktikum liegt die Datei <strong>Harnstoff</strong>.nb bereit. Kopieren<br />
sie einfach die <strong>von</strong> ihnen erstellte ASCII-Datei Daten1.DAT auf den Desktop<br />
und folgen sie den Anweisungen in Anhang IV. Sie erhalten drei neue Dateien,<br />
mit den Namen ohnepH.DAT, mitpH.DAT und komplett.DAT. Diese können sie<br />
mit Excel oder Origin öffnen und graphisch darstellen. Sie enthalten berechnete<br />
Daten der Konzentration in mol/l in Abhängigkeit <strong>von</strong> der Zeit in Minuten. "ohnepH.DAT"<br />
wurde nach Gl. 15 und den Daten aus 3b) "mitpH.DAT" ebenfalls<br />
nach Gl. 15 aber mit den Daten aus 3c) und "komplett.DAT" nach dem allgemeinen<br />
Zusammenhang Gl. 18/19 numerisch berechnet.<br />
4) Diskussion<br />
Vergleichen sie die unter 3c) erhaltenen Werte mit Literaturdaten (Angabe auf der Flasche)<br />
und diskutieren sie etwaige Abweichungen. Wie genau schätzen sie die Meßmethode<br />
ein (qualitativ) und welche Verbesserungen würden sie vornehmen, um zu genaueren<br />
Messungen zu gelangen. Ist die Leitfähigkeitsmessung gut geeignet, um die<br />
Konzentration des Produktes zu verfolgen (Abweichung bei der Kalibrierung, Zeitauflösung)?<br />
Welche Probleme ergeben sich, wenn man die Messungen unter konstanten pH-<br />
Bedingungen durchführen will und wie könnte man diese lösen (Leitfähigkeit, selektiverer<br />
Nachweis des Produktes)?<br />
Stellen sie die unter 3d) gemessene Konzentrations-Zeit-Kurve zusammen mit den berechneten<br />
Kurven graphisch dar. Welche Aussage lässt sich treffen? Welche Vorteile/Nachteile<br />
hat die Methode der Anfangsgeschwindigkeiten hinsichtlich der Ermittlung<br />
<strong>von</strong> Reaktionsmechanismen? Wie stark ist der Einfluss des pH-Wertes und der Produkthemmung<br />
(qualitativ)? Wie genau wird die experimentelle Kurve durch die Modellfunktion<br />
unter Berücksichtigung <strong>von</strong> pH- und Produktabhängigkeit der Geschwindigkeit beschrieben<br />
und wie erklären sie sich eine eventuelle Abweichung (beziehen sie hierzu die<br />
<strong>von</strong> ihnen während der Messung notierten pH-Werte mit in ihre Überlegungen ein)?<br />
Literatur<br />
[1] M. Fidaleo, R. Lavecchia, Kinetic Study of Enzymatic Urea Hydrolysis Kinetic<br />
Study of Enzymatic Urea Hydrolysis in the pH Range 4–9, Chem. Biochem. Eng. Q. 17<br />
(4) 311–318 (2003)<br />
[2] Tipton K. F., Dixon H. B. F., Methods Enzymol. 63, (1979), 183<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 13<br />
I) Herleitung der pH-Abhängigkeit<br />
Anhang<br />
Ziel der Ableitung ist, die Konzentration der Übergangsspezies UHS - unter der Annahme eines<br />
stationären Zustandes zu bestimmen, da sich die Produktbildungsgeschwindigkeit als<br />
d[P]<br />
−<br />
= k<br />
2[UHS<br />
]<br />
(A1)<br />
dt<br />
schreiben lässt. Die Behandlung nach dem Bodensteinschen Quasistationaritätsprinzip ergibt<br />
zunächst den zu Gl. 6 analogen Ausdruck:<br />
−<br />
− [UH ][S]<br />
[UHS ] = (A2)<br />
K M<br />
Des Weiteren muss man nun die unbekannte Konzentration des freien [UH - ] durch die eingesetzte<br />
Konzentration [U] 0 ausdrücken. Dazu werden die (bekannten) Gleichgewichtskonstanten<br />
der beiden Säure-Base Gleichgewichte verwendet:<br />
[UH<br />
−<br />
] = [U]<br />
0<br />
−[UH<br />
] −[U<br />
2<br />
2−<br />
−<br />
2−<br />
] −[UHS<br />
] −[UH<br />
S] −[US<br />
]<br />
Ausdrücken der unbekannten Konzentrationen durch die Dissoziationskonstanten, die Hydroniumionenkonzentration,<br />
[UH - ] und [UHS - ] liefert:<br />
[UH<br />
−<br />
2<br />
(A3)<br />
− +<br />
−<br />
− +<br />
−<br />
[UH ][H ] [UH ]K<br />
E,2<br />
[UH ][H ] [UHS ]K<br />
−<br />
ES,2<br />
] = [U]<br />
0<br />
−<br />
− −[UHS<br />
] −<br />
−<br />
(A4)<br />
+<br />
+<br />
K [H ]<br />
K<br />
[H ]<br />
E,1<br />
Einsetzen <strong>von</strong> Gl. A2 ergibt:<br />
⎛ +<br />
⎛<br />
+<br />
⎞⎞<br />
−<br />
= − ⎜[H<br />
] K<br />
E,2 S<br />
⎜<br />
[H ] K<br />
ES,2<br />
[UH ] [U] −<br />
+ +<br />
⎟⎟<br />
0<br />
[UH ]<br />
⎜<br />
+ + 1<br />
+<br />
(A5)<br />
⎟<br />
⎝<br />
K [H ] K ⎝ K [H<br />
+<br />
E,1<br />
M ES,1<br />
] ⎠⎠<br />
Benutzt man nun wiederum Gl. A2, um [UHS - ] in Gl. A1 durch [UH - ] zu ersetzen, erhält man<br />
d[P]<br />
dt<br />
=<br />
⎛<br />
⎜<br />
[H<br />
1+<br />
⎝ K<br />
+<br />
] K<br />
+<br />
[H<br />
woraus unmittelbar die Gln. 13 und 14 folgen.<br />
K<br />
M<br />
E,1<br />
k<br />
2<br />
E,2<br />
+<br />
[U]<br />
0<br />
[S]<br />
⎞ ⎛<br />
⎟ + ⎜<br />
[H<br />
S<br />
]<br />
⎠ ⎝ K<br />
+<br />
ES,1<br />
] K<br />
+<br />
[H<br />
ES,1<br />
ES,2<br />
+<br />
⎞<br />
+ 1⎟<br />
]<br />
⎠<br />
(A6)<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 14<br />
II) Herleitung der Konzentrations-Zeit-Funktion<br />
Ausgangspunkt für die Herleitung ist das Geschwindigkeitsgesetz Gl. 7:<br />
d[P]<br />
dt<br />
v [S]<br />
[S] + K<br />
max<br />
= (A7)<br />
M<br />
Unter der Bedingung eines stationären Zwischenzustandes erhält kann man die Abnahmegeschwindigkeit<br />
des Substrats durch Bildungsgeschwindigkeit der Produkte ausdrücken.<br />
d[S]<br />
dt<br />
d[P]<br />
dt<br />
v [S]<br />
[S] + K<br />
max<br />
= − = −<br />
(A8)<br />
M<br />
Ist die Funktion [S](t) nun im betrachteten Bereich stetig, eindeutig und streng monoton (die<br />
ersten beiden Bedingungen sollten immer erfüllt sein und für die dritte ist erfüllt, weil die<br />
Konzentration <strong>von</strong> <strong>Harnstoff</strong> ständig abnimmt), so kann man die Ableitung der Umkehrfunktion<br />
t([S]) folgendermaßen schreiben:<br />
dt<br />
d[S]<br />
⎛ d[S] ⎞<br />
= ⎜ ⎟<br />
⎝ dt ⎠<br />
−1<br />
K<br />
M<br />
= − −<br />
v [S]<br />
max<br />
1<br />
v<br />
max<br />
(A9)<br />
Diese lässt sich sofort integrieren, wodurch man erhält:<br />
K [S]<br />
= ([S]<br />
) − C1<br />
(A10)<br />
v v<br />
M<br />
t − ln +<br />
max<br />
max<br />
Elementare Umformung ergibt dann:<br />
− v<br />
max<br />
K<br />
t + C<br />
M<br />
2<br />
= ln<br />
[S]<br />
K<br />
([S]<br />
) + mit C<br />
2<br />
= v<br />
maxC1<br />
M<br />
(A11)<br />
Dies kann man alsdann auch schreiben als<br />
e<br />
was für [S](t) ergibt:<br />
−vmaxt+<br />
C<br />
K<br />
K<br />
M<br />
M<br />
2<br />
=<br />
[S]<br />
K<br />
M<br />
e<br />
[S]<br />
K<br />
M<br />
(A12)<br />
[S](t) = K<br />
M<br />
⎧<br />
⎪e<br />
W⎨<br />
⎪<br />
⎩<br />
−v<br />
max<br />
K<br />
K<br />
t+<br />
C<br />
M<br />
M<br />
2<br />
⎫<br />
⎪<br />
⎬<br />
⎪<br />
⎭<br />
(A13)<br />
Um zu Gl. 15 zu gelangen, muss man noch die Integrationskonstante C 2 bestimmen. Diese<br />
folgt aus der Anfangsbedingung [S](0)=[S] 0 .<br />
C2<br />
C2<br />
⎧ ⎫<br />
K<br />
[S] 0<br />
M KM<br />
⎪e<br />
⎪ e [S]<br />
0 KM<br />
[ S] ( 0) = K<br />
MW⎨<br />
⎬ → = e<br />
(A14)<br />
⎪ K<br />
M ⎪ K<br />
M<br />
K<br />
M<br />
⎩ ⎭<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 15<br />
Hieraus folgt direkt<br />
[S] 0<br />
⎛ ⎞<br />
⎜ KM<br />
C = ⎟<br />
2<br />
K<br />
M<br />
ln [S]<br />
0<br />
e<br />
(A15)<br />
⎜ ⎟<br />
⎝ ⎠<br />
und damit Gl. 15.<br />
III) Herleitung der Reaktionsgeschwindigkeit mit Produkthemmung<br />
Ausgangspunkt der Herleitung ist abermals die Annahme eines stationären Zustandes für<br />
Spezies US, diesmal allerdings unter Beachtung der Gleichgewichtstontanten K P , die angibt,<br />
wie viel freies Enzym in der "Sackgasse" landet.<br />
d[US]<br />
k1[U][S]<br />
Ansatz:<br />
= k1[U][S]<br />
− k<br />
−1[US]<br />
− k<br />
2[US]<br />
= 0 → [US] =<br />
(A16)<br />
dt<br />
k + k<br />
Die unbekannte Konzentration des freien Enzyms stellt sich dann wie folgt dar:<br />
[ U] = [U]<br />
0<br />
− [US] − ([UP] + [USP])<br />
(A17)<br />
2<br />
−1<br />
Substitution <strong>von</strong><br />
[U][S]<br />
[ US] = und<br />
K M<br />
([U]<br />
+ [S])<br />
[P]<br />
[UP] + [USP] =<br />
(A18)<br />
K P<br />
führt zu<br />
[U]<br />
0<br />
= (A19)<br />
[S]<br />
1+<br />
K<br />
M<br />
[U]<br />
[P] [P][S]<br />
+ +<br />
K K K<br />
P<br />
M<br />
P<br />
und unter Verwendung der ersten Beziehung in (18) endlich:<br />
d[P]<br />
dt<br />
= k<br />
2<br />
[U][S] =<br />
k<br />
2<br />
[U]<br />
⎛ [P] ⎞ +<br />
( K ) ⎜<br />
⎟ M + [S] 1<br />
⎝ K<br />
P ⎠<br />
0<br />
[S]<br />
(A20)<br />
IV) Beschreibung des zur Auswertung benötigten Mathematica ® -Sheets<br />
Zunächst muss das Verzeichnis in der ersten Zeile mit shift + enter bestätigt werden. Danach<br />
sind die Werte für pH, v max , v max *, K M und [S] 0 einzutragen. Achten Sie darauf, dass Sie als<br />
Einheiten mol/L bzw. mol/(L⋅min) verwenden. Dann noch einmal shift + enter drücken. Die<br />
ASCII-Dateien komplett, ohnepH und mitpH befinden sich nun auf dem Desktop. Zur Kontrolle<br />
wird der Plot unten gleich angezeigt.<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie
<strong>Hydrolyse</strong> <strong>von</strong> <strong>Harnstoff</strong> / <strong>Michaelis</strong>-<strong>Menten</strong>-<strong>Kinetik</strong> 16<br />
Beachten Sie, dass das Mathematica-Programm drei verschiedenen Maximalgeschwindigkeiten<br />
kennt. Die erste ("vm", in Zeile 3) ist die <strong>von</strong> Ihnen bestimmte hypothetische Maximalgeschwindigkeit<br />
v max * aus Gleichung 13. Die zweite ("v", in Zeile 5) ist die <strong>von</strong> Ihnen mittels<br />
des Lineweaver-Burk-Plots experimentell bestimmte Maximalgeschwindigkeit. Die dritte<br />
("vcorr", in Zeile 10) ist die zur Langzeitmessung 2b gehörige Maximalgeschwindigkeit und<br />
wird vom Programm aus vmax* und dem <strong>von</strong> Ihnen in 2b gemessenen mittleren pH-Wert der<br />
Lösung berechnet. Dieser pH-Wert ist nicht derselbe wie der der Messungen aus 2a!<br />
_________________________________________________________________________________________<br />
Apparatives Praktikum <strong>Physikalische</strong> Chemie, Dr. Christof Maul WS 2010/1<br />
TU Braunschweig, Institut für <strong>Physikalische</strong> und Theoretische Chemie