Keimungspraktikum - Kantonsschule Wil
Keimungspraktikum - Kantonsschule Wil
Keimungspraktikum - Kantonsschule Wil
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Kantonsschule</strong> <strong>Wil</strong><br />
<strong>Keimungspraktikum</strong><br />
Biologiepraktikum 6. Semester<br />
Hinweis: Damit die Resultate dieses Praktikums optimal protokolliert werden können,<br />
muss jede Gruppe auf einem separaten Blatt eine Protokollvorlage herstellen.<br />
Diese muss dann zu Beginn des Praktikums der Lehrkraft vorgewiesen werden.<br />
Theorie<br />
1. Die Struktur des reifen Samens<br />
Während der letzten Reifestadien dehydriert der Samen, bis er nur noch einen Wassergehalt von ungefähr<br />
fünf bis 15 Prozent seines Gewichts aufweist. Das Embryowachstum ist nun beendet und wird bis<br />
zur Keimung des Samens ruhen. Der Embryo ist von seinen vergrösserten Cotyledonen oder vom Endosperm<br />
oder von beiden umgeben. Embryo und Nahrungsvorrat sind in einer Samenschale (Testa)<br />
eingeschlossen, die von den Integumenten der Samenlage gebildet wird.<br />
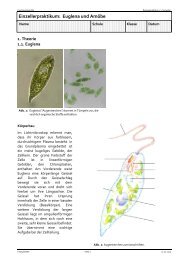
Sie können einen dicotylen Samen näher betrachten,<br />
wenn Sie den Samen einer Gartenbohne (Phaseolus<br />
vulgaris) öffnen (Abbildung a). In diesem Stadium ist<br />
der Embryo eine gestreckte Struktur, eine Achse, der<br />
die Cotyledonen (Keimblätter) anhängen. Die Embryoachse<br />
unterhalb des Ansatzpunktes der Cotyledonen<br />
wird als Hypocotyl (vom griechischen hypo für "unter")<br />
bezeichnet. Das Hypocotyl endet in der Radicula, der<br />
Keimwurzel. Den Teil der Embryoachse oberhalb der<br />
Cotyledonen nennt man Epicotyl (vom griechischen<br />
epi für "auf" oder "über"). An seiner Spitze befindet<br />
sich die Plumula (Keim- oder Stammknospe). Sie besteht<br />
aus der Spross-Spitze mit einem Paar Miniaturblättern.<br />
Die Cotyledonen der Gartenbohne sind vor der Keimung<br />
fleischig, da sie bei der Samenentwicklung mit<br />
Nährstoffen aus dem Endosperm beladen werden. Die<br />
Samen einiger Dicotyledonen, wie zum Beispiel die<br />
des Rizinus (Ricinus communis), halten ihre Nahrungsreserven<br />
im Endosperm zurück und haben sehr dünne<br />
Keimblätter (Abbildung b). Diese übernehmen die<br />
Nährstoffe erst dann aus dem Endosperm und leiten<br />
sie zum Embryo, wenn der Samen keimt.<br />
Der Samen einer Monocotyledonen wie Mais besitzt<br />
ein einzelnes Keimblatt (Abbildung c), das Scutellum.<br />
Dieses ist sehr dünn, hat aber eine grosse Oberfläche,<br />
was die Absorption von Nährstoffen während der Keimung<br />
erheblich verbessert. Der Embryo ist von einer<br />
Scheide eingeschlossen. Diese Scheide besteht aus einer<br />
Coleorrhiza, welche die Wurzel bedeckt und ein<br />
Abb. 1: Samen verschiedener Pflanzen<br />
Coleoptile, die den embryonalen Spross einschliesst.<br />
2. Evolutionäre Anpassungen im Keimungsprozess erhöhen die Überlebenschancen des Keimlings<br />
Die Keimung des Samens symbolisiert für viele Menschen den Beginn pflanzlichen Lebens. Tatsächlich<br />
enthält aber der Samen bereits eine winzige Pflanze, vollständig ausgerüstet mit Keimwurzel und<br />
Keimspross. Bei der Keimung handelt es sich demnach nicht um den Lebensbeginn einer Pflanze, son-<br />
Sy/Zö Seite 1 21.02.2013
<strong>Kantonsschule</strong> <strong>Wil</strong><br />
Sy/Zö Seite 2 21.02.2013<br />
Biologiepraktikum 6. Semester<br />
dern um die Wiederaufnahme von Wachstum und Entwicklung, die zeitweilig aussetzten, als der Samen<br />
reifte und der Embryo in eine Ruhephase überging. Manche Samen keimen, sobald sie sich in einer<br />
geeigneten Umgebung befinden. Andere Samen befinden sich in einer Keimruhe (Dormanz) und keimen<br />
erst, wenn ein spezifisches Signal aus der Umwelt diese bricht.<br />
3. Keimruhe<br />
Die Entwicklung des Samens war einer der wichtigsten Faktoren bei der Anpassung der Pflanzen an die<br />
speziellen Probleme, die sich beim Leben und der Fortpflanzung auf dem Festland stellen. Terrestrische<br />
Lebensräume sind mit ihren schwankenden Umweltbedingungen, wie Temperatur und Wasserverfügbarkeit,<br />
im Allgemeinen nicht so konstant wie Seen oder Meere. Die Keimruhe der Samen erhöht die<br />
Wahrscheinlichkeit, dass die Keimung zu einem Zeitpunkt und an einem Ort stattfindet, der für den<br />
Keimling möglichst vorteilhaft ist. So keimen zum Beispiel Samen von Wüstenpflanzen nur nach einem<br />
ausgiebigen Regenfall. Würde dies schon nach einem bescheidenen Sprühregen geschehen, könnte der<br />
Boden für den Keimling schon bald wieder zu trocken sein. Wo Naturfeuer häufig auftreten, benötigen<br />
Samen intensive Hitze, um die Keimruhe zu brechen. Daher sind Keimlinge reichlich vorhanden, nachdem<br />
ein Feuer konkurrierende Vegetation beseitigt hat. In Gegenden mit harten Wintern sind die Samen<br />
für längere Zeit der Kälte ausgesetzt. Demzufolge keimen Samen, die im Sommer oder Herbst<br />
ausgesät werden, nicht vor dem folgenden Frühling. Dies stellt eine lange Wachstumsperiode bis zum<br />
nächsten Winter sicher. Sehr kleine Samen, wie die einiger Latticharten, benötigen für ihre Keimung<br />
Licht und brechen ihre Keimruhe nur, wenn sie flach genug eingesät werden, damit der Keimling über<br />
die Bodenoberfläche hinausragen kann. Manche Samen besitzen eine Schale, die während der Passage<br />
durch das tierische Verdauungssystem chemischen Angriffen ausgesetzt und geschwächt werden<br />
muss. Hinzu kommt, dass sie auf dieser Weise wahrscheinlich weiter verbreitet werden, bevor sie keimen.<br />
Der Zeitraum, in dem ein ruhender Samen lebens- und keimfähig bleibt, schwankt je nach Spezies und<br />
Umweltbedingungen zwischen wenigen Tagen bis zu Jahrzehnten oder sogar länger. Die meisten Samen<br />
sind ausdauernd genug, um ein bis zwei Jahre abwarten zu können, bis günstige Bedingungen für<br />
die Keimung herrschen. Daher befindet sich im Boden stets eine grosse Zahl ungekeimter Samen, die<br />
sich über die Jahre angesammelt hat. Das ist einer der Gründe, warum sich nach Feuer, Dürre, Flut oder<br />
anderen Naturkatastrophen sehr rasch neue Vegetation einstellt.<br />
4. Vom Samen zum Keimling<br />
Der erste Schritt bei der Keimung vieler Samen ist das Quellen, das heisst die auf dem niedrigen Wasserpotential<br />
des trockenen Samens beruhende Aufnahme von Wasser. Die Wasserspeicherung verursacht<br />
ein Ausdehnen des Samens sowie ein Aufplatzen der Schale und löst Veränderungen im Metabolismus<br />
des Embryos aus, der dadurch zur Wiederaufnahme seines Wachstums veranlasst wird. Enzyme<br />
beginnen, die Vorratsstoffe des<br />
Endosperms oder der Cotyledonen<br />
abzubauen, und die<br />
Nährstoffe werden zu den<br />
Wachstumszonen des Embryos<br />
transportiert.<br />
In Gerstenkörnern und anderen<br />
Getreiden wurde diese Mobilisierung<br />
von Nahrungsreserven<br />
am Ausführlichsten untersucht.<br />
Daher werden wir Getreide als<br />
ein Beispiel für diesen Vorgang<br />
nehmen (Abbildung links). Bald<br />
Abb. 2: Mobilisierung von Nahrungsreserven bei Getreidekörnern<br />
nach der Wasseraufnahme be-
<strong>Kantonsschule</strong> <strong>Wil</strong><br />
Sy/Zö Seite 3 21.02.2013<br />
Biologiepraktikum 6. Semester<br />
ginnt das Aleuron, die dünne äussere Schicht des Endosperms, mit der Bildung von a-Amylase und anderen<br />
Enzymen, welche die im Endosperm gespeicherte Stärke abbauen. (Ein ähnliches Enzym in unserem<br />
Speichel trägt zur Verdauung von Brot und anderen aus stärkehaltigem Endosperm ungekeimter<br />
Getreidekörner hergestellten Lebensmitteln bei.) Wird der Embryo aus einem Samen entfernt, bevor<br />
dieser mit Wasser in Berührung kommt, wird keine α-Amylase produziert. Das lässt vermuten, dass der<br />
Embryo ein Signal an das Aleuron schickt, um die Enzymbildung zu initiieren. Dieses chemische Signal<br />
wurde als eine Klasse von Pflanzenhormonen identifiziert, die man als Gibberelline bezeichnet.<br />
Das erste Organ, das aus dem keimenden Samen austritt, ist die Radicula oder Keimwurzel. Als nächstes<br />
muss die Spross-Spitze die Erdoberfläche durchbrechen. Bei Gartenbohnen und anderen Dicotyledonen<br />
(Abbildung a) bildet sich im Hypocotyl ein Haken. Durch das Wachstum wird dieser Haken über<br />
die Erdoberfläche hinausgeschoben. Lichtstimulierung richtet das Hypocotyl auf und hebt die Cotyledonen<br />
sowie das Epicotyl an. Auf diese Weise werden der zarte Spross-Scheitel und die massigen Cotyledonen<br />
eher über die Erdoberfläche hinausgezogen, als mit der Spitze voran durch den schmirgelartig<br />
wirkenden Boden gestossen. Das Epicotyl breitet nun seine ersten Laubblätter aus, die sich<br />
entfalten, ergrünen und mit der Nahrungsproduktion durch Photosynthese beginnen. Die Cotyledonen<br />
verwelken und fallen vom Keimling ab. Ihre Nahrungsreserven wurden vom keimenden Embryo verbraucht.<br />
Für den Keimling ist Licht der Haupthinweis<br />
darauf, dass er den Boden durchbrochen<br />
hat. Das Hyopocotyl der Gartenbohne<br />
streckt sich solange und schiebt<br />
seine Hakenkrümmung aufwärts, bis es<br />
aus der Dunkelheit heraustritt. Erst wenn<br />
der Keimling Licht wahrnimmt, richtet<br />
sich der Haken auf, und das Epicotyl beginnt<br />
sich zu strecken. Lassen wir den Samen<br />
im Dunkeln keimen, können wir den<br />
Keimling mit diesem Trick dazu bringen,<br />
sich so zu verhalten, als ob er noch vergraben<br />
sei. Der unbelichtete Keimling<br />
streckt dann ein übertrieben langes Hypocotyl<br />
mit einem Haken an seiner Spitze<br />
in die Höhe, und die Laubblätter werden<br />
nicht grün. Nachdem der Keimling seine<br />
Nahrungsreserven erschöpft hat, hört er<br />
auf zu wachsen und stirbt.<br />
Erbsen zeigen ein anderes Keimverhalten<br />
(Abbildung b), obwohl sie derselben Familie<br />
wie die Bohnen angehören. Ein Haken<br />
bildet sich im Epicotyl, nicht im Hypocotyl.<br />
Der Spross wird sanft durch Strecken des<br />
Epicotyls und Aufrichten des Hakens aus<br />
dem Boden herausgehoben. Die Cotyledonen<br />
der Erbse bleiben im Gegensatz zu<br />
denen der Bohne im Boden zurück.<br />
Monocotyledonen wie zum Beispiel Mais<br />
durchbrechen bei ihrer Keimung auf noch<br />
andere Weise den Boden. Die Coleoptile,<br />
die den Keimspross umschliessende<br />
Abb. 3: Keimung verschiedener Pflanzen<br />
Keimblattscheide, schiebt sich nach oben
<strong>Kantonsschule</strong> <strong>Wil</strong><br />
Biologiepraktikum 6. Semester<br />
durch den Boden in die Luft. Der Spross wächst dann durch den von der röhrenförmigen Coleoptile gebildeten<br />
Tunnel gerade nach oben (Abbildung c).<br />
Die Keimung eines Pflanzensamens ist genau wie die Geburt oder das Schlüpfen eines Tieres ein kritisches<br />
Entwicklungsstadium. Der widerstandsfähige Samen bringt einen zerbrechlichen Keimling hervor,<br />
der Räubern, Parasiten, Wind und anderen Gefahren ausgesetzt ist. In der freien Natur überlebt nur<br />
ein kleiner Bruchteil von Keimlingen, um sich selbst wieder fortpflanzen zu können. Den Risiken im<br />
Überleben des Individuums steht die Produktion einer enormen Anzahl von Samen gegenüber, die der<br />
natürlichen Selektion reichlich Material für die Sichtung nach den erfolgreichsten genetischen Kombinationen<br />
anbietet. Betrachtet man jedoch die bei Blüte und Fruchtbildung verbrauchten Resourcen, ist<br />
feststellen, dass es sich hierbei um eine sehr aufwendige Art der Fortpflanzung handelt. Die ungeschlechtliche<br />
(asexuelle) Reproduktion ist eine alternative Form der Vermehrung, die im Allgemeinen<br />
einfacher und für die Nachkommen weniger gefährlich ist als die geschlechtliche (sexuelle) Fortpflanzung.<br />
Ziele:<br />
I. Den Quellungsdruck der Keimung erleben.<br />
II. Kennen lernen der Faktoren welche die Keimung beeinflussen.<br />
Material:<br />
Versuch 1a:<br />
Messzylinder 100 ml<br />
Schott-Schale 80 mit Deckel<br />
Erbsen Pisum sativum<br />
Versuch 1b:<br />
Joghurt- oder Wegwerfbecher 1,5 dl<br />
Modellgips (vorbereitet)<br />
Becherglas 250 ml<br />
Erbsen Pisum sativum<br />
Versuch 2a:<br />
2 Glas-Petrischalen mit Deckel<br />
Erbsen Pisum sativum<br />
Versuch 2b:<br />
3 P-Petrischalen mit Deckel<br />
Alufolie<br />
Scotchtape<br />
Samen von Kresse Lepidium sativum<br />
Versuch 2c:<br />
5 P-Petrischalen mit Deckel<br />
Orangensaft<br />
Apelsaft<br />
Orangenscheibe<br />
Apfelscheibe<br />
Samen von Kresse Lepidium sativum<br />
Versuch 2d:<br />
6 P-Petrischalen mit Deckel<br />
Samen von Kresse Lepidium sativum<br />
Samen von Zwiebel Allium cepa<br />
Samen von Jungfer im Grünen Nigella damascena<br />
Alufolie<br />
Allgemein:<br />
Haushaltspapier<br />
Schere<br />
10 ml Spritze<br />
2. Becherglas 250 ml für Leitungswasser<br />
Permanent-Marker<br />
Kühlschrank 4ºC<br />
Wärmeschrank 37ºC<br />
Sy/Zö Seite 4 21.02.2013
<strong>Kantonsschule</strong> <strong>Wil</strong><br />
Arbeit:<br />
Biologiepraktikum 6. Semester<br />
1.) Quellung<br />
a) Quantitative Untersuchung der Quellung<br />
In einem 100 ml Messzylinder wird in 50 ml Wasser das Raumvolumen von 50 Erbsen bestimmt. Nach<br />
der Volumenbestimmung werden Wasser und Erbsen in eine Schottschale umgegossen. Nach 24 h, 48<br />
h und 96 h werden die Erbsen abgetrocknet und das Raumvolumen erneut in 50 ml Wasser gemessen.<br />
b) Quellungsdruck<br />
In einen halb mit Gips gefüllten Joghurtbecher werden ca. 10 trockene Erbsen eingedrückt. Anschliessend<br />
wird der Becher mit Gips ausgegossen. Nach dem Erstarren des Gipses wird der Gipsklotz in Wasser<br />
eingelegt. Das Resultat wird nach 24 h protokolliert.<br />
2.) Keimung<br />
a) Einfluss von Sauerstoff auf die Keimung<br />
20 Erbsen werden je in eine, mit zwei Lagen Haushaltpapier (selber zuschneiden) ausgelegte Glas-<br />
Petrischale gegeben. Eine der beiden Petrischalen wird mit Wasser gefüllt, so dass die Erbsen vollständig<br />
bedeckt sind und damit keinen Luftkontakt mehr haben. Die andere so, dass die Erbsen ca. halb bedeckt<br />
sind (evtl. muss nach 48 h etwas Wasser nachgefüllt werden). Auswertung nach 24 h, 48 und 96 h.<br />
b) Einfluss der Temperatur auf die Keimung<br />
3 P-Petrischalen werden je mit zwei Lagen Haushaltpapier belegt, mit 7ml Wasser befeuchtet und 20<br />
Samen der Gartenkresse (Lepidium sativum) bestückt. Anschliessend werden die Schalen mit Klebeband<br />
verschlossen und bei verschiedenen Temperaturen inkubiert (4°C im Kühlschrank, 20°C Zimmertemperatur<br />
und 36°C im Wärmeschrank). Alle Schalen werden im Dunkeln gehalten (in Alufolie einwickeln).<br />
Die Ergebnisse nach 24h protokollieren.<br />
c) Natürliche keimungshemmende Substanzen<br />
Die zwei Lagen Haushaltpapier von 3 P-Petrischalen werden mit je 7ml Orangensaft, Apfelsaft und mit<br />
Leitungswasser getränkt. In 2 weitere Petrischalen werden auf das mit 7 ml Wasser getränkte Haushaltspapier<br />
je eine dünne Scheibe Apfel oder eine dünne Scheibe Orange ausgelegt. Auf jeden der 5<br />
"Nährböden" werden 10 Kressesamen ausgelegt. Nach 48 h wird das Ergebnis protokolliert.<br />
d) Einfluss des Lichtes auf die Keimung<br />
6 P-Petrischalen werden mit zwei Lagen Haushaltpapier belegten und mit 7ml Wasser befeuchteten. 2<br />
Petrischalen werden mit je 20 Samen Kresse (Lepidium sativum), 2 Petrischalen mit je 20 Samen der<br />
Küchenzwiebel (Allium cepa) und 2 Petrischalen mit je 20 Samen der Jungfer im Grünen (Nigella sativa)<br />
bestückt. Jeweils eine der Schalen mit gleichartigen Samen stellt man im Licht auf, die anderen werden<br />
mit Alufolie verdunkelt. Nach 96 h werden die Keimungsgrade der einzelnen Ansätze verglichen.<br />
Achtung:<br />
• Das Protokollieren gut vorbereiten! (Genau auszählen und die Keimungsgrade (Länge, Farbe,<br />
Keimblätter schon offen, Pilzbefall) unterscheiden)<br />
• Jede Gruppe entsorgt nach der Auswertung die Samen und Keimlinge und reinigt ihre Schalen!<br />
Sy/Zö Seite 5 21.02.2013