Lösung Aufgabe 5.2.1 Verlauf der Isobaren und Isochoren im T,s ...
Lösung Aufgabe 5.2.1 Verlauf der Isobaren und Isochoren im T,s ...
Lösung Aufgabe 5.2.1 Verlauf der Isobaren und Isochoren im T,s ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Lösung</strong> <strong>Aufgabe</strong> <strong>5.2.1</strong><br />
<strong>Verlauf</strong> <strong>der</strong> <strong>Isobaren</strong> <strong>und</strong> <strong>Isochoren</strong> <strong>im</strong> T, s-Diagramm<br />
Isobare:<br />
Aus F<strong>und</strong>amentalgleichung:<br />
T ds = dh − vdp<br />
ideales Gas:<br />
dh = c p dT<br />
⎫<br />
⎪⎬<br />
⎪⎭ T ds = c p dT − vdp<br />
dp = 0 ⇒ T (ds) p = c p (dT ) p<br />
⇒<br />
( ) ∂T<br />
= T ∂s p c p<br />
Isochore:<br />
Aus F<strong>und</strong>amentalgleichung:<br />
T ds = du + pdv<br />
ideales Gas:<br />
du = c v dT<br />
⎫<br />
⎪⎬<br />
⎪⎭ T ds = c v dT − pdv<br />
dv = 0 ⇒ T (ds) v = c v (dT ) v<br />
⇒<br />
( ) ∂T<br />
= T ∂s v c v<br />
Da c p − c v = R gilt c p > c v , <strong>und</strong> es folgt:<br />
( ) ( )<br />
∂T ∂T<br />
/ = T / T = c p<br />
= κ > 1<br />
∂s v ∂s p c v c p c v<br />
1
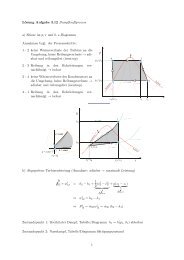
Das Verhältnis <strong>der</strong> Steigung <strong>der</strong><br />
<strong>Isochoren</strong> zur <strong>Isobaren</strong> entspricht<br />
an je<strong>der</strong> Stelle dem Verhältnis <strong>der</strong><br />
spezifischen Wärmen.<br />
h<br />
v = const arctan(T/c p )<br />
Außerdem verlaufen die <strong>Isobaren</strong><br />
stets flacher als die <strong>Isochoren</strong>.<br />
p = const<br />
arctan(T/c v )<br />
Isobare <strong>und</strong> Isochore haben bei konstanten<br />
spezifischen Wärmen c p <strong>und</strong><br />
c v auf Isothermen stets die gleiche<br />
Steigung.<br />
s<br />
Die Funktionen T (s) für isobare <strong>und</strong> isochore Zustandsän<strong>der</strong>ungen erhält<br />
man durch Integration <strong>der</strong> jeweiligen Differentiale<br />
( ) ∂T<br />
= T ,<br />
∂s p c p<br />
( ) ∂T<br />
= T .<br />
∂s v c v<br />
Diese haben die allgemeine Form<br />
( ) dT<br />
= 1 ds c T .<br />
Durch Trennung <strong>der</strong> Variablen <strong>und</strong> Integration erhält man<br />
dT<br />
T<br />
= 1 c ds ⇒ ln T T 0<br />
= 1 c (s − s 0) bzw.<br />
T<br />
= exp( s − s 0<br />
)<br />
T 0 c<br />
Isobare:<br />
Isochore:<br />
T<br />
T 0<br />
= exp( s − s 0<br />
c p<br />
)<br />
T<br />
T 0<br />
= exp( s − s 0<br />
c v<br />
)<br />
2
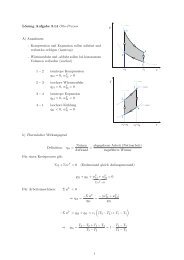
Isobare:<br />
h<br />
p = const<br />
p<br />
arctan(T/c p )<br />
Bei konstanter Temperatur<br />
steigt die Entropie<br />
für anwachsenden Druck.<br />
s<br />
Isochore:<br />
h<br />
v = const<br />
v<br />
arctan(T/cv)<br />
Bei konstanter Temperatur<br />
steigt die Entropie<br />
für anwachsendes Volumen.<br />
s<br />
3