Ãbungsblatt 9 - Institut für Physikalische Chemie - Universität Stuttgart
Ãbungsblatt 9 - Institut für Physikalische Chemie - Universität Stuttgart
Ãbungsblatt 9 - Institut für Physikalische Chemie - Universität Stuttgart
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Übung zur Vorlesung <strong>Physikalische</strong> <strong>Chemie</strong><br />
-Grundlagen der Thermodynamik-<br />
Dr. Natalie Preisig<br />
<strong>Institut</strong> für <strong>Physikalische</strong> <strong>Chemie</strong>, Raum: 09.363, Universität <strong>Stuttgart</strong><br />
e-mail: n.preisig@ipc.uni-stuttgart.de, Tel.: 0711-685-64462<br />
Übungsblätter finden Sie unter: http://www.ipc.uni-stuttgart.de/AKStubenrauch/lehre/ oder in ILIAS<br />
Übungsblatt 9 – Phasendiagramme; Hebelgesetz; Wiederholungsaufgaben<br />
Aufgabe 1: Betrachten Sie eine Mischung aus zwei Komponenten A und B. p A * und p B * sind die<br />
Dampfdrucke der reinen Komponenten. Zeigen Sie mit Hilfe des Raoultschen Gesetzes die Abhängigkeit<br />
l<br />
des Dampfdrucks der Mischung p von dem Stoffmengenbruch x B (Gleichung für obere Kurve des<br />
Dampfdruckdiagramms). Mit Hilfe des Raoultschen und des Daltonschen Gesetzes zeigen Sie die<br />
Abhängigkeit des Dampfdrucks der Mischung p von dem Stoffmengenbruch x g B (Gleichung für die untere<br />
Kurve des Dampfdruckdiagramms).<br />
(4 Punkte)<br />
Aufgabe 2: Nachfolgende Abbildung zeigt das Dampfdruckdiagramm der Mischung aus Benzol und Toluol<br />
bei T = 22 o C.<br />
(4 Punkte)<br />
Dampfdruckdiagramm<br />
80<br />
70<br />
Gesamtdruck p ges.<br />
, mbar<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1,0<br />
Molenbruch von Benzol<br />
Abb. 1. Dampfdruckdiagramm des Benzol – Toluol – Gemisches bei T = 22 o C.<br />
a) Geben Sie an, welche Phasen in den einzelnen Diagrammgebieten vorliegen.<br />
b) Wir befinden sich in Zweiphasengebiet, d.h. dass Flüssigkeit und Gasphase koexistieren. Mit Hilfe des<br />
Dampfdruckdiagramms bestimmen Sie graphisch jeweils die Zusammensetzung des Dampfes (x B g und x T g ),<br />
der mit einer Flüssigkeit der Zusammensetzung 1) x B l = 0.10; 2) x B l = 0.25; 3) x B l = 0.50 und 4) x B l = 0.75<br />
im Gleichgewicht steht. Füllen Sie Tabelle 1 aus.<br />
c) Ausgehend von einer flüssigen Mischung der Zusammensetzung x B l = 0.60 wurde der Druck von 70 mbar<br />
auf 50 mbar reduziert. Es bilden sich zwei Phasen aus. Wie sind die Phasen zusammengesetzt und welches<br />
Stoffmengenverhältnis n l /n g beobachten Sie? Zeichnen Sie die entsprechenden Konode und Isoplethe auf das<br />
1
Dampfdruckdiagramm. Unterhalb welches Drucks wird das Gemisch komplett gasförmig, wenn der Druck<br />
weiter reduziert wird?<br />
Tab. 1. Zusammensetzung der flüssigen Phase (x B l und x T l ) und des Dampfes<br />
(x B g und x T g ) für Benzol/Toluol-Gemisch bei 22 o C.<br />
Zusammensetzung der fl. Phase<br />
x B l und x T<br />
l<br />
Zusammensetzung des Dampfes<br />
x B g und x T<br />
g<br />
1) x B l = 0.10, x T l = x B g = , x T<br />
g<br />
=<br />
2) x B l = 0.25, x T l = x B g = , x T<br />
g<br />
=<br />
3) x B l = 0.50, x T l = x B g = , x T<br />
g<br />
=<br />
4) x B l = 0.75, x T l = x B g = , x T<br />
g<br />
=<br />
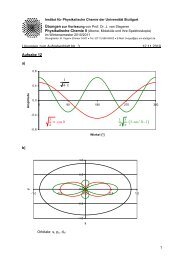
Aufgabe 3: Bei 25 o C wurde eine Mischung aus zwei flüssigen Substanzen A und B hergestellt: m A = 30 g,<br />
m B = 70 g, M A = 86.2 g mol -1 , M B = 123.0 g mol -1 . Dann wurde diese Mischung auf 15 o C abgekühlt. Es<br />
bilden sich zwei Phasen aus (s. Abb. 2). Bestimmen Sie die Phasenzusammensetzungen und das<br />
Stoffmengenverhältnis der koexistierenden Phasen. Zeichnen Sie die entsprechenden Konode und Isoplethe.<br />
Unterhalb welcher Temperatur T* wird diese Mischung zweiphasig?<br />
Berechnen Sie auch die Zusammensetzung und die Anteile der beiden koexistierenden Phasen bei 10 o C.<br />
(4 Punkte)<br />
Phasendiagramm<br />
30<br />
25<br />
Einphasenbereich<br />
20<br />
T krit.<br />
T / °C<br />
15<br />
10<br />
5<br />
Zweiphasenbereich<br />
0<br />
-5<br />
0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1,0<br />
Abb. 2. Phasendiagramm für das System A/B. T – Temperatur, x B – Molenbruch der Substanz B in der<br />
Mischung.<br />
Aufgabe 4: Bei T 1 = 20 o C wurde aus zwei Flüssigkeiten A und B eine flüssige Mischung hergestellt (x A =<br />
0.3, x B = 0.7). Das Siedediagramm dieser idealen Mischung ist in Abb. 3 dargestellt. Betrachten Sie die<br />
Erwärmung dieser Mischung bis die Temperatur T 5 = 100 o C erreicht ist.<br />
a) Bei welcher Temperatur T 2 fängt diese Mischung an zu sieden? Wie ist die Zusammensetzung des ersten<br />
gebildeten Dampfes bei dieser Temperatur?<br />
x B<br />
2
) Bestimmen Sie die Zusammensetzung der flüssigen Phase (x A l und x B l ) und des Dampfes (x A g und x B g )<br />
bei T 3 = 60 o C und das Stoffmengenverhältnis n l /n g .<br />
c) Oberhalb welcher Temperatur T 4 liegt keine flüssige Phase mehr vor? Wie ist die Zusammensetzung der<br />
letzten verbliebenen Tropfen Flüssigkeit bei dieser Temperatur, wenn fast alles verdampft ist?<br />
d) Zeichnen Sie die Temperaturen T 1 , T 2 , T 3, T 4 und T 5 , die Konoden bei T 2 , T 3, T 4 und die Molbrüche x l A und<br />
x g A bei 60 o C in das Siedediagramm. Füllen Sie die Tab. 2 aus.<br />
(5 Punkte)<br />
120<br />
Siedediagramm einer idealer Mischung<br />
100<br />
Dampf<br />
80<br />
Temperatur T<br />
60<br />
40<br />
20<br />
Flussigkeit<br />
Zweiphasenbereich<br />
Abb. 3. Siedediagramm für das System A/B.<br />
Tab. 2. Zusammensetzung der flüssigen Phase (x A l und x B l ) und des Dampfes (x A g und x B g ) für A/B-System<br />
bei verschiedenen Temperaturen.<br />
Temperatur, o C<br />
Zusammensetzung der fl. Phase<br />
x A l und x B<br />
l<br />
Zusammensetzung des Dampfes<br />
x A g und x B<br />
g<br />
T 1 = 20 o C x A l = 0.3, x B l = 0.7 –<br />
T 2 =<br />
T 3 = 60 o C<br />
T 4 =<br />
0<br />
0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1,0<br />
Molenbruch von A<br />
T 5 = 100 o C – x A g = , x B<br />
g<br />
=<br />
Aufgabe 5: Bei 90 o C sind die Dampfdrücke von Toluol und O-Xylol 533 mbar und 200 mbar. Welche<br />
Zusammensetzung hat eine flüssige Mischung aus diesen beiden Komponenten, die bei 90 o C unter einem<br />
Druck von 0.5 bar siedet? Welche Zusammensetzung hat der dabei entstehende Dampf? (3 Punkte)<br />
3
Aufgabe 6: Wir betrachten einen Carnotschen Kreisprozess mit 1 mol eines idealen Gases als<br />
Arbeitsmedium. Die molare Wärmekapazität des Gases bei konstantem Volumen beträgt 12.47 J mol -1 K -1 .<br />
Das Gas wird zuerst bei 500 K isotherm von 1 L auf 10 L expandiert. Danach entspannt es sich adiabatisch<br />
bis die Temperatur 300 K erreicht. Anschließend findet eine isotherme Kompression statt, gefolgt von einer<br />
adiabatischen Kompression zurück zum Anfangszustand. Zeichnen Sie in ein p,V-Diagramm den<br />
zugehörigen Kreisprozess ein. Bestimmen Sie für jeden Einzelschritt sowie für den gesamten Kreisprozess<br />
q, w und U. Wie groß ist der Wirkungsgrad des Prozesses? (4 Punkte)<br />
4