Lehramt - Institut für Physikalische Chemie
Lehramt - Institut für Physikalische Chemie
Lehramt - Institut für Physikalische Chemie
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
UV-VIS<br />
Die Grenzquantenausbeuten φ ′ max und φ max betragen für Pyren bei Zimmertemperatur<br />
Excimer: φ ′ max = 0,65<br />
Monomer: φ max = 0,62<br />
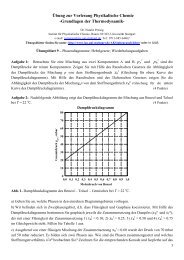
Durch Auftragen des Quotienten I ′ /I gegen c erhält man Ursprungsgeraden. Aus den Steigungen<br />
ermittelt man die Halbwertskonzentrationen. Beachten Sie, dass die Fläche unter der<br />
Excimer- bzw. Monomerbande proportional ist zu I’ bzw. zu I. Näherungsweise lässt sich I’<br />
bzw. I nach folgenden Gleichungen ermitteln<br />
I ′ = I ′ relmax ·b′ 1/2 und I = I relmax ·b 1/2 (2.39)<br />
I ′ relmax ,I relmax : maximale Instensität der Excimer- bzw. Monomerbande<br />
b ′ 1/2 ,b 1/2 : Halbwertsbreite der Excimeren- bzw. Monomerenbande<br />
2.4.2.2.2. Bestimmung der bimolekularen Geschwindigkeitskonstanten k a der Assoziation<br />
und der Viskosität<br />
Für die Geschwindigkeitskonstante gilt folgende Beziehung (s. Definition der Halbwertskonzentration,<br />
Gl. 2.30 )<br />
k a = k e +k d<br />
c h<br />
. (2.40)<br />
Die Häufigkeitskonstante k e der Strahlung beträgt 1,3 ·10 6 s −1 . Die Quantenausbeute ist oben<br />
angegeben.<br />
2.4.2.2.3. Interpretation der Geschwindigkeitskonstanten (Diffusionskontrolle)<br />
Bevor die Moleküle A und A* miteinander reagieren können, müssen sie zunächst zusammenstoßen.<br />
Ob nach einem Stoß tatsächlich eine Reaktion stattfindet hängt von Parametern<br />
ab wie: Höhe der Reaktionsbarriere, Begegnungszeit, sterische Eigenschaften, Lösungsmittel,<br />
usw. In Lösung kann man (im Gegensatz zur Gasphase) davon ausgehen, dass die Stoßzeit<br />
lange genug ist, damit ein Stoßpaar mit seiner Umgebung genügend Energie austauschen<br />
kann, um reagieren zu können. Zur genaueren Untersuchung unterteilen wir den Prozess<br />
A+A ∗ = AA ∗<br />
mit Hilfe eines kinetischen Schemas in einfache Teilschritte. Wir nehmen an, dass die Bildung<br />
des Stoßpaares A---A ∗ ein Prozess zweiter Ordnung ist:<br />
A + A ∗ = A---A ∗ v = k D [A][A ∗ ]<br />
k D ist von den Diffusionseigenschaften von A und A ∗ abhängig. Das Stoßpaar kann wieder<br />
auseinander diffundieren, ohne reagiert zu haben, oder es kann ein Excimer AA ∗ bilden. Wir<br />
nehmen an, dass beide Reaktionen pseudo-erster Ordnung sind, dann gilt<br />
A---A ∗ = A + A* v = k D ′[A---A ∗ ]<br />
A---A ∗ = AA ∗ v = k R [A---A ∗ ].<br />
42