Lehramt - Institut für Physikalische Chemie
Lehramt - Institut für Physikalische Chemie
Lehramt - Institut für Physikalische Chemie
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
UV-VIS<br />
Unter Excimeren versteht manMolekül-Assoziate, die nur inangeregten Elentronenzuständen<br />
existieren. Sie sind deshalb unmittelbar nur in Emissionsspektren, vor allem Fluoreszenzspektren,<br />
zu erkennen. Trotz ihrer Kurzlebigkeit sind sie für viele photophysikalische und<br />
photochemische Effekte verantwortlich.<br />
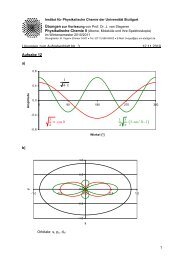
Die Entstehung von Excimeren kann anhand des in Abb. 2.11 gezeigten Potentialkurvenverlaufs<br />
erläutert werden. Danach ist der Grundzustand des Excimers instabil, denn bei Verringerung<br />
des Molekülabstands nimmt die potentielle Energie stetig zu. Befindet sich aber einer<br />
der beiden Reaktionspartner im elektronisch angeregten Zustand, bildet sich ein Potentialminimum<br />
heraus, in dem das Eximer stabilisiert wird.<br />
Fluoreszenzemission und innermolekulare strahlungslose Desaktivierung angeregter Moleküle<br />
A ∗ stehen mit chemischen Prozessen gemäß folgendem Schema in Konkurrenz (Abb. 2.12).<br />
Abb. 2.12.: Die Excimerenbildung (k r ) steht mit Fluoreszenzemission (k e ) und strahlungsloser<br />
Desaktivierung (k d )in Konkurrenz.<br />
Während die Prozesse mit k e und k d als monomolekulare Reaktionen angesehen werden<br />
können,<br />
− d[A∗ ]<br />
= (k e +k d )·[A ∗ ] (gilt bei k r = 0), (2.27)<br />
dt<br />
ist im Fall eines hinzukommenden “chemischen” Konkurrenzprozesses<br />
− d[A∗ ]<br />
= (k e +k d +k a ·[B])·[A ∗ ], (2.28)<br />
dt<br />
wobei k a die Geschwindigkeitskonstante einer bimolekularen Reaktion darstellt.<br />
Der Konkurrenzprozess, dies kann eine chemische Reaktion oder auch der Übertrag der elektronischen<br />
Anregungsenergie auf ein anderes Molekül sein, führt zu einem schnelleren Verschwinden<br />
der fluoreszierenden Substanz A ∗ und dadurch zu einer Reduktion der Fluoreszenzintensität.<br />
Man spricht dann von Fluoreszenzlöschung oder Quenching.<br />
Die Fluoreszenz-Quantenausbeute φ ist der Bruchteil der angeregten Moleküle, der unter<br />
Emission eines Lichtquants desaktiviert wird und ist somit gegeben durch<br />
φ =<br />
k e<br />
k e +k d +k r<br />
. (2.29)<br />
Man kann diesen Ausdruck umittelbar verstehen als Quotienten der Häufigkeit der günstigen<br />
Ereignisse (Fluoreszenz) und der Häufigkeit aller möglichen Ereignisse. Beträgt also die<br />
absorbierte Intensität I a [Quanten/s], so ist die Fluoreszenzintensität I = φ·I a .<br />
38