Ãbungsblatt 7 - Institut für Physikalische Chemie - Universität Stuttgart
Ãbungsblatt 7 - Institut für Physikalische Chemie - Universität Stuttgart
Ãbungsblatt 7 - Institut für Physikalische Chemie - Universität Stuttgart
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Übung zur Vorlesung <strong>Physikalische</strong> <strong>Chemie</strong><br />
-Grundlagen der Thermodynamik-<br />
Dr. Natalie Preisig<br />
<strong>Institut</strong> für <strong>Physikalische</strong> <strong>Chemie</strong>, Raum: 09.363, Universität <strong>Stuttgart</strong><br />
e-mail: n.preisig@ipc.uni-stuttgart.de, Tel.: 0711-685-64462<br />
Übungsblätter finden Sie unter: http://www.ipc.uni-stuttgart.de/AKStubenrauch/lehre/<br />
Übungsblatt 7 – Wiederholungsaufgaben<br />
Aufgabe 1: In einer auf 20 o C temperierten 10-Liter-Stahlflasche befinden sich 25 mol Helium. Nach dem<br />
Öffnen der Flasche strömt das Gas gegen einen Außendruck von 1.030 bar unter isothermer Expansion aus.<br />
Welche maximale Volumenarbeit verrichtet es dabei?<br />
(3 Punkte)<br />
Aufgabe 2: Die Verbrennungsenthalpie für Naphthalin C 10 H 8 (s) beträgt -5157 kJ mol -1 .<br />
a) Geben Sie die Reaktionsgleichung der Verbrennung an.<br />
b) Stellen Sie den Reaktionsverlauf (gemäß Satz von Hess) der Bildung (aus den Elementen) und<br />
Verbrennung von Naphthalin graphisch dar und berechnen Sie die molare Standardbildungsenthalpie für<br />
Naphthalin. Die Standardbildungsenthalpien von H 2 O und CO 2 sind -286 und -394 kJ mol -1 . (3 Punkte)<br />
Aufgabe 3: Berechnen Sie die Standard-Reaktionsenthalpie für die folgende Reaktion:<br />
C 6 H 6 (g) + 3H 2 (g) → C 6 C 12 (g)<br />
Die Standardbildungsenthalpien der beteiligten Stoffe bei 298 K und 1 bar sind in der Tabelle 1 aufgelistet.<br />
(3 Punkte)<br />
Tab. 1 Standardbildungsenthalpien B H bei 298 K und 1 bar.<br />
Substanz B H kJ mol -1<br />
C 6 H 6 (g) + 82.9<br />
C 6 C 12 (g) - 123.1<br />
H 2 (g) 0.0<br />
Aufgabe 4: Eine Probe eines idealen Gases, die zu Beginn bei 250 K und 1 bar ein Volumen von 30 dm 3<br />
hat, wird isotherm komprimiert. Auf welches Volumen muss komprimiert werden, wenn die Entropie um<br />
5 J K -1 erniedrigt werden soll? (3 Punkte)<br />
Aufgabe 5: Wir erhöhen den Druck einer flüssigen Probe von 35 g isotherm von 1 bar auf 3000 bar und<br />
finden dabei eine Zunahme der Freien Enthalpie um 12 kJ. Wie groß ist die Dichte der Flüssigkeit?<br />
(3 Punkte)<br />
1
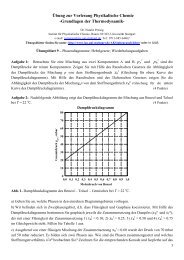
Aufgabe 6: Nachfolgende Abbildung zeigt das Zustandsdiagramm von CO 2 .<br />
a) Geben Sie an, welchen Aggregatzustand das Kohlendioxid in den Gebieten A, B und C annimmt.<br />
b) Welche Aggregatzustände kann CO 2 bei Normaldruck annehmen?<br />
c) Auf welchen Druck muss CO 2 mindestens komprimiert werden, damit es flüssig wird?<br />
d) Welche Temperatur hat Trockeneis (festes CO 2 ), wenn es bei Normaldruck mit gasförmigem CO 2 im<br />
Gleichgewicht steht?<br />
e) Ein Feuerlöscher enthält flüssiges CO 2 . Welchem Druck muss dieser bei 20 o C mindestens standhalten?<br />
Zeichnen Sie auch relevante Linien oder Punkte in das Diagramm.<br />
(3 Punkte)<br />
Abb. 1. Phasendiagramm von CO 2 .<br />
2