Demonstrationsversuch: Wasserelektrolyse und Elektrolyseur
Demonstrationsversuch: Wasserelektrolyse und Elektrolyseur
Demonstrationsversuch: Wasserelektrolyse und Elektrolyseur
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Verbrennungskalorimetrie<br />
Energie Nährstoffanteil (in g)<br />
Lebensmittel<br />
(in kJ<br />
je 100 g)<br />
Eiweiß<br />
Fett<br />
Kohlenhydrate<br />
Fleisch 1155 18 21 −<br />
Bauchspeck 2530 8 60 −<br />
Rotbarsch 475 18 4 −<br />
Ei 615 11 10 1<br />
Milch 275 3,5 3,5 5<br />
Hartkäse 1555 25 28 3<br />
Butter 3240 1 83 −<br />
Brötchen 1165 7 1 58<br />
Kartoffeln 355 2 − 19<br />
Schokolade 2355 9 33 55<br />
Äpfel 210 0,3 1 12<br />
Bier 195 0,5 − 4,5<br />
Weinbrand 1005 − − 0,1<br />
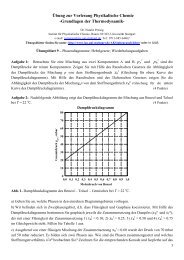
Bild 1: Links: Die Tabelle zeigt eine Zusammenstellung von Nährwerten einiger Lebensmittel.<br />
Im Rahmen einer bewußten Ernährung sollten Männer nicht mehr als 10500 <strong>und</strong> Frauen<br />
nicht mehr 8800 kJ pro Tag zu sich nehmen. Beide Werte werden jedoch mit 16000 bzw.<br />
12200 kJ pro Tag deutlich überschritten.<br />
Rechts: Was 1 kJ alles bewirken kann … (die Leistung einer 100 W Glühbirne entspricht<br />
8640 kJ pro Tag <strong>und</strong> ist mit dem täglichen Energieumsatz eines Erwachsenen vergleichbar<br />
(siehe Text)).<br />
Der Energiegehalt von Nährstoffen − Eiweiß, Kohlenhydrate <strong>und</strong> Fette − kann mittels<br />
Verbrennung kalorimetrisch bestimmt werden. Der auf diese Weise messbare, physikalische<br />
Brennwert beträgt bei Kohlenhydraten durchschnittlich 17,2 kJ⋅g -1 , bei Fetten 38,9 kJ⋅g -1 <strong>und</strong><br />
bei Eiweißstoffen 23,4 kJ⋅g -1 <strong>und</strong> ist dem physiologischen Brennwert von Kohlenhydraten<br />
<strong>und</strong> Fetten, die nahezu vollständig zu Kohlendioxid <strong>und</strong> Wasser umgesetzt werden, sehr<br />
ähnlich. Der Abbau von Eiweiß jedoch ist unvollständig. Neben Kohlendioxid <strong>und</strong> Wasser<br />
entsteht Harnstoff, so dass der physiologische Brennwert nur 17 kJ⋅g -1 beträgt.<br />
Ein Reihe von bahnbrechenden Ideen führte im 19. Jahrh<strong>und</strong>ert zur Klärung scheinbar<br />
alltäglicher Begriffe wie Wärme, Arbeit <strong>und</strong> Energie. Diese Erkenntnisse räumten auch mit<br />
der Vorstellung auf, Wärme sei ein Stoff, der von einem Körper auf einen anderen überzugehen<br />
vermag. Der Arzt Robert von Mayer beschrieb 1842 als erster, dass Energie weder<br />
verbraucht noch erzeugt werden kann, sondern dass immer nur eine Energieart in eine andere<br />
umgewandelt wird. Der englische Physiker James Prescott Joule (die Energieeinheit Joule<br />
wurde nach ihm benannt) untersuchte die Wärmeentwicklung von elektrischem Strom <strong>und</strong><br />
stellte ein elektrisches Wärmeäquivalent auf. William Thomson, der spätere Lord Kelvin <strong>und</strong><br />
Namensgeber der absoluten Temperatureinheit, verstand Wärme als Bewegung von Teilchen<br />
(„On the dynamical theory of heat“). Damit war es zum Begriff „Thermodynamik“ nicht mehr<br />
weit. Die Beschreibung thermodynamischer Gesetze durch sogenannte Hauptsätze geht auf<br />
Rudolf Clausius zurück. Nach ihm lautet der erste Hauptsatz: „Der Energieinhalt der Welt ist<br />
2