Molekulargenetische Diagnostik von Imprinting ... - BIOspektrum
Molekulargenetische Diagnostik von Imprinting ... - BIOspektrum
Molekulargenetische Diagnostik von Imprinting ... - BIOspektrum
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
753<br />
Methylierungsveränderungen<br />
<strong>Molekulargenetische</strong> <strong>Diagnostik</strong><br />
<strong>von</strong> <strong>Imprinting</strong>-Erkrankungen<br />
THOMAS EGGERMANN 1 , LUKAS SOELLNER 1 , SUSANNE BENS 2 , SABRINA SPENGLER 1 ,<br />
REINER SIEBERT 2 , KARIN BUITING 3 , BERNHARD HORSTHEMKE 3 ,<br />
MATTHIAS BEGEMANN 1<br />
1 INSTITUT FÜR HUMANGENETIK, RWTH AACHEN<br />
2 INSTITUT FÜR HUMANGENETIK, UNIVERSITÄT SCHLESWIG-HOLSTEIN, KIEL<br />
3 INSTITUT FÜR HUMANGENETIK, UNIVERSITÄT ESSEN<br />
Genomic <strong>Imprinting</strong> is defined as the expression of only one allele of a<br />
gene in a parent-of-origin specific way, its disturbance leads to an altered<br />
expression associated with specific syndromes. As the identification of<br />
multilocus methylation defects made the locus specific association questionable,<br />
molecular tests aiming on the identification of multiple loci<br />
should be implemented in routine diagnostics as they allow an efficient<br />
molecular characterization of patients with ambiguous phenotypes.<br />
DOI: 10.1007/s12268-013-0388-8<br />
© Springer-Verlag 2013<br />
Genomische Prägung<br />
ó Für die Entwicklung eines Organismus ist<br />
nicht nur die Vollständigkeit der Erbinformation,<br />
sondern auch die regelrechte Vererbung<br />
der Erbanlagen <strong>von</strong> beiden Eltern notwendig.<br />
Bereits 1980 postulierte Engel [1],<br />
dass die Vererbung eines Chromosomenpaares<br />
<strong>von</strong> nur einem Elternteil (uniparentale<br />
Disomie, UPD) mit klinischen Auffälligkeiten<br />
assoziiert sein sollte. Tatsächlich wurden in<br />
den folgenden Jahren UPDs verschiedener<br />
Chromosomen bei Patienten mit spezifischen<br />
klinischen Bildern nachgewiesen. Als zugrunde<br />
liegender Mechanismus wurde die elterliche<br />
Prägung (genomic imprinting) identifiziert.<br />
Während beim regelrechten <strong>Imprinting</strong><br />
nur eine Genkopie in Abhängigkeit <strong>von</strong> der<br />
elterlichen Herkunft exprimiert wird, kommt<br />
es bei der Störung des <strong>Imprinting</strong>musters,<br />
z. B. durch UPD, zu einer fehlenden oder übermäßigen<br />
Expression beider Genkopien.<br />
Derzeit sind ca. 80 geprägte humane Gene<br />
bekannt, häufig sind sie zu Clustern<br />
zusammengefasst. Die Regulation der geprägten<br />
Gene erfolgt daher eher nicht auf Einzelgenebene,<br />
sondern vielmehr durch übergeordnete<br />
Chromatinstrukturen.<br />
Verschiedene molekulare Mechanismen liegen<br />
dem genomischen <strong>Imprinting</strong> zugrunde,<br />
dabei wird die Expression geprägter Gene<br />
wesentlich durch DNA-Methylierung beeinflusst.<br />
Neben der UPD wurden drei weitere<br />
molekulare Veränderungen beobachtet, die<br />
bei nahezu allen bekannten <strong>Imprinting</strong>-<br />
Erkrankungen auftreten (Tab. 1, Abb. 1):<br />
chromosomale Imbalancen (Deletionen/Duplikationen),<br />
aberrante DNA-Methylierungsmuster<br />
(Hypo- oder Hypermethylierungen)<br />
mit oder ohne Veränderung der genomischen<br />
Sequenz und Punktmutationen in geprägten<br />
Genen. Die Gruppe der angeborenen <strong>Imprinting</strong>-Erkrankungen<br />
umfasst derzeit acht<br />
Krankheitsbilder, die außer durch die genannten<br />
gleichartigen molekularen Veränderungen<br />
auch durch teilweise überlappende kli-<br />
¯ Abb. 1: Molekulare Veränderungen bei<br />
<strong>Imprinting</strong>-Erkrankungen. Beispielhaft ist die<br />
Expression eines nicht geprägten Gens sowie<br />
jeweils eines maternal und eines paternal<br />
geprägten Gens dargestellt. Während das nicht<br />
geprägte Gen <strong>von</strong> Veränderungen der Methylierung<br />
nicht betroffen ist und damit eine gleichbleibende<br />
Expression zeigt, führen molekulare<br />
Veränderungen durch die verschiedenen (Epi-)<br />
Mutationstypen bei geprägten Genen zur veränderten<br />
Genproduktmenge. UPD: uniparentale<br />
Disomie.<br />
<strong>BIOspektrum</strong> | 07.13 | 19. Jahrgang
754 WISSENSCHAFT · SPECIAL: MOLEKULARE DIAGNOSTIK<br />
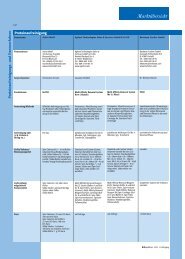
Tab. 1: Übersicht über die derzeit bekannten acht angeborenen <strong>Imprinting</strong>-Erkrankungen, die nachweisbaren molekularen Veränderungen und die klinischen Hauptmerkmale.<br />
<strong>Imprinting</strong>-Erkrankung Synonym/ Häufigkeit OMIM Chromosom/ (Epi-)Mutationstyp Detektionsrate Hauptmerkmale<br />
Abkürzung geprägte Region der einzelnen (Epi-)<br />
Mutationstypen<br />
Transienter neonataler TNDM 1/800.000 601410 6q24: PLAGL1(ZAC1)/ – upd(6)pat 40 % pränataler Kleinwuchs, transienter Diabetes mit<br />
Diabetes mellitus HYMA1 – paternale Duplikation 40 % Dehydratation, Hyperglykämie, fehlende Keto-<br />
– Hypomethylierung 20 % azidose, Makroglossie, Nabelhernie<br />
Silver-Russell-Syndrom Russell-Silver- 1/10.000 180860 7 – upd(7)mat ∼ 10 % prä-/postnataler Kleinwuchs, relative Makro-<br />
Syndrom, SRS, RSS 11p15: IGF2/H19 – upd(11p15)mat ein Fall berichtet cephalie, Asymmetrie, dreieckiges Gesicht<br />
– Duplikationen matern. Materials < 1 %<br />
– Hypomethylierung > 38 %<br />
Beckwith-Wiedemann- Wiedemann-Beck-with- 1/15.000 130650 11p15: ICR1: IGF2/H19; – upd(11p15)pat ∼ 20 % prä- und postnataler Großwuchs, Organo-<br />
Syndrom Syndrom, EMG-Syndrom, ICR2: KCNQ1OT1/LIT1; – chromosomale Aberrationen 2–4 % megalie, Makroglossie, Omphalozele, neonatale<br />
BWS CDKN1C – Hypermethylierung 5–10 % Hypoglykämie, Hemihypertrophie, Tumorrisiko<br />
– Hypomethylierung 40–50 %<br />
– Punktmutation 5 % (sporadisch),<br />
40–50 % (familiär)<br />
upd(14)pat-Syndrome Wang-Syndrom selten 608149 14q32 – upd(14)pat ? pränataler Kleinwuchs, Polyhydramnion,<br />
– Deletionen matern. Materials Bauchwanddefekte, glockenförmiger Thorax<br />
– Methylierungsdefekte mit coat-hanger rib sign<br />
upd(14)mat-Syndrom Temple-Syndrom selten 14q32: DLK1(MEG3)/ – upd(14)mat ? prä-/postnataler Kleinwuchs, kleine Hände<br />
GTL2 – Deletionen patern. Materials und Füße, stammbetonte Adipositas, muskuläre<br />
– Methylierungsdefekte Hypotonie mit Fütterungsproblemen, frühzeitige<br />
Pubertät<br />
Prader-Willi-Syndrom Prader-Labhart-Willi- 1/25.000– 176270 15q11q13 – Deletionen patern. Materials 70 % Muskelschwäche, Fütterungsprobleme,<br />
Syndrom, PWS 1/10.000 – upd(15)mat ∼ 30 % Adipositas, Hyperphagie, Kleinwuchs,<br />
– Methylierungsdefekte ∼ 1 % Hypogonadismus, geistige Behinderung<br />
Angelman-Syndrom Happy Puppet-Syndrom, 1/20.000– 105830 15q11q13: UBE3A – Deletionen matern. Materials 70 % Mikrozephalie, Ataxie, Epilepsie, Ruhelosigkeit,<br />
AS 1/12.000 – upd(15)pat 1–3 % häufiges Lachen, geistige Behinderung, keine<br />
– Methylierungsdefekte ∼ 4 % Sprache<br />
– Punktmutationen 10–15 %<br />
Pseudohypopara- PHPIb selten 603233 20q13: GNAS maternal vererbte Deletionen, ? isolierte renale PTH-Resistenz<br />
thyroidismus Ib die aberrante Methylierungen<br />
bewirken<br />
nische Merkmale charakterisiert<br />
sind (Tab. 1).<br />
Für alle bekannten <strong>Imprinting</strong>-<br />
Erkrankungen ist die Assoziation<br />
zwischen Erkrankung und spezifischer,<br />
nur auf einen Genlocus<br />
beschränkter <strong>Imprinting</strong>-Veränderung<br />
berichtet (Tab. 1). Daher<br />
war es erstaunlich, dass bei<br />
Patienten mit transientem neonatalem<br />
Diabetes mellitus<br />
(TNDM) neben der typischen<br />
6q24-Hypomethylierung <strong>Imprinting</strong>-Störungen<br />
weiterer Loci zu<br />
beobachten waren [2]. Bei mehreren<br />
<strong>Imprinting</strong>-Erkrankungen<br />
wurde zwischenzeitlich ein solcher<br />
Multilocus-Methylierungsdefekt<br />
(MLMD) berichtet, allerdings<br />
scheint er nur beim TNDM,<br />
Silver-Russell-Syndrom (SRS) und<br />
Beckwith-Wiedemann-Syndrom<br />
(BWS) häufiger aufzutreten. Interessanterweise<br />
zeigen BWS- bzw.<br />
SRS-Patienten mit gleichartigen<br />
Hypomethylierungen beider im -<br />
printing control regions (ICRs) in<br />
der Region 11p15 jeweils das für<br />
die Erkrankung typische klinische<br />
Bild, sodass derzeit unklar<br />
ist, wie es zur Ausprägung der<br />
spezifischen Symptomatik bei<br />
anscheinend gleichem Epigenotyp<br />
kommt. Möglicherweise tragen<br />
diese Patienten ein gewebespezifisches<br />
Mosaik, wobei die<br />
Methylierungsstörung des für<br />
eine Erkrankung relevanten<br />
Locus in einem bestimmten<br />
Gewebe zur jeweils typischen<br />
Symptomatik führt.<br />
Mögliche Ursachen <strong>von</strong><br />
<strong>Imprinting</strong>-Defekten<br />
Während es sich bei den chromosomalen<br />
Imbalancen (Deletionen/Duplikationen),<br />
uniparentalen<br />
Disomien und Punktmutationen<br />
in geprägten Genen<br />
um „klassische“ chromosomale<br />
oder molekulare Mutationen handelt,<br />
fasst man unter Epimutationen<br />
Veränderungen der Chromatinstruktur<br />
sowie chemischer<br />
DNA-Modifikationen, und nicht<br />
solche der DNA-Sequenz zusammen.<br />
Aufgrund seiner Komplexität<br />
und der Vielzahl der be -<br />
<strong>BIOspektrum</strong> | 07.13 | 19. Jahrgang
755<br />
teiligten Faktoren ist der humane <strong>Imprinting</strong>-<br />
Zyklus anfällig für Fehler. Diese können bei<br />
der Löschung der Prägung in den Keimzellen,<br />
während ihrer Etablierung oder bei der<br />
Aufrechterhaltung über die Zellteilungen hinweg<br />
auftreten. Dabei können theoretisch alle<br />
beteiligten Faktoren und Abläufe betroffen<br />
sein, auch kann die Fehlerrate durch prädisponierende<br />
cis- und/oder trans-agierende<br />
Varianten oder Umwelteinflüsse beeinflusst<br />
werden. Bei cis-wirkenden Faktoren handelt<br />
es sich um molekulare Veränderungen, die<br />
auf dem gleichen Chromosom in unmittelbarer<br />
Nähe zum geprägten Locus auf diesen<br />
einwirken. So wurden bei BWS-Patienten ciswirkende<br />
Deletionen der ICR1 in 11p15<br />
berichtet: Familienmitglieder zeigten hier<br />
nur dann das klinische Bild eines BWS, wenn<br />
die Deletion das maternale Chromosom 11<br />
betraf [3–5]. Der Nachweis, dass sowohl<br />
maternal als auch paternal methylierte<br />
Loci auf verschiedenen Chromosomen<br />
beim MLMD durch Methylierungsverän -<br />
derungen betroffen sind, deutet auf eine<br />
ursächliche Beteiligung trans-agierender Faktoren<br />
hin.<br />
Locusspezifische <strong>Diagnostik</strong> <strong>von</strong><br />
<strong>Imprinting</strong>-Erkrankungen<br />
Die derzeitige labordiagnostische Abklärung<br />
der molekularen Defekte bei Patienten mit<br />
<strong>Imprinting</strong>-Erkrankungen berücksichtigt im<br />
Wesentlichen zwei Aspekte:<br />
1. Die Analytik ist in der Regel krankheitsspezifisch<br />
ausgerichtet, das heißt in<br />
Abhängigkeit <strong>von</strong> der klinischen Symptomatik<br />
wird die erkrankungsspezifische<br />
<strong>Imprinting</strong>-Region untersucht. So wird z. B.<br />
bei klinischem Verdacht auf ein BWS spezifisch<br />
auf Veränderungen in 11p15 getestet,<br />
psychomotorisch retardierte und adipöse<br />
Kinder werden in Hinblick auf das<br />
Prader-Willi-Syndrom (PWS) (15q11–13)<br />
untersucht.<br />
2. Einfluss hat weiterhin das krankheitsspezifische<br />
Spektrum <strong>von</strong> Mutationen und<br />
Epimutationen: Während z. B. mehr als<br />
70 Prozent der Patienten mit PWS oder<br />
Angelman-Syndrom (AS) Deletionen in<br />
15q11–13 tragen, steht bei Kindern mit<br />
SRS eine Methylierungsstörung in 11p15<br />
im Vordergrund. Unabhängig <strong>von</strong> diesen<br />
unterschiedlichen Häufigkeiten sollte aber<br />
bei allen <strong>Imprinting</strong>-Erkrankungen zuerst<br />
ein Methylierungstest durchgeführt werden,<br />
da dieser nahezu alle genomischen<br />
und epigenetischen Veränderungen detektiert.<br />
Vor diesem Hintergrund ist die Mehrzahl der<br />
verwendeten Methoden und Algorithmen<br />
indikationsspezifisch ausgerichtet (Tab. 2),<br />
weiterhin tragen sie dem breiten Spektrum<br />
<strong>von</strong> (Epi-)Mutationen durch einen kombinierten<br />
Einsatz <strong>von</strong> methylierungssensitiven,<br />
quantitativen und Sequenzierverfahren Rechnung<br />
[6, 7].<br />
Bei den aktuell eingesetzten Techniken lassen<br />
sich rein auf die Gendosis ausgerichtete<br />
Verfahren und quantitativ/methylierungssensitive<br />
Methoden unterscheiden (Tab. 2);<br />
dabei können mit den rein quantitativen Verfahren<br />
bereits zum Teil genomweite hochauflösende<br />
Analysen durchgeführt werden,<br />
die den Nachweis <strong>von</strong> Imbalancen sowie – im<br />
Falle <strong>von</strong> SNP-Arrays einschließlich Unter -<br />
suchung elterlicher DNA-Proben – <strong>von</strong><br />
UPDs geprägten Regionen erlauben (Abb. 2).<br />
Methylierungsveränderungen sind aber auf<br />
diese Weise nicht darstellbar, sodass diese<br />
Methoden zur molekularen <strong>Diagnostik</strong> <strong>von</strong><br />
<strong>Imprinting</strong>-Erkrankungen mit einem hohen<br />
Anteil <strong>von</strong> Methylierungsdefekten nicht geeignet<br />
sind. Dagegen können mit den methylierungssensitiven<br />
Methoden auch quantitative<br />
Veränderungen detektierbar sein. Bei auffälligem<br />
Methylierungsergebnis in diesen Tests<br />
kann dann aber eine Unterscheidung zwischen<br />
den verschiedenen (Epi-)Mutationsklassen<br />
(Imbalance, UPD, Epimutation) durch<br />
zusätzliche Analysen notwendig werden.<br />
Berücksichtigt werden sollte aber auch die<br />
Sensitivität einer Methodik, um genomische<br />
oder epigenetische Mosaike zu erfassen, die<br />
bei einzelnen Erkrankungen wie dem SRS<br />
und dem BWS <strong>von</strong> erheblicher Bedeutung<br />
sind.<br />
Zusammenfassend sollte also bei der molekulargenetischen<br />
Testung <strong>von</strong> <strong>Imprinting</strong>-<br />
Erkrankungen den methylierungssensitiven<br />
Verfahren der Vorzug gegeben werden, da je<br />
nach Befund und Krankheitsbild unterschiedliche<br />
molekulare Veränderungen möglich<br />
sind.<br />
Einschränkungen der<br />
locusspezifischen <strong>Diagnostik</strong> und<br />
Nutzen der Multilocus-Testung<br />
Da nahezu alle bekannten <strong>Imprinting</strong>-Erkrankungen<br />
mit heterogenen klinischen Merkmalen<br />
assoziiert sind, erscheint die Entscheidung<br />
für eine locusspezifische <strong>Diagnostik</strong><br />
bei Vorliegen des charakteristischen<br />
Vollbildes sinnvoll, diese wird aber im Falle<br />
einer abgeschwächten Symptomatik oder<br />
eines teilweise unspezifischen klinischen Bildes<br />
wesentlich erschwert. Hinzu kommen die<br />
teilweise überlappenden phänotypischen Auffälligkeiten<br />
der verschiedenen <strong>Imprinting</strong>-<br />
Erkrankungen: So sollte bei milder PWS-<br />
Symptomatik (Hypotonie, Adipositas) und<br />
molekularem Ausschluss einer Chromosom-<br />
15-Störung an das Vorliegen eines<br />
upd(14)mat-Syndroms gedacht werden.<br />
Die locusspezifische Ausrichtung der molekularen<br />
Testung beim Vorliegen ungewöhnlicher<br />
klinischer Symptome wird daher zunehmend<br />
infrage gestellt: Hier kann die Testung<br />
mehrerer geprägter Loci auf verschiedenen<br />
Chromosomen (Multilocus-Analytik) zum<br />
Nachweis epigenetischer und genomischer<br />
Veränderungen führen [8], die mit Einzellocus-Tests<br />
nicht erfasst werden. Beispiele hierfür<br />
sind neben den Fällen mit MLMD auch<br />
solche mit genomweiter paternaler UPD im<br />
<strong>BIOspektrum</strong> | 07.13 | 19. Jahrgang
756 WISSENSCHAFT · SPECIAL: MOLEKULARE DIAGNOSTIK<br />
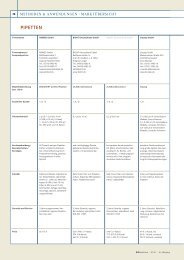
Tab. 2: Diagnostische Verfahren zum Nachweis genomischer und epigenetischer Veränderungen in <strong>Imprinting</strong>-Regionen.<br />
Methode Nachweis <strong>von</strong> Zahl der Loci/Test Vorteile Nachteile<br />
UPD CNVs Epimutation<br />
Auf genomische Imbalancen ausgerichtete Tests, Methylierungstestung nicht möglich<br />
Mikrosatelliten-Analyse ja einzelne Loci nein einzelne Loci schnell, kostengünstig, Quantifizierung keine Unterscheidung zwischen UPD und CNV möglich,<br />
(MSA) möglich DNA-Probe mindestens eines Elternteils notwendig<br />
Konventionelle nein > 5 Mb nein gesamtes Genom genomweiter Nachweis großer balancierter/ geringe Auflösung (> 5 Mb), Zellkultur notwendig<br />
Zytogenetik unbalancierter Umbauten<br />
FISH nein Einzellocus nein einzelne Loci kleine Deletionen/(Duplikationen) Mikroduplikationen nur schwer identifizierbar: Informationen<br />
zur betroffenen Region notwendig, Zellkultur notwendig<br />
Molekulare Karyotypisierung SNP-Array genomweit nein gesamtes Genom hochauflösender genomweiter Nachweis kein Methylierungsnachweis, keine Detektion balancierter<br />
(Array-CGH/SNP-Array) unbalancierter Umbauten Umbauten<br />
Methylierungsspezifische (MS-) Tests<br />
MS-Southern Blot ja Einzellocus ja einzelne Loci quantitativ große DNA-Mengen erforderlich, zeitaufwendig, keine Unterscheidung<br />
zwischen (Epi-)Mutationstypen<br />
MS-PCR ja Einzellocus ja einzelne Loci schnell, kostengünstig, Quantifizierung keine Unterscheidung zwischen (Epi-)Mutationstypen,<br />
möglich nur semiquantitativ<br />
MS-Pyrosequenzierung ja Einzellocus ja einzelne Loci quantitativ keine Unterscheidung zwischen (Epi-)Mutationstypen<br />
QAMA: Real-Time-PCR- ja Einzellocus ja einzelne Loci quantitativ keine Unterscheidung zwischen (Epi-)Mutationstypen<br />
basierter Methylierungsassay<br />
Bisulfit-Sequenzierung ja Einzellocus ja einzelne Loci quantitativ zeitaufwendig, Klonierung oder Next Generation Sequencing<br />
notwendig, keine Unterscheidung zwischen (Epi-)Mutationstypen<br />
MS-MLPA ja mehrere Loci ja bis zu ca. 46 Loci quantitativ, Differenzierung zwischen (Epi-) empfindlich bzgl. DNA-Qualität<br />
Mutationstypen möglich, Nachweis einer<br />
MLMD<br />
Methylierungsarray ja (ja) ja alle geprägten Genorte (hoch- quantitativ, Nachweis einer MLMD, Nachweis keine Unterscheidung zwischen (Epi-)Mutationstypen<br />
(z. B. Bead-Array) auflösend) sowie genomweit <strong>von</strong> Methylierungsstörungen außerhalb<br />
(niedrig auflösend) geprägter Genorte<br />
MS-SNuPE ja mehrere Loci ja Multilocus quantitativ, Nachweis einer MLMD keine Unterscheidung zwischen (Epi-)Mutationstypen<br />
CGH: comparative genome hybridisation; FISH: Fluoreszenz-in situ-Hybridisierung; MLPA: multiplex ligation-dependent probe amplification; MS: methylierungsspezifisch; QAMA: PCR for quantitative analysis of methylated alleles; SNP:<br />
single nucleotide polymorphism; SNuPE: single nucleotide primer extension<br />
<strong>BIOspektrum</strong> | 07.13 | 19. Jahrgang
757<br />
Mosaik bei Patienten mit BWS-Merkmalen,<br />
aber mit ungewöhnlichen, über das achte<br />
Lebensjahr hinausgehenden Tumorereignissen.<br />
Die gleichzeitige Testung verschiedener differenziell<br />
methylierter Regionen (DMRs) und<br />
geprägter Loci, aber auch mehrerer CpGs derselben<br />
DMR durch Multilocus-Verfahren geht<br />
einher mit einer erhöhten Sensitivität für<br />
schwache Methylierungsmosaike, da auch<br />
unterschiedliche CpG-Inseln der gleichen<br />
Region unterschiedliche Methylierungsgrade<br />
aufweisen.<br />
Zusammenfassend bietet die Multilocus-<br />
Testung im Vergleich zur Analyse einzelner<br />
Loci folgende Vorteile:<br />
– Durch die Testung mehrerer CpGs bzw.<br />
DMRs kann der Test sensitiver sein als Einzellocus-Analysen<br />
und somit die Aufdeckung<br />
auch geringgradiger Epimutations-<br />
Mosaike erlauben.<br />
– Bei untypischen klinischen Bildern ermöglicht<br />
sie eine parallele Analyse verschiedener<br />
Loci.<br />
– Mit dem gleichen Ansatz können Patienten<br />
mit verschiedenen Syndromen und<br />
Phänotypen, die auf eine Methylierungsstörung<br />
hinweisen, untersucht werden; insbesondere<br />
bei seltenen Krankheitsbildern<br />
ist die Durchführung aufwendiger Ein -<br />
zeluntersuchungen nicht notwendig. Mit<br />
Ausnahme <strong>von</strong> Punktmutationen können<br />
alle Mutations- und Epimutationstypen<br />
(UPD, Deletionen/Duplikationen, Methylierungsstörung)<br />
erfasst werden.<br />
– Sie erlaubt den Nachweis eines MLMD und<br />
genomweiter UPDs.<br />
Auch bei den derzeit verwendeten Routineverfahren<br />
zur Multilocus-Testung ist aber zu<br />
berücksichtigen, dass diese methodisch<br />
bedingt nur auf wenige geprägte Genorte ausgerichtet<br />
sind.<br />
Genomweite Methylierungsanalysen auf<br />
der Basis <strong>von</strong> Array- und Next Generation<br />
Sequencing-Verfahren bei Patienten mit klinischem<br />
Verdacht auf das Vorliegen einer<br />
<strong>Imprinting</strong>-Erkrankung werden zeigen, wie<br />
das Muster aberranter Methylierungen tatsächlich<br />
aussieht und welche Relevanz der<br />
MLMD für die Ätiologie der Erkrankungen<br />
hat. Auch bleibt abzuwarten, ob die implementierten<br />
Multilocus-Tests entsprechend<br />
modifiziert werden sollten oder ob genomweite<br />
Verfahren hier zum Einsatz kommen<br />
werden.<br />
Ähnlich ist die Suche nach den genomischen<br />
Grundlagen des MLMD zu bewerten:<br />
Erste Berichte über genomische Mutationen<br />
A<br />
B<br />
˚ Abb. 2: Ausgewählte Methoden zur <strong>Diagnostik</strong> <strong>von</strong> <strong>Imprinting</strong>-Erkrankungen. A, Mikrosatelliten-Analytik<br />
zum Nachweis einer maternalen uniparentalen Disomie des Chromosoms 7. In beiden<br />
untersuchten STR(short tandem repeat)-Markern lassen sich beim Patienten nur maternale Allele<br />
nachweisen. In der MS-PCR lässt sich bei gleichem Epigenotyp nur das mütterliche Allel darstellen.<br />
B, Testung geprägter Genloci auf Chromosom 11p15 bei unterschiedlichen Patienten. In der<br />
MS-MLPA zeigen die Sonden, die den Methylierungszustand der geprägten ICR1-Region anzeigen,<br />
eine Signalreduktion, somit liegt eine ICR1-Untermethylierung vor. In der MS-SNuPE-Analytik zeigen<br />
sich für die 11p15-Genorte H19/IGF2P0 (paternal methyliert) und LIT1 (maternal methyliert)<br />
gegensätzliche Methylierungsgrade im Sinne einer paternalen UPD dieser Region, während andere<br />
Loci unauffällig sind. Die Mikrosatelliten-Analyse am gleichen Genort bestätigt die Duplikation<br />
maternalen Materials.<br />
bei Patienten mit MLMD bzw. bei deren Müttern<br />
[9] weisen auf mögliche monogene Ursachen<br />
hin.<br />
Von besonderer Bedeutung ist diese Beobachtung<br />
für die genetische Beratung: Zwar<br />
treten <strong>Imprinting</strong>-Erkrankungen in der Regel<br />
sporadisch auf, familiäre Fälle werden aber<br />
immer wieder dokumentiert [10]. Dabei sind<br />
diese familiären Fälle zwar eher auf chromosomale<br />
Umbauten zurückzuführen und damit<br />
bei Patienten mit Duplikationen oder Deletionen<br />
als Ursache der Erkrankung zu beobachten,<br />
es werden aber auch familiäre Fälle<br />
auf der Basis einer primären Epimutation<br />
(Mutation eines <strong>Imprinting</strong>zentrums oder<br />
<strong>Imprinting</strong>faktors) oder einer uniparentalen<br />
Disomie berichtet. Daher ist es notwendig,<br />
die Ursachen eines auffälligen <strong>Imprinting</strong>-<br />
Tests abzuklären, zum einen im Hinblick auf<br />
die eindeutige Einordnung des Mutations-/<br />
Epimutationstyps (Imbalance, UPD, Methylierungsstörung,<br />
Punktmutation), zum anderen<br />
im Hinblick auf ein mögliches Wiederholungsrisiko.<br />
<strong>BIOspektrum</strong> | 07.13 | 19. Jahrgang
758 WISSENSCHAFT · SPECIAL<br />
Danksagung<br />
Die Autoren sind Mitglieder des<br />
vom Bundesministerium für Bildung<br />
und Forschung geförderten<br />
nationalen Netzwerks „<strong>Imprinting</strong><br />
Diseases“ (Förderkennzeichen:<br />
01GM1114) sowie des <strong>von</strong><br />
der Europäischen Union im Rahmen<br />
des COST-Programms geförderten<br />
Netzwerks EUCID.net<br />
(European Network of <strong>Imprinting</strong><br />
Disorders) (BM1208; www.imprin<br />
ting-disorders.eu).<br />
ó<br />
Literatur<br />
[1[ Engel E (1980) A new genetic concept:<br />
uniparental disomy and its potential effect,<br />
isodisomy. Am J Med Genet 6:137–143<br />
[2[ Mackay DJ, Boonen SE, Clayton-Smith J et<br />
al. (2006) A maternal hypomethylation syndrome<br />
presenting as transient neonatal diabetes<br />
mellitus. Hum Genet 120:262–269<br />
[3[ Sparago A, Cerrato F, Vernucci M et al.<br />
(2004) Microdeletions in the human H19<br />
DMR result in loss of IGF2 imprinting and<br />
Beckwith-Wiedemann syndrome.<br />
Nat Genet 36:958–960<br />
[4[ Prawitt D, Enklaar T, Gärtner-Rupprecht<br />
B et al. (2005) Microdeletion of target sites<br />
for insulator protein CTCF in a chromosome<br />
11p15 imprinting center in Beckwith-<br />
Wiedemann syndrome and Wilms’ tumor.<br />
Proc Natl Acad Sci USA 102:4085–4090<br />
[5[ Cerrato F, Sparago A, Verde G et al.<br />
(2008) Different mechanisms cause imprinting<br />
defects at the IGF2/H19 locus in<br />
Beckwith-Wiedemann syndrome and Wilms’<br />
tumour. Hum Mol Genet 15:1427–1435<br />
[6[ Ramsden SC, Clayton-Smith J, Birch R et<br />
al. (2010) Practice guidelines for the molecular<br />
analysis of Prader-Willi and Angelman<br />
syndromes. BMC Med Genet 11:70<br />
AUTOREN<br />
[7[ Eggermann T, Begemann M, Binder G<br />
et al. (2010) Silver-Russell syndrome: genetic<br />
basis and molecular genetic testing.<br />
Orphanet J Rare Dis 5:19<br />
[8[ Azzi S, Rossignol S, Steunou V et al.<br />
(2009) Multilocus analysis in a large cohort<br />
of 11p15-related foetal growth disorders<br />
(Russell Silver and Beckwith Wiedemann<br />
syndromes) reveals simultaneous loss of<br />
methylation at paternal and maternal imprinted<br />
loci. Hum Mol Genet 18:4724–4733<br />
[9[ Meyer E, Lim D, Pasha S et al. (2009)<br />
Germline mutation in NLRP2 (NALP2) in a<br />
familial imprinting disorder (Beckwith-<br />
Wiedemann Syndrome). PLoS Genet<br />
5:e1000423<br />
[10[ Bartholdi D, Krajewska-Walasek M,<br />
Ounap K et al. (2009) Epigenetic mutations<br />
of the imprinted IGF2-H19 domain in Silver-<br />
Russell syndrome (SRS): results from a large<br />
cohort of patients with SRS and SRS-like phenotypes.<br />
Am J Med Genet 46:192–197<br />
Korrespondenzadresse:<br />
Prof. Dr. Thomas Eggermann<br />
Institut für Humangenetik<br />
RWTH Aachen<br />
Pauwelsstraße 30<br />
D-52074 Aachen<br />
Tel.: 0241-80-88008<br />
Fax: 0241-80-82394<br />
teggermann@ukaachen.de<br />
Thomas Eggermann, Lukas Soellner, Susanne Bens, Sabrina Spengler,<br />
Reiner Siebert, Karin Buiting, Bernhard Horsthemke und Matthias Begemann<br />
(v. l. n. r.)<br />
Die Autorinnen und Autoren sind Mitglieder des vom BMBF geförderten Netzwerks<br />
„<strong>Imprinting</strong>-Erkrankungen“ (Förderkennzeichen: 01G1114), das die<br />
Ursachen angeborener <strong>Imprinting</strong>-Erkrankungen verfolgt, mit dem Ziel, <strong>Diagnostik</strong><br />
und Betreuung <strong>von</strong> Patienten mit diesen seltenen Erkrankungen zu<br />
verbessern.<br />
Arzneimittel in den Schlagzeilen<br />
Epigenetischer Modulator als<br />
Wunderwaffe für das Herz?<br />
ó Die Beteiligung epigenetischer Mechanismen an physiologischen<br />
und pathologischen Prozessen wird zurzeit in vielen<br />
Bereichen der Biomedizin sehr aktiv erforscht. Im Vordergrund<br />
stehen dabei die Entwicklungsbiologie sowie die Krebsforschung,<br />
aber es rücken auch andere Organsysteme und Erkrankungen<br />
mehr und mehr in den Fokus. Eine aktuelle Arbeit<br />
<strong>von</strong> P. Anand und Kollegen in Cell ((2013) 154:569–582) zeigt,<br />
dass Bromodomänen-Proteine eine wichtige Rolle in der Pathogenese<br />
und Therapie der Herzhypertrophie und -Insuffizienz<br />
spielen könnten. Bromodomänen wurden zuerst bei Drosophila<br />
entdeckt. Sie erkennen und binden sich an acetylierte<br />
Histone im Zellkern und modulieren dadurch die Chromatinstruktur<br />
und die Genexpression. Einem internationalen Team<br />
unter der Leitung <strong>von</strong> James Bradner, Harvard University, gelang<br />
bereits 2010 die Identifizierung einer niedermolekularen<br />
Verbindung, JQ1, die die Bindung des Bromodomänen-Proteins<br />
BRD4 an acetylierte Histone verhindet (Abb.). Aufgrund<br />
dieser Eigenschaft bewirkt JQ1 eine Hemmung des Wachstums<br />
<strong>von</strong> Plattenepithel-Karzinomen und multiplen Myelomzellen.<br />
In der aktuellen Arbeit kann nun gezeigt werden, dass<br />
JQ1 auch das pathologische Wachstum <strong>von</strong> Herzmuskelzellen<br />
in vitro und <strong>von</strong> Mausherzen nach chronischer Druckbelastung<br />
in vivo hemmen kann. Nicht nur die kardiale Hypertrophie wurde<br />
durch JQ1 vermindert, auch die Pumpfunktion wurde deutlich<br />
verbessert. Auf molekularer Ebene hemmte JQ1 die Elongation<br />
bei der Transkription und verminderte dadurch die pathologische<br />
Genexpression (Abb.).<br />
Y Das Ausmaß der durch JQ1 in vitro und in vivo erzielten<br />
„therapeutischen“ Effekte ist sehr beeindruckend. Dies mag<br />
auch erklären, weshalb Bromodomänen-Proteine als Angriffspunkte<br />
für neue Arzneistoffe große Hoffnungen wecken. Aber<br />
Vorsicht: JQ1 hemmt bei männlichen Mäusen die Spermatogenese<br />
und könnte den Weg zu einem Kontrazeptivum für den<br />
Mann weisen (Matzuk MM et al., Cell (2012) 150:673). Aber die<br />
potente Interferenz mit essenziellen Vorgängen im Körper könnte<br />
auch die Gefahr für schwere unerwünschte Nebenwirkungen<br />
bergen!<br />
Lutz Hein, Freiburg ó<br />
<strong>BIOspektrum</strong> | 07.13 | 19. Jahrgang