TiHo Bibliothek elib - Tierärztliche Hochschule Hannover
TiHo Bibliothek elib - Tierärztliche Hochschule Hannover TiHo Bibliothek elib - Tierärztliche Hochschule Hannover
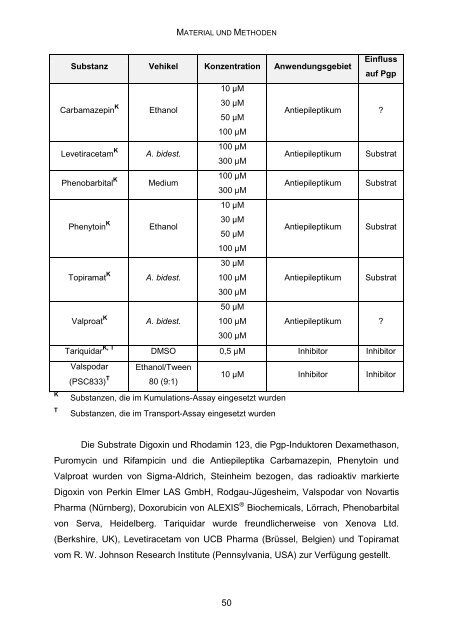
MATERIAL UND METHODEN Substanz Vehikel Konzentration Anwendungsgebiet Einfluss auf Pgp Carbamazepin K Ethanol 10 µM 30 µM 50 µM Antiepileptikum ? 100 µM Levetiracetam K A. bidest. 100 µM 300 µM Antiepileptikum Substrat Phenobarbital K Medium 100 µM 300 µM Antiepileptikum Substrat Phenytoin K Ethanol 10 µM 30 µM 50 µM Antiepileptikum Substrat 100 µM Topiramat K A. bidest. 30 µM 100 µM Antiepileptikum Substrat 300 µM Valproat K A. bidest. 50 µM 100 µM Antiepileptikum ? 300 µM Tariquidar K, T DMSO 0,5 µM Inhibitor Inhibitor Valspodar Ethanol/Tween (PSC833) T 80 (9:1) 10 µM Inhibitor Inhibitor K T Substanzen, die im Kumulations-Assay eingesetzt wurden Substanzen, die im Transport-Assay eingesetzt wurden Die Substrate Digoxin und Rhodamin 123, die Pgp-Induktoren Dexamethason, Puromycin und Rifampicin und die Antiepileptika Carbamazepin, Phenytoin und Valproat wurden von Sigma-Aldrich, Steinheim bezogen, das radioaktiv markierte Digoxin von Perkin Elmer LAS GmbH, Rodgau-Jügesheim, Valspodar von Novartis Pharma (Nürnberg), Doxorubicin von ALEXIS ® Biochemicals, Lörrach, Phenobarbital von Serva, Heidelberg. Tariquidar wurde freundlicherweise von Xenova Ltd. (Berkshire, UK), Levetiracetam von UCB Pharma (Brüssel, Belgien) und Topiramat vom R. W. Johnson Research Institute (Pennsylvania, USA) zur Verfügung gestellt. 50
MATERIAL UND METHODEN Radioaktiv markiertes 3 H-Digoxin wurde mit unmarkiertem Digoxin, welches zuvor in DMSO gelöst wurde, gemischt und in serumfreiem Medium (Opti-MEM ® ) aufgenommen. Die Endkonzentration betrug 0,1 % DMSO. Verapamil wurde ebenfalls mit unmarkiertem Verapamil gemischt. Dieses wurde vorher in Ethanol gelöst und in Opti-MEM ® aufgenommen. Die Endkonzentration des Ethanols betrug < 0,1 %. Sofern Ethanol als Lösungsmittel für einige Antiepileptika eingesetzt wurde, betrug die Endkonzentration ≤ 0,5 %. 4.3.1 Kumulations-Assay Der Kumulations-Assay, auch Uptake-Assay genannt, diente in dieser Arbeit der Überprüfung der Funktionalität von Pgp. Das Prinzip dieser Methode besteht in der Messung bestimmter markierter Substrate in den Zellen. Bei diesen Stoffen, die Substrate für Pgp sind, kann es sich um Fluoreszenzfarbstoffe oder auch um radioaktiv markierte Substrate handeln. Man macht sich hier Fähigkeit des Pgps zunutze, Substanzen aktiv aus den Zellen zu pumpen. Aus diesem Grund kann immer nur eine gewisse Menge Substrat von den Zellen aufgenommen werden. Aussaat der Zellen Die Zellen wurden für alle Kumulationsversuche so ausgesät, dass sich nach 2-3 Tagen konfluente Monolayer gebildet haben. Die Ablösung der Zellen erfolgte wie in Abschnitt 4.2.1 beschrieben. Die Kultivierung der Zellen für Kumulations- Assays erfolgte auf 6Well-Platten mit einem Volumen von 3ml/Well. In zwei Kumulationsversuchen erfolgte die Aussaat der rBCEC-Zellen auf 12Well-Platten mit einem Volumen von 1,5 ml Zellsuspension pro Well. Substanzbehandlung der Zellen Die Behandlung der Zellen begann am 3. Tag der Konfluenz. Bei jedem Behandlungszyklus wurden neben den zu testenden Antiepileptika immer eine Kontrollgruppe und bekannte Pgp-Induktoren und –Inhibitoren mitgeführt, um Aussagen zur Sensitivität des Assays machen zu können. Dazu wurden zu Beginn dieser Versuche verschiedene Induktoren für Pgp in den einzelnen Zelllinien ausgetestet und die Substanz, die eine reproduzierbare Induktion der Pgp- Funktionalität erzielte, für weitere Versuche verwendet. Angaben zu den verwendeten Substanzen und Konzentrationen sind Tabelle 4.1 zu entnehmen. 51
- Seite 7 und 8: SUMMARY ...........................
- Seite 9 und 10: EINLEITUNG 1 EINLEITUNG Epilepsien
- Seite 11 und 12: STAND DER FORSCHUNG 2 STAND DER FOR
- Seite 13 und 14: STAND DER FORSCHUNG (Epileptogenese
- Seite 15 und 16: STAND DER FORSCHUNG Dank der Forsch
- Seite 17 und 18: STAND DER FORSCHUNG 2.2 Pharmakores
- Seite 19 und 20: STAND DER FORSCHUNG Pharmakoresiste
- Seite 21 und 22: STAND DER FORSCHUNG Abbildung 2.1:
- Seite 23 und 24: STAND DER FORSCHUNG Diese Schranke
- Seite 25 und 26: STAND DER FORSCHUNG Rolle. Aus dies
- Seite 27 und 28: STAND DER FORSCHUNG erniedrigten un
- Seite 29 und 30: STAND DER FORSCHUNG Pgp an mehreren
- Seite 31 und 32: STAND DER FORSCHUNG 2.6 Wechselwirk
- Seite 33 und 34: STAND DER FORSCHUNG x A Induktoren
- Seite 35 und 36: STAND DER FORSCHUNG Antiepileptika
- Seite 37 und 38: STAND DER FORSCHUNG Ein weiterer Pg
- Seite 39 und 40: STAND DER FORSCHUNG zur Verfügung.
- Seite 41 und 42: STAND DER FORSCHUNG Dieser Umstand
- Seite 43 und 44: STAND DER FORSCHUNG junction-Protei
- Seite 45 und 46: STAND DER FORSCHUNG Hirnkapillarend
- Seite 47 und 48: FRAGESTELLUNGEN UND ZIELE DER ARBEI
- Seite 49 und 50: MATERIAL UND METHODEN Modell für T
- Seite 51 und 52: MATERIAL UND METHODEN - 10 % (v/v)
- Seite 53 und 54: MATERIAL UND METHODEN Enzymlösung
- Seite 55 und 56: MATERIAL UND METHODEN in Kultur geh
- Seite 57: MATERIAL UND METHODEN Tabelle 4.1:
- Seite 61 und 62: MATERIAL UND METHODEN Bestimmung de
- Seite 63 und 64: MATERIAL UND METHODEN Zellsuspensio
- Seite 65 und 66: MATERIAL UND METHODEN apparenten pa
- Seite 67 und 68: MATERIAL UND METHODEN einer Substan
- Seite 69 und 70: MATERIAL UND METHODEN wurden für a
- Seite 71 und 72: ERGEBNISSE bestätigt. Die kleinere
- Seite 73 und 74: ERGEBNISSE 5.1.3 Pgp-Funktionalitä
- Seite 75 und 76: Rhodamin 123 (Fluoreszenz/mg Protei
- Seite 77 und 78: Rhodamin 123 (Fluoreszenz/mg Protei
- Seite 79 und 80: Rhodamin 123 (Fluoreszenz/mg Protei
- Seite 81 und 82: Rhodamin 123 (% Kontrolle) ERGEBNIS
- Seite 83 und 84: Rhodamin 123 (Fluoreszenz/mg Protei
- Seite 85 und 86: ERGEBNISSE Zusammenfassung möglich
- Seite 87 und 88: ERGEBNISSE Tabelle 5.2: Übersicht
- Seite 89 und 90: ERGEBNISSE 5.1.3.4 Einfluss des Ser
- Seite 91 und 92: ERGEBNISSE Die Linie, die in beiden
- Seite 93 und 94: Rhodamin 123 (% Kontrolle) Rhodamin
- Seite 95 und 96: ERGEBNISSE Efflux (nicht gezeigt).
- Seite 97 und 98: TEER (*cm 2 ) ERGEBNISSE Zeitraum v
- Seite 99 und 100: % Digoxin % Digoxin % Digoxin ERGEB
- Seite 101 und 102: % Rhodamin 123 % Rhodamin 123 % Dig
- Seite 103 und 104: % Rhodamin 123 % Rhodamin 123 ERGEB
- Seite 105 und 106: % Rhodamin 123 % Rhodamin 123 % Rho
- Seite 107 und 108: % Rhodamin 123 % Digoxin % Rhodamin
MATERIAL UND METHODEN<br />
Substanz Vehikel Konzentration Anwendungsgebiet<br />
Einfluss<br />
auf Pgp<br />
Carbamazepin K Ethanol<br />
10 µM<br />
30 µM<br />
50 µM<br />
Antiepileptikum ?<br />
100 µM<br />
Levetiracetam K A. bidest.<br />
100 µM<br />
300 µM<br />
Antiepileptikum Substrat<br />
Phenobarbital K Medium<br />
100 µM<br />
300 µM<br />
Antiepileptikum Substrat<br />
Phenytoin K Ethanol<br />
10 µM<br />
30 µM<br />
50 µM<br />
Antiepileptikum Substrat<br />
100 µM<br />
Topiramat K A. bidest.<br />
30 µM<br />
100 µM Antiepileptikum Substrat<br />
300 µM<br />
Valproat K A. bidest.<br />
50 µM<br />
100 µM Antiepileptikum ?<br />
300 µM<br />
Tariquidar K, T DMSO 0,5 µM Inhibitor Inhibitor<br />
Valspodar Ethanol/Tween<br />
(PSC833) T 80 (9:1)<br />
10 µM Inhibitor Inhibitor<br />
K<br />
T<br />
Substanzen, die im Kumulations-Assay eingesetzt wurden<br />
Substanzen, die im Transport-Assay eingesetzt wurden<br />
Die Substrate Digoxin und Rhodamin 123, die Pgp-Induktoren Dexamethason,<br />
Puromycin und Rifampicin und die Antiepileptika Carbamazepin, Phenytoin und<br />
Valproat wurden von Sigma-Aldrich, Steinheim bezogen, das radioaktiv markierte<br />
Digoxin von Perkin Elmer LAS GmbH, Rodgau-Jügesheim, Valspodar von Novartis<br />
Pharma (Nürnberg), Doxorubicin von ALEXIS ® Biochemicals, Lörrach, Phenobarbital<br />
von Serva, Heidelberg. Tariquidar wurde freundlicherweise von Xenova Ltd.<br />
(Berkshire, UK), Levetiracetam von UCB Pharma (Brüssel, Belgien) und Topiramat<br />
vom R. W. Johnson Research Institute (Pennsylvania, USA) zur Verfügung gestellt.<br />
50