Praktikum Nanopartikelfällung - Lehrstuhl Mechanische ...
Praktikum Nanopartikelfällung - Lehrstuhl Mechanische ...
Praktikum Nanopartikelfällung - Lehrstuhl Mechanische ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
OTTO-VON-GUERICKE-UNIVERSITÄT MAGDEBURG<br />
Institut für Verfahrenstechnik<br />
<strong>Lehrstuhl</strong> 120 für <strong>Mechanische</strong> Verfahrenstechnik<br />
1<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong><br />
Inhalt:<br />
1. Einleitung<br />
2. Theoretische Grundlagen zur nasschemischen Nanopartikelbildung<br />
3. Aufgabestellung und Versuchsdurchführung<br />
4. Versuchsauswertung und Diskussion der Ergebnisse<br />
5. Hinweise zur <strong>Praktikum</strong>svorbereitung<br />
6. Arbeitsschutz und Sicherheitsvorschriften<br />
7. Symbolverzeichnis<br />
8. Literatur<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
2<br />
1. Einleitung<br />
Die Erzeugung feinster Partikel mit Größen im Nanometerbereich gewinnt heutzutage im Bereich<br />
der Verfahrenstechnik und bei den Materialwissenschaften zunehmend an Bedeutung.<br />
Viele wichtige Anwendungen fordern Produkte mit einer engen Partikelgrößenverteilung im<br />
Bereich von unter 1 Mikrometer bis herunter zu wenigen Nanometern. Beispiele für solche<br />
Anwendungen sind Katalysatoren mit signifikant höherer Aktivität, Metalle höherer Festigkeit,<br />
Füllstoffe, Pigmente nahezu beliebiger Spektralfarbe, keramische Pulver, magnetische<br />
Flüssigkeiten sowie pharmazeutische, medizinische und kosmetische Produkte.<br />
2. Theoretische Grundlagen zur nasschemischen Nanopartikelbildung<br />
2.1 Allgemeine Übersicht zu Herstellungsprozessen von Nanopartikeln<br />
Zur Herstellung nanoskaliger Partikel in der flüssigen Phase steht eine Reihe von klassischen<br />
Prozessen zur Verfügung [1-3]. Dazu zählen der Fällungsprozess in homogener Lösung und<br />
in kompartimentierten Systemen, wie z.B. in Mikro- und Makroemulsionen, der Hydrothermalprozess<br />
sowie der Sol-Gel-Prozess.<br />
2.2 Fällungssynthese in flüssiger Phase<br />
2.2.1 Theoretische Grundlagen<br />
Bei der Fällung kommt es durch intensives Vermischen zweier Edukte zu einer Übersättigung<br />
im Reaktionsraum. Phänomenologisch kann die Fällungssynthese als eine chemische Reaktion<br />
betrachtet werden, die durch die Entstehung eines neuen Stoffes aus den eingesetzten Ausgangsreagenzien<br />
gekennzeichnet ist, bei der der abzutrennende Stoff von der flüssigen bzw.<br />
gelösten Phase in einen kristallinen Feststoff überführt wird. Zur Induzierung dieses Stoffübergangs<br />
von einer Phase in die andere muss eine thermodynamische Triebkraft aufgeprägt<br />
werden. Bei den Fällungsprozessen ist diese gleichbedeutend mit der Einstellung des Zustandes<br />
einer übersättigten Lösung, d.h. die Konzentration der auszufällenden Komponente muss<br />
höher sein als ihre Sättigungskonzentration bei gegebenen Zustandsgrößen und Zusammen-<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
3<br />
setzung, damit der Phasenwechsel Flüssig-Fest erfolgt. Ein Maß für den Abstand des Systems<br />
vom Zustand des thermodynamischen Gleichgewichtes stellt dabei die Übersättigung dar [1].<br />
2.2.2 Fällung in wässrigem Medium<br />
Nach Erreichen der Übersättigung werden mit Hilfe homogener und heterogener Keimbildung<br />
nanokristalline Partikel erzeugt. Nach Bildung der Primärpartikel bzw. Keime beginnt ein<br />
diffusionskontrolliertes Partikelwachstum. Die wichtigste Anforderung an den Fällungsprozess<br />
kann wie folgt zusammengefasst werden: Um Partikel mit einer engen Größenverteilung<br />
zu erhalten, muss das gesamte Produkt innerhalb kurzer Zeit ausfallen. Ist dies nicht der Fall,<br />
so liegen zuerst Keime in einer noch stark übersättigten Mutterlauge vor. Die Folgen sind<br />
sowohl Wachstum als auch Neubildung der Kristallkeime unter Absenkung der Mutterlaugenkonzentration.<br />
Dies führt zum Entstehen polydisperser Partikelsysteme. Nach vollständiger<br />
Fällung muss ein zweiter Wachstumsmechanismus an der Partikelkontakten, der die Agglomeration<br />
der Primärpartikel bewirkt, unterbunden werden.<br />
Die <strong>Nanopartikelfällung</strong> wird in der Regel durch drei wichtige Mikroprozesse bestimmt:<br />
• Keimbildung<br />
• Partikelwachstum<br />
• Agglomeration, Alterung und Reifung der gebildeten Nanopartikel<br />
2.2.2.1 Modellvorstellung von LaMer und Dinegar (1950)<br />
Das Modell von LaMer kann den Verlauf von Kristallisations- und Fällungsvorgängen wie<br />
folgt beschreiben [2]. Der Verlauf der Konzentration C einer sich bildenden schwerlöslichen<br />
Verbindung ist dazu in Abbildung 1 schematisch dargestellt. Soll durch eine chemische Reaktion<br />
diese schwerlösliche Verbindung gebildet werden, so steigt die Konzentration der Ausgangsverbindung<br />
beim Hinzufügen schnell mit der Zeit an. Sobald die Konzentration C einen<br />
kritischen Wert C 0 , die kritische Übersättigung, überschritten hat, setzt spontan Keimbildung<br />
ein. Dieser Zeitraum wird als Induktionszeit bezeichnet. Gleichzeitig mit der Keimbildung<br />
beginnt auch das Wachstum der gebildeten Keime zu Partikeln, was dazu führt, dass die Kon-<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
4<br />
zentration C ein Maximum durchläuft und dann abzunehmen beginnt. Nach einiger Zeit fällt<br />
die Konzentration C unter die kritische Übersättigung C 0 .<br />
Konzentration einer schwerlöslichen Verbindung<br />
+<br />
+<br />
+<br />
+<br />
+<br />
+<br />
+<br />
C 0<br />
C 0<br />
Keimbildung kritische Übersättigung C 0<br />
Übersättigung<br />
Wachstum<br />
Sättigungskonzentration C S<br />
C S<br />
Wachstum<br />
Keimbildung<br />
Reaktionszeit<br />
Abb. 1:<br />
Konzentrationsverlauf einer schwerlöslichen Verbindung während einer<br />
Fällungsreaktion mit der Reaktionszeit nach LaMer und Dinegar (1950)<br />
Im Bereich oberhalb der Löslichkeitsgrenze C S und unterhalb der kritischen Übersättigung C 0<br />
befindet sich die Lösung in einem metastabilen Zustand. Es findet keine Keimbildung mehr<br />
statt. Eine weitere Abnahme der Konzentration C ist nur noch durch das Wachstum der schon<br />
gebildeten Keime und Partikel auf Kosten der Ausgangsstoffe möglich. Parallel zu den hier<br />
beschriebenen Vorgängen kann noch die Agglomeration einzelner gebildeter Keime und Partikel<br />
zu größeren Einheiten (Agglomeraten) stattfinden und somit zum Partikelwachstum beitragen.<br />
2.3 Synthese von Siliziumdioxid: Fällungsprozess nach Stöber, Fink und Bohn [4, 5]<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
5<br />
Der Ausgangsstoff für die Synthese bildet Tetraethylorthosilicat Si(OC 2 H 5 ) 4 (TEOS), das Lösungsmittel<br />
ist ein Alkohol (vorwiegend Ethanol), Wasser und Ammoniak, der eine katalytische<br />
Einwirkung in den Hydrolyse- und Polykondensationsreaktionen ausübt.<br />
Die chemischen Reaktionen sind in den Gleichungen (1a) und (1b) dargestellt:<br />
• Hydrolyse:<br />
Si(OC 2 H 5 ) 4 + 4 H 2 O<br />
Si(OH) 4 + 4 C 2 H 5 OH (1a)<br />
• Polykondensation:<br />
Si(OH) 4 SiO 2 + 2 H 2 O (1b)<br />
Der Prozess der Partikelbildung ist durch eine Keimbildung mit einer nachfolgenden Wachstumsreaktion<br />
und Ostwald-Reifung zu erklären. Ist die Keimbildung und das Wachstum in<br />
der Ausgangslösung abgeschlossen, kann durch eine weitere, geringe Zugabe von TEOS ein<br />
Wachstumsprozess der Keime hervorgerufen werden, ohne dass ein zweiter Keimbildungsprozess<br />
auftritt.<br />
Der Partikeldurchmesser hängt sowohl von der Konzentration des TEOS bzw. des Wassers im<br />
Ethanol als auch von der Reaktionstemperatur ab. Der Vorteil des Prozesses ist die Herstellung<br />
von nahezu monodispersen, kugelförmigen Partikeln mit einer kontrolliert einstellbaren<br />
Größe. Als Nachteil ist zu erwähnen, dass die Reaktion bei geringen Partikelkonzentrationen<br />
durchgeführt werden muss.<br />
2.4 Kinetik der Partikelbildung – Morphologie von Siliziumdioxid<br />
Die Geschwindigkeit der Partikelbildung von Siliziumdioxid hängt einerseits von der Konzentration<br />
des Wassers ab, eine höhere Konzentration des Wassers beschleunigt die Hydrolysereaktion<br />
und somit die Partikelbildung selbst, anderseits beeinflusst der pH-Wert des Reaktionsmediums<br />
die Geschwindigkeiten der beiden Teilreaktionen, Hydrolyse und Polykonden-<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
6<br />
sationsreaktion. In einem sauren Reaktionsmedium verläuft die Teilreaktion der Hydrolyse<br />
wesentlich schneller als die Teilreaktion der Polykondensation. Im basischen Reaktionsmedium<br />
ist dagegen die Polykondensation wesentlich schneller als die Hydrolyse. Ursache dafür<br />
ist, daß die Hydrolyse und die Polykondensation sowohl nach einem säurekatalysierten Reaktionsmechanismus,<br />
als auch nach einem basekatalysierten Reaktionsmechanismus chemisch<br />
ablaufen können. Das führt dazu, dass im sauren pH-Bereich es zu einer Anreicherung des<br />
reaktiven Zwischenproduktes Siliziumtetrahydroxides Si(OH) 4 kommt, im basischen pH-<br />
Bereich aber zu einer Verarmung an Si(OH) 4 . Für die Partikelbildung hat dies zur Folge, dass<br />
in einem sauren Reaktionsmedium sich relativ viele Partikelkeime (Primärpartikel) bilden (die<br />
kritische Übersättigungskonzentration ist überschritten), während in einem basischen Reaktionsmedium<br />
nur wenige Partikelkeime vorliegen (die kritische Übersättigungskonzentration ist<br />
nur am Beginn der Reaktion überschritten), die nachfolgend nur wachsen können.<br />
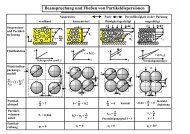
Damit lässt sich die die Bildung der Siliziumpartikel und deren Struktur mit zwei unterschiedlichen<br />
Wachstumsmodellen erklären [3].<br />
In einem sauren Reaktionsmedium neigen die Primärpartikel infolge ihrer hohen Konzentration<br />
zur Agglomeration, es entsteht ein dreidimensionales polymerartiges Netzwerk (Gelstruktur).<br />
Dieser Mechanismus wird als Reaction-limited cluster aggregation RLCA bezeichnet.<br />
Die Agglomerate haben eine poröse Struktur mit kleinen Poren (Abb. 2).<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
7<br />
pH < 7<br />
pH 7- 10 bei Anwesenheit von Salzen<br />
Si(OH)<br />
4<br />
Dimere<br />
Oligomere<br />
Partikel<br />
1 nm<br />
pH 7- 10 bei Abwesenheit von Salzen<br />
5 nm<br />
10 nm<br />
30 nm<br />
100 nm<br />
dreidimensionales Gel-<br />
Netzwerk<br />
Sol (Stöber-Partikel)<br />
Abb. 2:<br />
Morphologie von Siliziumdioxid-Partikeln<br />
In einem basischen Reaktionsmedium tritt infolge der geringeren Konzentration der Primärpartikel<br />
keine Agglomeration auf, sondern die Primärpartikel wachsen durch die Anlagerung<br />
von Si(OH) 4 (bis zur Erreichung der Sättigungskonzentration des Siliziumdioxides). Dieser<br />
Mechanismus wird Reaction-limited monomer cluster growth RLMC genannt. Es entstehen<br />
nichtporöse, kugelförmige, nahezu monodisperse Partikelsysteme. Diese Partikel werden auch<br />
als Stöber-Partikel bezeichnet.<br />
Liegen allerdings im basischen Reaktionsmedium zusätzlich Fremdsalze vor, verringern diese<br />
die Stabilität der Primärpartikel gegen Agglomeration, so dass hier ebenfalls der RLCA-<br />
Wachstumsmechanismus vorherrscht.<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
8<br />
2.5 Synthese von Titan (IV) - oxid : Sol - Gel - Fällungsprozess<br />
Die Herstellung von Nanopartikel aus Titan(IV) - oxid ist u.a. durch Umsetzung von Tetraisopropyl-orthotitanat<br />
Ti(OC 3 H 7 ) 4 in einer salpetersauren, wässrigen Lösung möglich. Der<br />
Herstellungsprozess besteht aus drei Teilreaktionen (Gl. 2a bis Gl. 2c). Die erste Teilreaktion<br />
ist eine Hydrolyse von Ti(OC 3 H 7 ) 4 , bei der Titan(IV) - hydroxid und Isopropanol gebildet<br />
werden. Der zweite Teilschritt ist eine nachfolgende Polykondensationsreaktion von Ti(OH) 4<br />
zu makroskopischem Titan(IV) - oxid.<br />
Bei der dritten Teilreaktion wird das Titan (IV) - oxid - Gel bis zu einem nanoskaligen Titan<br />
(IV) - oxid - Sol mechano-chemisch redispergiert (Gl. 2c).<br />
• Hydrolyse:<br />
wässrige Suspension, 50 °C Ti(OH) 4 + 4C 3 H 7 OH<br />
Ti(OC 3 H 7 ) 4 + 4 H 2 O<br />
pH 1,3 (0,1 M HNO 3 )<br />
Tetraisopropylorthotitanat Titan (IV) - hydroxid Isopropanol<br />
(2a)<br />
• Polykondensation :<br />
Ti(OH) 4<br />
wässrige Suspension, 50 °C TiO 2 + 2 H 2 O (2b)<br />
pH 1,3 (0,1 M HNO<br />
Titan (IV) – hydroxid<br />
3 )<br />
Titan (IV) - oxid<br />
• Chemische Redispergierung:<br />
wässrige Suspension, 50 °C<br />
TiO 2 (Gel) nano - TiO 2 (Sol)<br />
Titan (IV) – oxid<br />
pH 1,3 (0,1 M HNO 3 )<br />
Titan (IV) - oxid<br />
(2c)<br />
Auf dieser Weise ist die Herstellung von Partikeln in der Größenordnung von 10 nm bis 30<br />
nm möglicht. Zu Beginn des Fällungsprozesses werden augenblicklich in der Suspension polydisperse<br />
Agglomeratstrukturen mit einem mittleren Durchmesser von 150 µm bis 180 µm<br />
erzeugt.<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
9<br />
Infolge der Wechselwirkung zwischen den Hydroxylgruppen des Ti(OH) 4 und den Protonen<br />
H + der Salpetersäure HNO 3 entsteht eine elektrisch positiv geladene Oberfläche, weil die H + -<br />
Ionen an der Oberfläche adsorbiert werden. Mittels (mechano)-chemischer Redispergierung<br />
(Peptisation) können nahezu monomodale Partikelverteilungen erzeugt werden. Die Salpetersäure<br />
stabilisiert die Suspension.<br />
2.6 Experimentelle Methoden<br />
2.6.1 Ermittlung der Partikelgrößenverteilung – Photonenkorrelationsspektroskopie<br />
Zur Messung der Partikelgrößenverteilung und der mittleren Partikelgröße der synthetisierten<br />
nanoskaligen Partikel wird die Photonenkorrelationsspektroskopie (PCS) angewendet. Bei der<br />
Photonenkorrelationsspektroskopie wird die Intensitätsfluktuation des Streulichts der Partikel<br />
gemessen.<br />
Diese Fluktuationen sind auf die Brownsche Molekularbewegug (Selbstdiffusion der Partikel)<br />
zurückzuführen. Aus den Diffusionskoeffizienten der Partikel wird der hydrodynamische<br />
Durchmesser nach der Stokes-Einsteinschen Gleichung erhalten, der die Bewegung der Partikel<br />
in der Flüssigkeit beschreibt.<br />
Die Auswertung ist bei der Kenntnis der Wellenlänge des Lasers, des Streuwinkels und des<br />
Brechungsindexes der Lösung möglich. Über eine Autokorrelationsfunktion der Intensitätsfluktuationen<br />
ist eine direkte Möglichkeit zur Bestimmung des Diffusionskoeffizienten gegeben.<br />
Aus den Messungen erhält man eine streulichtintensitätsgewichtete Partikelgrößenverteilung.<br />
2.6.2 Ermittlung des Stabilitätsverhalten - Zetapotentialbestimmung<br />
Eine Suspension wird als stabil angesehen, wenn die erzeugten Nanopartikel in der Flüssigkeit<br />
isoliert vorliegen und nicht wieder zu größeren Einheiten agglomerieren. Die Stabilität<br />
von Dispersionen kann auf der Basis der DLVO - Theorie (Derjaguin, Landau, Verwey,<br />
Overbeek) verstanden werden, in der die Gesamtpotentialwechselwirkung zwischen den Partikeln<br />
durch Addition der van-der-Waals- und der elektrostatischen Potentiale beschrieben<br />
wird. Eine Suspension ist dann stabil, wenn die abstoßend wirkende elektrostatische Kraft die<br />
van-der-Waals-Kraft übersteigt. Damit wird zwischen den Partikeln eine im Vergleich zur<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
10<br />
thermischen Energie ausreichend hohe repulsive Energiebarriere erzeugt. Die Stabilität von<br />
Suspensionen kann durch das Zetapotential als Funktion des pH-Wertes beeinflusst werden.<br />
Bewegt sich ein mit einer elektrochemischen Doppelschicht umgebendes Nanopartikel im<br />
elektrischen Feld relativ zur Flüssigkeit, so wird ein Teil der diffusen Doppelschicht vom Partikel<br />
abgestreift und es entsteht eine Potentialdifferenz. Dieses Potential an der sogenannten<br />
Scherebene wird als Zetapotential bezeichnet und lässt sich durch elektrokinetische Messungen,<br />
wie z.B. Elektrophorese, bestimmen.<br />
3. Aufgabestellung und Versuchsdurchführung<br />
3.1 Aufgabenstellungen<br />
1. Herstellung von nanoskaligen Partikeln aus Siliziumdioxid nach Stöber, Fink und<br />
Bohn [4]:<br />
Die Erzeugung der Siliziumdioxidpartikel erfolgt durch Umsetzung von Tetraethylorthosilicat<br />
Si(OC 2 H 5 ) 4 (TEOS) in einer Mischung aus Isopropanol, Wasser und<br />
Ammoniak in einem Laborfällungsreaktor. Es ist die Konzentration des Tetraethylorthosilicat<br />
(TEOS) in 2 Versuchsreihen zu variieren (Temperatur und Rührerumfangsgeschwindigkeit<br />
bleibt konstant). Es sollen die Induktionszeiten bestiimt werden.<br />
Das ist der Zeitpunkt, bei dem die erste Trübung der Lösung erfolgt.<br />
2. Charakterisierung der Siliziumdioxidpartikel während des Prozessfortschrittes:<br />
Für die experimentelle Ermittlung der Partikelgrößenverteilung während der Nanopartikelbildung<br />
steht die Methode der Photonenkorrelationsspektroskopie (PCS) zur Verfügung.<br />
Es werden kontinuierlich Proben aus dem Fällungsreaktor entnommen und<br />
anschließend mit dem Photonenkorrelationsspektrometer charakterisiert.<br />
Es ist die zeitliche Veränderung:<br />
• der Partikelgrößenverteilungsfunktion Q o<br />
(d) und<br />
• des mittleren Partikeldurchmessers<br />
d<br />
50,0<br />
darzustellen und anschließend zu diskutieren.<br />
3. Charakterisierung der Stabilität der entstandenen Siliziumdioxidpartikel:<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
11<br />
Zur Ermittlung der Stabilität der entstandenen Suspensionen wird das Zetapotential<br />
bestimmt. Die Ergebnisse sollen ausführlichen diskutiert werden.<br />
4. Charakterisierung der nanoskaliger Titan(IV) – oxidpartikel:<br />
Im Vergleich zu den Siliziumdioxidpartikeln soll der Dispersionszustand und das Stabilitätsverhaltnes<br />
einer Suspension mit nanoskaligem Titan (IV) - oxid untersucht<br />
werden.<br />
Zu ermitteln sind:<br />
• die Partikelgrößenverteilungsfunktion Q o<br />
(d)<br />
• die Partikelgrößenverteilungsdichte q ( d )<br />
0<br />
• die mittleren Partikeldurchmesser<br />
• das Zetapotential.<br />
d<br />
50,0<br />
Es sollen die Partikelgrößenverteilungen und mittleren Durchmesser von SiO 2 und Titan(IV)-oxid<br />
im Gleichgewichtszustand verglichen werden.<br />
5. Berechnung des kritischen Keimbildungsradius , der kritischen Keimbildungskonzentration<br />
*<br />
C n<br />
und Partikelgröße der Siliziumpartikel beim Fällungsprozess:<br />
r krit<br />
Aus der Konzentration des Tetraethylorthosilicates (TEOS) im Reaktionsgemisch<br />
können die resultierende relative Übersättigung S, der kritische Keimbildungsradius<br />
r krit<br />
*<br />
, die kritische Keimbildungskonzentration sowie die Partikelgröße der Siliziumdioxidpartikel<br />
berechnet werden. Die Ergebnisse sollen mit den experimentellen<br />
Ergebnissen verglichen und aus dem Blickwinkel der Keimbildung- und Wachstumstheorie<br />
zur Diskussion gestellt werden. (vgl. Punkt 4.2 und 4.3)<br />
C n<br />
6. Charakterisierung der Hydrodynamik im Fällungsreaktor:<br />
Hier sind die Reynolds-Zahl, der Leistungseintrag des Rührers und der mittlere Schergradient<br />
.<br />
γ<br />
zu berechnen.<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
12<br />
3.2 Versuchsdurchführung<br />
3.2.1 Synthese und Charakterisierung der Siliziumdioxidpartikeln<br />
Zur Synthese von Siliziumdioxidpartikel nach Stöber werden sind zwei Laboransätze durchgeführt<br />
(Variation der Konzentration von Tetraethyl-orthosilicat TEOS). Das führt zu unterschiedlichen<br />
relativen Übersättigungen und Induktionszeiten!!<br />
Die Synthese wird in einem 0.25 l Fällungsreaktor bei konstanter Temperatur (25 °C) und<br />
konstanter Rührerdrehzahl (500 min -1 ) durchgeführt. Es wird ein Scheibenrührer benutzt, auf<br />
Strombrecher wird verzichtet. Eine Darstellung des Fällungsreaktors ist in Abb. 3 gegeben.<br />
Antrieb<br />
Rührer<br />
Fällungsreaktor<br />
Thermostat<br />
Abb. 3: Fällungsreaktor zur Synthese von Siliziumdioxid - Nanopartikeln<br />
Es wird eine Mischung aus 72 ml Wasser und 109 ml Isopropanol (C 3 H 7 OH) im Fällungsreaktor<br />
vorgelegt. Die Rührerdrehzahl wird auf 1000 min -1 eingestellt, die Mischung wird für<br />
einen Zeitraum von ca. 45 Sekunden homogenisiert. Anschließend werden 12 ml Ammoniak<br />
(25 % NH 4 OH) mit einer Pipette zur Wasser-Alkohol-Mischung vorsichtig dosiert. Danach<br />
wird die entsprechende Menge Tetraethylorthosilicat Si(OC 2 H 5 ) 4 zugegeben (Ansatz 1: 7,25<br />
ml, Ansatz 2: 4,0 ml, Dichte TEOS 0,934 g cm -3 ).<br />
Am Anfang ist die Lösung farblos, nach einem kurzen Zeitraum bekommt die Mischung<br />
eine leicht bläuliche, trübe Farbe infolge der Partikelbildung. Dieser Zeitraum wird als Induktionszeit<br />
bezeichnet. Die Induktionszeit wird mit einer Stoppuhr gemessen. Danach werden<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
13<br />
Proben der Suspension nach 2, 5, 7, 15, 30, 45 und 60 Minuten aus dem Fällungsreaktor entnommen.<br />
Die Probenahme erfolgt mit einer Plastikspritze. Die Proben werden immer von ein<br />
und derselben Stelle im Reaktor entnommen, mit destilliertem Wasser verdünnt. Die Partikelgrößenverteilungen<br />
werden mit dem Photonenkorrelationsspektrometer bestimmt.<br />
Nach dem Reaktionsende wird das Zetapotential der Siliziumdioxid-Nanopartikel in der Suspension<br />
gemessen.<br />
3.2.2 Charakterisierung der Titan(IV) - oxidpartikel<br />
Von einer bereitgestellten Suspension mit Titan(IV) - oxid - Nanopartikel werden die Partikelgrößenverteilung<br />
und das Zetapotential bestimmt. Diese Nanopartikel wurden nach dem<br />
Sol-Gel-Fällungsprozess (Punkt 2.4) synthetisiert. Die Messung der Partikelgrößenverteilung<br />
erfolgt ohne vorherige Verdünnung. Je Probe sind 3 Messungen durchzuführen.<br />
4. Versuchsauswertung und Diskussion der Ergebnisse<br />
4.1 Berechnung und Darstellung der Partikelgrößenverteilungen<br />
Aus der Photonkorrelationsspektroskopie erhält man die Mengenanteile µ ( d ) der jeweiligen<br />
Partikelgrößenklasse. Durch Aufsummieren der Mengenanteile kann die Partikelverteilungsfunktion<br />
Q(d<br />
i ) nach Gl. (3) berechnet werden.<br />
0<br />
0 i<br />
d<br />
∫<br />
∑<br />
Q ( d ) = q ( d ) ⋅d( d ) = µ (3)<br />
0<br />
i<br />
d<br />
u<br />
0<br />
n<br />
i=<br />
1<br />
0,i<br />
Die Partikelgrößenverteilungsdichte ( d ) bestimmt sich nach der Gl. (4):<br />
q ( d<br />
0<br />
q 0<br />
dQ ( d )<br />
µ<br />
0<br />
0,i<br />
i− 1...d<br />
i<br />
) = =<br />
(4)<br />
d( d ) ∆di<br />
wobei<br />
∆d<br />
i<br />
= d<br />
i<br />
− d<br />
i−1<br />
die Klassenbreite ist.<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
14<br />
Die entsprechenden Partikelgrößenverteilungen, Partikelverteilungsdichten und Mediandurchmesser<br />
der Partikel sind zu berechnen und gegen die Reaktionszeit graphisch darzustellen.<br />
4.2 Berechnung der relativen Übersättigung<br />
Die relative Übersättigung S ist definiert als das Verhältnis der tatsächlichen Konzentration in<br />
der übersättigten Reaktionslösung und der Sättigungskonzentration des Stoffes (Gl. 5).<br />
C<br />
SiO<br />
= (5)<br />
C<br />
S<br />
2<br />
S<br />
wobei<br />
CSiO 2<br />
die Massenkonzentration des SiO2 in der übersättigten Reaktionslösung und<br />
C<br />
S<br />
die Sättigungskonzentration des SiO 2 ist.<br />
Die Sättigungskonzentration<br />
C S<br />
(in ppm - parts per million) wird nach Gl. (6) berechnet:<br />
731<br />
log c S<br />
= − + 4,52<br />
(6)<br />
T<br />
wobei T die absolute Temperatur ist.<br />
4.3 Berechnung des kritischen Keimbildungsradius , der Anzahlkonzentration der<br />
kritischen Keime<br />
*<br />
C n<br />
und der Partikelgröße<br />
r krit<br />
Zur Berechnung des kritischen Keimbildungsradius<br />
r krit<br />
wird Gleichung (7) benutzt:<br />
r<br />
krit<br />
2⋅σ<br />
SiO<br />
M<br />
2 SiO2<br />
= (7)<br />
R ⋅T<br />
⋅ln S ρ<br />
s<br />
wobei σ<br />
SiO<br />
die Grenzflächenspannung Siliziumdioxid/ Wasser,<br />
2<br />
M<br />
SiO 2<br />
die Molmasse von Siliziumdioxid,<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
15<br />
ρ<br />
S<br />
S<br />
die Feststoffdichte der Partikel und<br />
die relative Übersättigung ist.<br />
Die Konzentration der kritischen Keime<br />
Boltzmann (Gl. 8):<br />
*<br />
C n<br />
folgt einer Energieverteilung nach Maxwell-<br />
C<br />
*<br />
n<br />
⎡ ∆G<br />
= CS<br />
exp⎢<br />
−<br />
⎣ kT<br />
max<br />
⎤<br />
⎥<br />
⎦<br />
(8)<br />
wobei ∆ Gmax<br />
die freie Keimbildungsenthalpie ist.<br />
Die freie Keimbildungsenthalpie läßt sich nach Gleichung (9) berechnen:<br />
3 2<br />
16 ⋅π<br />
⋅σ<br />
SiO<br />
⋅ M<br />
2 SiO2<br />
∆ Gmax<br />
=<br />
(9)<br />
2<br />
2<br />
3⋅<br />
ρ ( R ⋅T<br />
⋅ln S )<br />
Der Partikeldurchmesser der Siliziumpartikel kann anschließend aus der Stoffmenge (Masse)<br />
des gebildeten Siliziumdioxides, dessen Feststoffdichte und der Konzentration der kritischen<br />
Keime<br />
*<br />
C n<br />
berechnet werden.<br />
4.4 Berechnung der Reynolds - Zahl, des Leistungseintrags und des mittleren Schergradienten<br />
Um die Hydrodynamik im Fällungsreaktor zu charakterisieren, soll die Reynolds - Zahl des<br />
Rührers berechnet werden. Die Reynolds - Zahl ist mit Gl. (10) bestimmbar.<br />
Re<br />
R<br />
=<br />
2<br />
n ⋅ d<br />
R<br />
⋅ ρ<br />
η<br />
(10)<br />
mit<br />
d R<br />
ρ<br />
n<br />
der Rührerdurchmesser,<br />
die Dichte der Suspension,<br />
die Rührerdrehzahl und<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
16<br />
η<br />
die dynamische Viskosität.<br />
Der Leistungseintrag P wird aus Gl. (11) erhalten:<br />
P = c ⋅ ρ ⋅ n ⋅<br />
(11)<br />
3 5<br />
w<br />
d R<br />
wobei<br />
c w<br />
der Leistungsbeiwert ist.<br />
Der Leistungsbeiwert<br />
c w<br />
hängt vom Rührer, der geometrischen Anordnung im Behälter und<br />
den Kennzahlen, die die Strömung charakterisieren, ab. Für einen radialfördernden Scheibenrührer<br />
(6 Schaufeln) beträgt der Leistungsbeiwert 5,8.<br />
Der mittlere Schergradient γ lässt sich nach der Gl. (12) berechnen. Zur Berechnung der turbulenten<br />
Dissipationsenergie ε wird Gl. (13) benutzt.<br />
.<br />
1<br />
2<br />
.<br />
⎛ ε ⎞<br />
γ = ⎜ ⎟<br />
(12)<br />
⎝ υ ⎠<br />
⎛<br />
3 5<br />
⎞<br />
⎜<br />
cw<br />
⋅n<br />
⋅d<br />
R<br />
ε = ⎟<br />
(13)<br />
⎝ VSusp<br />
⎠<br />
4.5 Diskussion der Ergebnisse<br />
- Wie wird die Partikelgrößenverteilung sowie deren zeitliche Veränderung während der<br />
Synthese von der relativen Übersättigung beeinflusst?<br />
- Schätzen sie den Einfluß der relativen Übersättigung auf die Werte des kritischen Keimbildungsradius<br />
und der Anzahl der kritischen Keime ein? Vergleichen Sie ihre vorausberechneten<br />
und experimentellen Werte. Welche Aussagen können über Keimbildungs- und<br />
Wachstumsphase gemacht werden?<br />
- Diskutieren Sie die möglichen Ursachen für auftretende Unterschiede des Zetapotentials<br />
für die Suspensionen mit Siliziumdioxid- und Titan (IV) - oxidpartikel. Machen Sie Aussagen<br />
zur Stabilität der Nanopartikel.<br />
5. Hinweise zur <strong>Praktikum</strong>sdurchführung<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
17<br />
Anhand der nachfolgend aufgeführten Stichworte können Sie Ihr Wissen überprüfen bzw.<br />
zusätzlich ergänzen.<br />
Stichworte zur Vorbereitung<br />
Fällungsprozess, Keimbildung, Wachstum, relative Übersättigung, Sol-Gel-Prozess, Hydrolyse,<br />
Polykondensation, Redispergierung, Partikelmorphologie, Kinetik der Partikelbildung,<br />
Partikelgrößenverteilung, mittlere Partikelgrößen, kolloidale Stabilität, Zetapotential, Photonkorrelationsspektroskopie,<br />
Kennzahlen der Hydrodynamik<br />
6. Arbeitsschutz und Sicherheitsvorschriften<br />
Bei der Durchführung des <strong>Praktikum</strong>s ist der Gesundheits- und Arbeitsschutz einzuhalten<br />
(Laborordnung, Betriebsanweisung, Gefahrstoffdatenblätter)! Es sind Schutzbrille, Handschuhe<br />
and entsprechende Laborkleidung (Kittel) zu tragen.<br />
7. Symbolverzeichnis<br />
C SiO2 Massenkonzentration des SiO 2<br />
C S Sättigungskonzentration der SiO 2 [in ppm !!!]<br />
c w<br />
d i<br />
d 50,3<br />
d R<br />
∆ G max<br />
k<br />
M<br />
C n<br />
*<br />
n<br />
P<br />
Q 0 (d)<br />
q 0 (d)<br />
Re<br />
Leistungsbeiwert<br />
Partikeldurchmesser<br />
mittlerer Durchmesser (Mediandurchmesser)<br />
Rührerdurchmesser<br />
freie Keimbildungsenthalpie<br />
Boltzmann - Konstante<br />
Molmasse<br />
Konzentratration kritischer Keime (Mengenart Anzahl)<br />
Rührdrehzahl<br />
Leistungseintrag des Rührers<br />
Partikelgrößenverteilungsfunktion (Mengenart Anzahl)<br />
Partikelgrößenverteilungsdichte<br />
Reynolds-Zahl<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas
18<br />
R<br />
r krit<br />
S<br />
T<br />
allgemeine Gaskonstante<br />
kritischer Keimbildungsradius<br />
relative Übersättigung<br />
Temperatur<br />
Griechische Symbole<br />
σ<br />
ρ<br />
ρ<br />
S<br />
η<br />
.<br />
γ<br />
ε<br />
Grenzflächenspannung<br />
Fluiddichte<br />
Feststoffdichte<br />
dynamische Viskosität<br />
mittlerer Schergradient<br />
turbulente Dissipationsenergie<br />
8. Literaturverzeichnis<br />
[1] Sugimoto, T.: Fine Particles, Synthesis, Characterization, and Mechanism of Growth<br />
(Surfactant Science Ser. 92), Marcel Dekker Inc., New York 2000<br />
[2] Schubert, U.; Hüsing, N.: Synthesis of Inorganic Materials, WILEY-VCH, New York,<br />
2000<br />
[3] Brinker, C.J.; Scherer, G.W.: Sol-Gel-Science, The Physics and Chemistry of Sol-Gel-<br />
Science, Academic Press, San Diego 1990<br />
[4] Stöber, W.; Fink, A.; Bohn, E.: Controlled Growth of Monodisperse Silica Spheres in<br />
Micron Size Range, J. Colloid and Interface Sci. 26 (1968) 62 - 69<br />
[5] Giesche, H.: Synthesis of Monodisperse Silica Powders I. Particle Properties and Reaction<br />
Kinetics, Journal of European Ceramic Society, 14 (1994) 189 - 204<br />
<strong>Praktikum</strong> <strong>Nanopartikelfällung</strong> WS 2005/2006<br />
Prof. Dr.-Ing.habil. Jürgen Tomas