"Alkane - wichtige Energieträger" aus Allgemeine Chemie: Theorie ...
"Alkane - wichtige Energieträger" aus Allgemeine Chemie: Theorie ...
"Alkane - wichtige Energieträger" aus Allgemeine Chemie: Theorie ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
ÜBUNGEN ZUM THEMA<br />
"<strong>Alkane</strong> - <strong>wichtige</strong> Energieträger"<br />
<strong>aus</strong> <strong>Allgemeine</strong> <strong>Chemie</strong>: <strong>Theorie</strong> und Praxis (Baars / Christen)<br />
1. Weshalb gibt es so viele organische Verbindungen?<br />
2. Erklären Sie die Erscheinung, dass Kohlenwasserstoffe reaktionsträge Verbindungen sind,<br />
jedoch eine geringe Wärmebeständigkeit besitzen.<br />
3. Siliciumwasserstoffverbindungen sind sehr unbeständige Stoffe. Nennen Sie zwei Gründe<br />
dafür.<br />
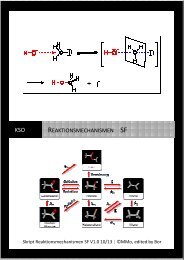
4. Geben Sie die Lewis-Formeln von drei funktionellen Gruppen an.<br />
5. Begründen Sie, weshalb die Trennungs- und Reinigungsoperationen für den praktisch<br />
arbeitenden organischen Chemiker grosse Bedeutung haben.<br />
6. Eine organische Substanz enthält <strong>aus</strong>ser Sauerstoff 40.12% Kohlenstoff und 6.75%<br />
Wasserstoff. 100mL ihres Dampfes wiegen bei Normbedingungen 0.268g. Geben Sie die<br />
Molekülformel an und schlagen Sie eine mögliche Lewis-Formel vor.<br />
7. 0.2g einer organischen Verbindung verbrennen zu 0.456g CO2 und 0.186g Wasser. Weitere<br />
Verbrennungsprodukte können nicht nachgewiesen werden. 0.25g der Substanz ergeben<br />
beim Verdampfen 96.5mL Dampf (bei Normbedingungen). Berechnen Sie die Molekülformel<br />
und geben Sie zwei mögliche Lewis-Formeln an.<br />
8. Stellen Sie die Lewis-Formeln für alle möglichen Isomere der Molekülformel C7H16 auf.<br />
9. Benennen Sie alle Verbindungen der Aufgabe 8.<br />
10. Schreiben Sie die Lewis-Formeln folgender Verbindungen: 4-Ethyl-2-methyloctan; 2,2,3,3-<br />
Tetramethylhexan; 2,3,4-Trimethylpentan.<br />
11. Erklären Sie den Unterschied in den Schmelz- und Siedepunkten der beiden Isomere Butan<br />
(Smp: -138°C, Sdp: -0.5°C) und 2-Methylpropan (Smp: -159.4°C, Sdp: -11.7°C).<br />
12. Wie viele Isomere können bei der Reaktion von 1mol Hexan mit 1mol Brom entstehen?<br />
Benennen Sie die möglichen Isomere.<br />
13. Weshalb sollte der Verbrauch an Halogenalkanen als Lösemittel möglichst eingeschränkt<br />
werden?<br />
14. Zeichnen Sie die Lewis-Formel für Ozon.<br />
15. Aus welchen Gründen werden die Freone (Kohlenwasserstoffe mit Fluor und/oder Chlor) für<br />
viele technische Zwecke verwendet?<br />
Bor 2013
16. Beschreiben Sie den Einfluss der Fluorchlorkohlenwasserstoffe (FCKW) auf den Ozongehalt<br />
der Stratosphäre.<br />
17. Welche Ersatzstoffe bieten sich für die FCKW's an?<br />
18. Was versteht man unter dem Ozonloch?<br />
!! Lösungen zu den Fragen sind bei M.Borer erhältlich !!<br />
Bor 2013