Dokument 1.pdf
Dokument 1.pdf
Dokument 1.pdf
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
mengesetzt, wobei meist ein Zentralteilchen, i. d.<br />
R. ein Metallkation, von so genannten Liganden<br />
(Nichtmetallmoleküle z. B. NO 3 - , Cl - oder NH3<br />
sowie organische Verbindungen, z. B. Huminsäuren)<br />
umgeben wird. Die Art und Anzahl der Liganden<br />
sowie die räumliche Lage der Liganden und<br />
Zentralteilchen sind für jeden Komplex charakteristisch<br />
und prägt dessen chemische Eigenschaften.<br />
Platin als Zentralteilchen wird meist von<br />
vier bzw. sechs Liganden umgeben. Palladium<br />
wird dagegen meist von zwei bis vier Teilchen<br />
umgeben, und in Rhodium-Komplexen ist darüber<br />
hinaus auch die Koordinationszahl drei anzutreffen.<br />
Komplexe können ebenso wie Moleküle<br />
eine positive oder negative Ladung tragen.<br />
Redox-Potenzial: Die meisten chemischen Reaktionen<br />
müssen als Umgruppierung von Verknüpfungen<br />
zwischen Atomen und Molekülen und<br />
damit als Verschiebung von Ladungsträgern<br />
(Elektronen) aufgefasst werden. Als Maß für die<br />
Triebkraft dieser Verschiebung zwischen zwei Reaktionspartnern<br />
(Molekülen oder Komplexen)<br />
kann in Lösung die elektrische Spannung (Potenzial-Differenz),<br />
die sich zwischen diesen aufbaut,<br />
herangezogen und auch gemessen werden.<br />
Diese Spannungsdifferenz wird als Redox-Potenzial<br />
bezeichnet. Die Kenntnis des Redox-Potenzials<br />
erlaubt eine Vorhersage über den Ablauf von<br />
Reaktionen. Als Bezugssystem wird die (formale)<br />
„Verknüpfung“ von zwei Wasserstoffionen mit<br />
Hilfe von zwei Elektronen zu einem Wasserstoffmolekül<br />
gewählt und dessen Potenzial gleich null<br />
gesetzt. Ein positives Redox-Potenzial bedeutet,<br />
dass dieser Stoff leicht Elektronen aufnehmen<br />
kann; dieser Vorgang wird als Reduktion bezeichnet.<br />
Ein negatives Redox-Potenzial bedeutet<br />
demzufolge, dass der Reaktionspartner Elektronen<br />
leichter abgibt; diesen Vorgang bezeichnet<br />
man als Oxidation. Reduktion und Oxidation können<br />
niemals unabhängig voneinander ablaufen:<br />
M. a. W., eine Oxidation tritt immer neben einer<br />
Reduktion auf; ein solches Reaktionspaar wird als<br />
Redox-Reaktion bezeichnet.<br />
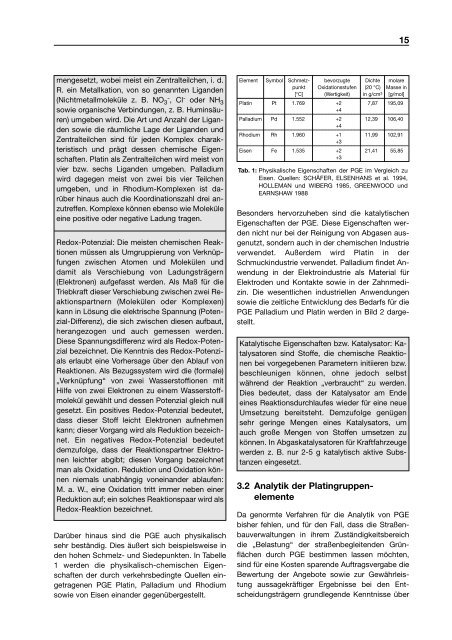
Darüber hinaus sind die PGE auch physikalisch<br />
sehr beständig. Dies äußert sich beispielsweise in<br />
den hohen Schmelz- und Siedepunkten. In Tabelle<br />
1 werden die physikalisch-chemischen Eigenschaften<br />
der durch verkehrsbedingte Quellen eingetragenen<br />
PGE Platin, Palladium und Rhodium<br />
sowie von Eisen einander gegenübergestellt.<br />
Besonders hervorzuheben sind die katalytischen<br />
Eigenschaften der PGE. Diese Eigenschaften werden<br />
nicht nur bei der Reinigung von Abgasen ausgenutzt,<br />
sondern auch in der chemischen Industrie<br />
verwendet. Außerdem wird Platin in der<br />
Schmuckindustrie verwendet. Palladium findet Anwendung<br />
in der Elektroindustrie als Material für<br />
Elektroden und Kontakte sowie in der Zahnmedizin.<br />
Die wesentlichen industriellen Anwendungen<br />
sowie die zeitliche Entwicklung des Bedarfs für die<br />
PGE Palladium und Platin werden in Bild 2 dargestellt.<br />
3.2 Analytik der Platingruppenelemente<br />
15<br />
Element Symbol Schmelz- bevorzugte Dichte molare<br />
punkt Oxidationsstufen (20 °C) Masse in<br />
[°C] (Wertigkeit) in g/cm3 [g/mol]<br />
Platin Pt 1.769 +2<br />
+4<br />
7,87 195,09<br />
Palladium Pd 1.552 +2<br />
+4<br />
12,39 106,40<br />
Rhodium Rh 1.960 +1<br />
+3<br />
11,99 102,91<br />
Eisen Fe 1.535 +2<br />
+3<br />
21,41 55,85<br />
Tab. 1: Physikalische Eigenschaften der PGE im Vergleich zu<br />
Eisen. Quellen: SCHÄFER, ELSENHANS et al. 1994,<br />
HOLLEMAN und WIBERG 1985, GREENWOOD und<br />
EARNSHAW 1988<br />
Katalytische Eigenschaften bzw. Katalysator: Katalysatoren<br />
sind Stoffe, die chemische Reaktionen<br />
bei vorgegebenen Parametern initiieren bzw.<br />
beschleunigen können, ohne jedoch selbst<br />
während der Reaktion „verbraucht“ zu werden.<br />
Dies bedeutet, dass der Katalysator am Ende<br />
eines Reaktionsdurchlaufes wieder für eine neue<br />
Umsetzung bereitsteht. Demzufolge genügen<br />
sehr geringe Mengen eines Katalysators, um<br />
auch große Mengen von Stoffen umsetzen zu<br />
können. In Abgaskatalysatoren für Kraftfahrzeuge<br />
werden z. B. nur 2-5 g katalytisch aktive Substanzen<br />
eingesetzt.<br />
Da genormte Verfahren für die Analytik von PGE<br />
bisher fehlen, und für den Fall, dass die Straßenbauverwaltungen<br />
in ihrem Zuständigkeitsbereich<br />
die „Belastung“ der straßenbegleitenden Grünflächen<br />
durch PGE bestimmen lassen möchten,<br />
sind für eine Kosten sparende Auftragsvergabe die<br />
Bewertung der Angebote sowie zur Gewährleistung<br />
aussagekräftiger Ergebnisse bei den Entscheidungsträgern<br />
grundlegende Kenntnisse über