mehratomige Gase
mehratomige Gase
mehratomige Gase
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
1.Wärmekapazität<br />
Auch für thermische Energie gilt die Energieerhaltung:<br />
Wir stellen uns vor, dass wir einem Gas durch Heizung die Wärmemenge Q<br />
zuführen:<br />
Körper oder Gas Körper oder Gas<br />
m,T, V m, T+∆T,V<br />
Q von außen<br />
Die Energieerhaltung fordert, dass die gesamte Energie Q zur Temperaturerhöhung<br />
verwendet wird:<br />
Q = cm∆T<br />
Diese Gleichung definiert die Wärmekapazität c<br />
1
Die Einheit der Wärmekapazität ist:<br />
[] c<br />
=<br />
[ Q]<br />
J<br />
=<br />
[ m][<br />
T ] kg ⋅ K<br />
Gemessen wird die Wärmekapazität mit einem Kalorimeter. Die einfachste<br />
Form ist das Tauchkalorimeter, bei der eine Probe m2 mit der unbekannten<br />
Wärmekapazität c2 auf die Temperatur T2 aufgeheizt wird und dann in ein<br />
Wasserbad der Masse m1, der bekannten Wärmekapazität c1 und der Temperatur T1 geworfen wird:<br />
vorher<br />
nachher<br />
Probe c 2?,m 2T 2<br />
H 2O<br />
c 1,m 1,T 1<br />
H 2O<br />
c 1,m 1,T 0<br />
Probe<br />
c 2?,m 2T 0<br />
Nach der Einstellung des Gleichgewichtes hat man die Messgrößen m 1, m 2<br />
T 1,T 2,T 0 und c 1=4187 J/(kgK) für H 2O und man kann<br />
2
die unbekannte Wärmekapazität c 2 berechnen:<br />
abgegebene Wärmemenge = aufgenommene Wärmemenge<br />
c<br />
2<br />
m<br />
2<br />
( T<br />
2<br />
c<br />
Experiment Kalorimeter<br />
−T<br />
2<br />
=<br />
0<br />
)<br />
c<br />
1<br />
=<br />
c<br />
m<br />
(<br />
m<br />
1<br />
1<br />
2<br />
m<br />
1<br />
( T<br />
T<br />
)(<br />
T<br />
0<br />
2<br />
0<br />
−T<br />
−T<br />
−T<br />
1<br />
0<br />
1<br />
)<br />
)<br />
oder<br />
Für höhere Genauigkeit muss man die Wärmekapazität des Gefäßes mit<br />
berücksichtigen<br />
Bei der experimentellen Bestimmung der Wärmekapazität sind verschiedene<br />
Definitionen üblich. Man kann einmal die Wärmekapazität auf ein Mol einer<br />
Substanz beziehen (Molare Wärmekapazität C) und man muss berücksichtigen,<br />
ob die Messung bei konstantem Druck (CP) oder konstantem Volumen (CV) bestimmt wurde:<br />
3
c P,c V: Wärmekapazität pro kg [J/(kg K]<br />
C P, C V: Molare Wärmekapazität [J/(Mol K]<br />
Wärmekapazität von idealen <strong>Gase</strong>n<br />
Bei idealen <strong>Gase</strong>n kann man die Wärmekapazität leicht ausrechen:<br />
Bei konstantem Volumen gibt es für ein Mol eines <strong>Gase</strong>s<br />
den einfachen Zusammenhang<br />
1 2<br />
Ekin. gesamt = M Mol v<br />
2<br />
=<br />
3<br />
2<br />
RT<br />
Q erzeugt eine Temperaturerhöhung um ∆T, also gilt:<br />
Q = CV<br />
∆T<br />
= R∆T<br />
2<br />
3 also<br />
Bei konstantem Druck muss man beachten, dass die Temperaturerhöhung<br />
um ∆T einmal genau wie oben zu einer Erhöhung der kinetischen Energie<br />
3<br />
um R∆T<br />
führt.<br />
2<br />
C V<br />
=<br />
3<br />
2<br />
R<br />
4
Zusätzlich folgt aus der Zustandsgleichung eine Änderung des Volumens um ∆V<br />
gemäß der Beziehung:<br />
p∆V = R∆T<br />
Dieser Betrag ist eine Arbeit, die das Gas bei der Expansion leistet, sie muss<br />
aus der zugeführten Energie Q aufgebracht werden. Man stelle sich z.B. vor, dass<br />
das Gas bei der Erwärmung von T 1 auf T 2 das Volumen um ∆V vergrößert:<br />
p<br />
F<br />
∆V ∆l p∆V = A∆l<br />
= F∆l<br />
A<br />
Die Energiebilanz lautet also:<br />
Q =<br />
C<br />
P<br />
∆T<br />
C<br />
P<br />
=<br />
= C<br />
3<br />
2<br />
V<br />
R∆T<br />
+ R∆T<br />
+<br />
R<br />
=<br />
5<br />
2<br />
R<br />
also<br />
ist eine Arbeit, die der<br />
Kolben nach außen abgeben<br />
kann;<br />
5
Mit der Einführung der Ausdehnungsarbeit kann man jetzt den 1. Hauptsatz<br />
formulieren, man schreibt ihn differenziell bezogen auf eine kleine<br />
Wärmemenge dQ, die man von außen zuführt und die eine kleine Erhöhung<br />
der inneren Energie dU in Form einer Temperaturerhöhung bewirkt und<br />
zusätzlich eine Arbeit pdV leistet:<br />
= 1. Hauptsatz<br />
dQ dU +<br />
pdV<br />
Die Vorzeichenkonvention ist hier so, dass bedeutet:<br />
pdV > 0 : Arbeit nach außen abgegeben<br />
pdV<br />
< 0 :<br />
Arbeit von außen hereingebracht<br />
Bei <strong>Gase</strong>n gilt:<br />
V=konstant: p=konstant:<br />
dQ =<br />
dU = mcV<br />
dT<br />
dQ = dU + pdV = mcV<br />
dT +<br />
pdV<br />
6
Wärmekapazität realer <strong>Gase</strong><br />
Die obigen Ableitungen der molaren spezifische Wärme gelten exakt nur für<br />
einatomige <strong>Gase</strong>, bei <strong>mehratomige</strong>n <strong>Gase</strong>n aus Molekülen (z.B. O 2 oder N 2)<br />
ist die Situation etwas komplizierter:<br />
ideales Gas<br />
He<br />
Hg-Dampf<br />
H 2<br />
O 2<br />
CO 2<br />
NH 3<br />
C P (J/Mol K)<br />
20.78<br />
(5/2 R)<br />
20.95<br />
20.80<br />
28.83<br />
(7/2 R)<br />
29.39<br />
36.84<br />
4R<br />
36.80<br />
C V (J/Mol K)<br />
12.47<br />
(3/2 R)<br />
12.62<br />
12.46<br />
20.47<br />
(5/2 R)<br />
21.12<br />
28.49<br />
3R<br />
28.20<br />
C P -C V<br />
(J/MolK)<br />
8.31<br />
( R)<br />
8.34<br />
8.33<br />
8.38<br />
8.22<br />
8.35<br />
8.60<br />
1 atomig<br />
1-atomig<br />
1-atomig<br />
2-atomig<br />
2-atomig<br />
mehratomig<br />
mehratomig<br />
7
Es fällt auf, dass die für die idealen <strong>Gase</strong> abgeleiteten Beziehungen nur<br />
für einatomige <strong>Gase</strong> gelten, für <strong>mehratomige</strong> <strong>Gase</strong> gibt es systematische<br />
Abweichungen.<br />
Schauen wir uns noch einmal die Ableitung der kinetischen Energie eises<br />
Moleküls etwas genauer an. Das Molekül kann sich in 3 Richtungen bewegen,<br />
(x, y, z) zu jeder Richtung gehört eine mittlere kinetische Energie<br />
1<br />
mv x kBT<br />
2 2<br />
1 2 = zusammen also 3/2 k BT.<br />
Man sagt das das Molekül 3 Freiheitsgrade der Bewegung hat, zu jedem<br />
Freiheitsgrad gehört eine mittlere thermische Energie von 1/2k BT. Bezogen<br />
auf ein Mol gehört deshalb auch ein Beitrag von ½ R zur Wärmekapazität,<br />
zusammen also<br />
C V<br />
3<br />
= R mit der Zahl der Bewegungsfreiheitsgrade z=3<br />
2<br />
8
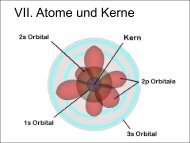
Bei komplizierteren Molekülen gibt es neben den Freiheitsgrades für die<br />
Translationsbewegung , noch Rotationsfreiheitsgrade, d.h. die Moleküle<br />
können thermische Energie auch in Form von Rotationen aufnehmen. Betrachten wir<br />
ein 2-atomiges Molekül (Hantel):<br />
x<br />
x<br />
z<br />
z<br />
y<br />
y<br />
Das Molekül kann Rotationen um die z-Achse<br />
und die x-Achse ausführen, hat also 2 Rotationsfreiheitsgrade<br />
zusätzlich. Die Rotationsenergie ist dabei<br />
1 2<br />
Erot<br />
= Θω<br />
2<br />
Die Drehung um die y-Achse (Längsachse) ist nicht<br />
möglich.<br />
Kompliziertere Moleküle mit drei oder<br />
mehr Atomen können dagegen um alle 3 Achsen rotieren<br />
und haben 3 Rotationsfreiheitsgrade zusätzlich<br />
9
Der Gleichverteilungssatz der sagt nun, dass im thermische Gleichgewicht<br />
jeder Bewegungsfreiheitsgrad des Moleküls im Mittel genau ½ k BT<br />
an thermischer Energie aufnimmt, dann erhält man für die Wärmekapazität<br />
die allgemeine Formel:<br />
C V<br />
=<br />
z<br />
2<br />
R<br />
einatomiges Gas: z=3 (3 Translationen)<br />
zweiatomiges Gas: z =5 (3 Translationen, 2 Rotationen)<br />
<strong>mehratomige</strong>s Gas: z= 6 (3 Translationen, 3 Rotationen)<br />
Das stimmt mit der Tabelle oben gut überein.<br />
Bei der Wärmekapazität von Festkörpern und Flüssigkeiten gibt es<br />
zunächst einmal eine Vereinfachung. Da die Volumenänderung mit der<br />
Temperatur klein ist, braucht man zwischen CP und CV nicht zu unter<br />
scheiden:<br />
≈ = für Festkörper.<br />
CV CV<br />
C<br />
10
Genau wie bei <strong>Gase</strong>n können die Atome im Festkörper thermische Energie in Form<br />
von Translationsbewegungen (kinetische Energie ) aufnehmen. Da die Atome im<br />
Festkörper elastische Schwingungen ausführen, gibt es auch noch eine potenzielle<br />
Energie, die im Mittel gleich der kinetischen Energie sein muss, also<br />
gilt für Festkörper aus einatomigen Molekülen:<br />
3 3<br />
C = R + R =<br />
2 2<br />
3R<br />
kin. Energie pot.Energie<br />
Experimentelle Beispiele: Experiment NaCl<br />
Au<br />
Pb<br />
Al 2 O 3<br />
SiO 2<br />
Benzol<br />
C 6 H 6<br />
C(J/Mol K)<br />
(300 K)<br />
25.4 (ca. 3R)<br />
26.8<br />
77.2<br />
44.6<br />
136<br />
Bei komplizierteren Molekülen<br />
kommen noch eine Reihe von<br />
internen Molekülschwingungen<br />
hinzu, die thermische Energie<br />
aufnehmen können.<br />
11