Energikonvertering ved Solid Oxide Electrolyser Cells
Energikonvertering ved Solid Oxide Electrolyser Cells
Energikonvertering ved Solid Oxide Electrolyser Cells
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
5.4. MODEL AF SOEC-ANLÆG<br />
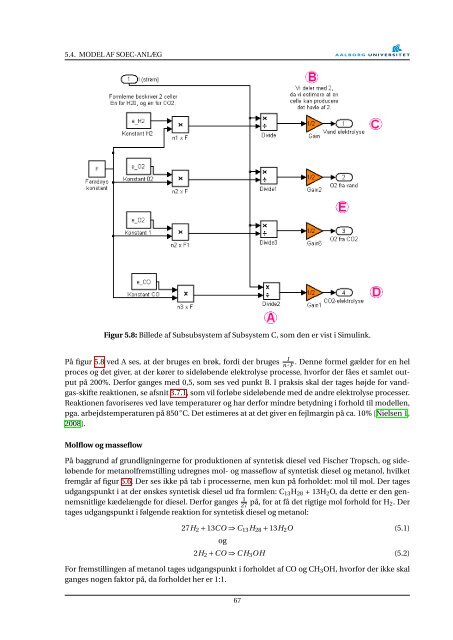
Figur 5.8: Billede af Subsubsystem af Subsystem C, som den er vist i Simulink.<br />
På figur 5.8 <strong>ved</strong> A ses, at der bruges en brøk, fordi der bruges n ·F . Denne formel gælder for en hel<br />
proces og det giver, at der kører to sideløbende elektrolyse processe, hvorfor der fåes et samlet output<br />
på 200%. Derfor ganges med 0,5, som ses <strong>ved</strong> punkt B. I praksis skal der tages højde for vandgas-skifte<br />
reaktionen, se afsnit 3.7.1, som vil forløbe sideløbende med de andre elektrolyse processer.<br />
Reaktionen favoriseres <strong>ved</strong> lave temperaturer og har derfor mindre betydning i forhold til modellen,<br />
pga. arbejdstemperaturen på 850 ◦C. Det estimeres at at det giver en fejlmargin på ca. 10% [Nielsen 1,<br />
2008].<br />
Molflow og masseflow<br />
På baggrund af grundligningerne for produktionen af syntetisk diesel <strong>ved</strong> Fischer Tropsch, og sideløbende<br />
for metanolfremstilling udregnes mol- og masseflow af syntetisk diesel og metanol, hvilket<br />
fremgår af figur 5.6. Der ses ikke på tab i processerne, men kun på forholdet: mol til mol. Der tages<br />
udgangspunkt i at der ønskes syntetisk diesel ud fra formlen: C13H28 + 13H2O, da dette er den gennemsnitlige<br />
kædelængde for diesel. Derfor ganges 1<br />
27 på, for at få det rigtige mol forhold for H2. Der<br />
tages udgangspunkt i følgende reaktion for syntetisk diesel og metanol:<br />
I<br />
27H2 + 13CO ⇒ C13H28 + 13H2O (5.1)<br />
og<br />
2H2 +CO ⇒ C H3OH (5.2)<br />
For fremstillingen af metanol tages udgangspunkt i forholdet af CO og CH3OH, hvorfor der ikke skal<br />
ganges nogen faktor på, da forholdet her er 1:1.<br />
67