2. Immunhistokemisk teknik - NordiQC
2. Immunhistokemisk teknik - NordiQC
2. Immunhistokemisk teknik - NordiQC
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>2.</strong> <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Af Ole Nielsen<br />
<strong>2.</strong>1 INDLEDNING ........................................................................................................... 11<br />
<strong>2.</strong>2 DEFINITIONER.......................................................................................................... 11<br />
<strong>2.</strong><strong>2.</strong>1 Antigener ....................................................................................................... 11<br />
<strong>2.</strong><strong>2.</strong>2 Antistoffer ...................................................................................................... 11<br />
<strong>2.</strong>3 PRÆPARATION: PARAFFINSNIT........................................................................................ 13<br />
<strong>2.</strong>3.1 Fiksering .......................................................................................................143<br />
<strong>2.</strong>3.2 Afkalkning ...................................................................................................... 14<br />
<strong>2.</strong>3.3 Vævsfremføring til paraffin ............................................................................... 15<br />
<strong>2.</strong>3.4 Skæring, montering, tørring og opbevaring af snit................................................ 15<br />
<strong>2.</strong>3.5 Afparaffinering og hydrering.............................................................................. 15<br />
<strong>2.</strong>4 PRÆPARATION: CYTOLOGISK MATERIALE OG FRYSESNIT............................................................ 16<br />
<strong>2.</strong>4.1 Fremstilling .................................................................................................... 16<br />
<strong>2.</strong>4.2 Tørring og opbevaring ...................................................................................... 16<br />
<strong>2.</strong>4.3 Fiksering ........................................................................................................ 17<br />
<strong>2.</strong>5 BLOKERING AF “ENDOGEN AKTIVITET” ............................................................................... 18<br />
<strong>2.</strong>5.1. Endogen enzymaktivitet ................................................................................... 18<br />
<strong>2.</strong>5.2 Endogen biotin ................................................................................................ 19<br />
<strong>2.</strong>6 EPITOP DEMASKERING (RETRIEVAL).................................................................................. 20<br />
<strong>2.</strong>6.1 Proteolytiske enzymer ...................................................................................... 20<br />
<strong>2.</strong>6.2 Varmeinduceret epitop demaskering (HIER) ........................................................ 21<br />
<strong>2.</strong>7 BLOKERING AF USPECIFIK ANTISTOFADHÆSION ..................................................................... 27<br />
<strong>2.</strong>8 PRIMÆRT ANTISTOF.................................................................................................... 28<br />
<strong>2.</strong>8.1 Valg af antistof................................................................................................ 28<br />
<strong>2.</strong>8.2 Afprøvning af antistoffer ................................................................................... 29<br />
<strong>2.</strong>8.3 Antistof-inkubation .......................................................................................... 30<br />
<strong>2.</strong>8.4 Antistoftiter, inkubationstid og temperatur .......................................................... 31<br />
<strong>2.</strong>8.5 Fortyndervæske .............................................................................................. 32<br />
<strong>2.</strong>8.6 Opbevaring og holdbarhed af antistoffer ............................................................. 32<br />
<strong>2.</strong>8.7 Kontrolprocedurer............................................................................................ 33<br />
<strong>2.</strong>9 SKYLLEPROCEDURE .................................................................................................... 33<br />
<strong>2.</strong>9.1 Skyllebuffer .................................................................................................... 34<br />
<strong>2.</strong>9.2 Skylletid......................................................................................................... 34<br />
<strong>2.</strong>10 DETEKTIONSSYSTEMER ............................................................................................. 34<br />
<strong>2.</strong>10.1 Direkte <strong>teknik</strong>ker............................................................................................. 34<br />
<strong>2.</strong>10.2 Indirekte <strong>teknik</strong>ker .......................................................................................... 35<br />
<strong>2.</strong>11 KROMOGEN/SUBSTRATOPLØSNING ................................................................................ 41<br />
<strong>2.</strong>11.1 Horse radish peroxidase ................................................................................... 41<br />
<strong>2.</strong>11.2 Alkalisk phosphatase........................................................................................ 42<br />
<strong>2.</strong>12 KERNEFARVNING .................................................................................................... 44<br />
<strong>2.</strong>13 REFERENCER......................................................................................................... 44<br />
Mogens Vyberg 2005
10 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
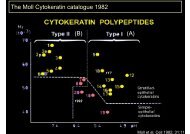
Figur <strong>2.</strong>1: Flowchart over metodologiske parametre i den immunhistokemiske <strong>teknik</strong>.<br />
Nedfrysning<br />
Skæring af snit<br />
Montering af snit<br />
Tørring af snit<br />
Opbevaring<br />
Fiksering<br />
Anvendte forkortelser<br />
Ab(s) antibody(-ies) (antistof(fer))<br />
AP alkaline phophatase<br />
CD cluster of differentiation<br />
CK cytokeratin<br />
ER estrogen receptor<br />
Materiale<br />
Væv Celler<br />
Fiksering<br />
Evt afkalkning<br />
Fremføring til<br />
paraffin<br />
Skæring af snit<br />
Montering af snit<br />
Tørring af snit<br />
Afparaffinering og<br />
hydrering<br />
Blokering af<br />
“endogen aktivitet”<br />
Epitop demaskering<br />
Blokering af<br />
“uspecifik adhæsion”<br />
Primært antistof<br />
Skylleprocedure<br />
Detektionssystem<br />
Kromogen/substratopl.<br />
Kernefarvning<br />
Montering af dækglas<br />
Cytospin, dup,<br />
smear m.v.<br />
Tørring<br />
Opbevaring<br />
Fiksering<br />
HRP horse radish (peberrod) peroxidase<br />
mAb monoclonal antibody<br />
pAb polyclonal antibody<br />
PBS phosphate buffered saline<br />
PgR progesteron receptor<br />
rmAb rabbit (kanin) mAb<br />
TBS tris buffered saline<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 11<br />
<strong>2.</strong>1 Indledning<br />
<strong>Immunhistokemisk</strong>e <strong>teknik</strong>ker er traditionelt<br />
“multi-step” <strong>teknik</strong>ker, hvor mange forskellige<br />
metodologiske parametre har betydning<br />
for det endelige resultat. I dette kapitel, der<br />
tager sit udgangspunkt i den praktiske immunhistokemi,<br />
som den udøves i diagnostisk<br />
sammenhæng, belyses de vigtigste parametres<br />
indflydelse på farvningsresultaterne. Der<br />
fokuseres specielt på immunenzymatiske<br />
<strong>teknik</strong>ker på paraffinsnit, frysesnit og cytologisk<br />
materiale.<br />
Gennemgangen af parametrene og deres<br />
betydning for farvningsresultatet følger “flowchartet”,<br />
Fig. <strong>2.</strong>1. Foruden den teoretiske<br />
gennemgang af de enkelte parametre anføres<br />
en række basale, praktiske præparations- og<br />
farvningsmæssige protokoller. Disse protokoller<br />
beskriver gennemprøvede, robuste og<br />
reproducerbare metoder.<br />
Teknikker, der anvendes til immunfluorescens,<br />
immunelektronmikroskopi og molekylærbiologiske<br />
undersøgelser, omtales ikke.<br />
<strong>2.</strong>2 Definitioner<br />
<strong>2.</strong><strong>2.</strong>1 Antigener<br />
Et antigen er et molekyle, der kan give anledning<br />
til dannelse af antistof ved injektion i<br />
et hvirveldyr. Langt de fleste antigener er<br />
proteiner eller proteinforbindelser, men kulhydrater<br />
og lipider kan også virke som antigener.<br />
Nogle kemiske substanser, fx metaller,<br />
er ikke i sig selv antigener, men kan i forbindelse<br />
med et protein danne en struktur, der<br />
udløser antistofdannelse. Sådanne substanser<br />
kaldes haptener. De antigene egenskaber<br />
ligger som regel i ét eller flere mindre områder<br />
af et molekyle. Disse områder kaldes<br />
antigene determinanter eller epitoper og består<br />
oftest af 4-8 aminosyrer eller monosaccharidenheder.<br />
En epitop kan bestå af en<br />
kontinuert sekvens af nabostillede aminosyrer<br />
i den primære proteinstruktur, eller af flere<br />
mindre aminosyresekvenser, der er bragt i<br />
tæt relation til hinanden gennem proteinmolekylets<br />
foldning (tertiære struktur). (Fig.<br />
<strong>2.</strong>2).<br />
Figur <strong>2.</strong>2: Model af antigen. De sorte områder repræsenterer<br />
antigene epitoper.<br />
Mogens Vyberg 2005<br />
<strong>2.</strong><strong>2.</strong>2 Antistoffer<br />
Antistoffer eller immunglobuliner (Ig) er glycoproteiner,<br />
der produceres i en organisme<br />
som reaktion på en antigenstimulation. Antistofferne<br />
binder sig med stor affinitet og specificitet<br />
til det stimulerende antigen. Antistoffer<br />
produceres i plasmaceller, der er transformerede<br />
B-lymfocytter, og afgives bl.a. til<br />
blodet, hvorfra de kan isoleres. I højere hvirveldyr<br />
findes fem klasser af immunglobuliner:<br />
IgA, IgD, IgE, IgG og IgM. Alle immunglobuliner<br />
er opbygget af tunge og lette proteinkæder.<br />
De fem immunglobulinklasser er bl.a.<br />
karakteriseret ved hver deres indhold af tunge<br />
kæder, α (alfa: IgA), δ (delta: IgD), ε<br />
(epsilon: IgE), γ (gamma: IgG) og µ (my:<br />
IgM). De lette kæder, der er fælles for alle<br />
immunglobulinklasser, kan enten være af<br />
type κ (kappa) eller λ (lambda).<br />
De fleste antistoffer, der anvendes til immunhistokemi,<br />
er af IgG-klassen, mens et mindre<br />
antal er af IgM-klassen. IgG-molekylet består<br />
af to tunge kæder (γ) og to lette kæder (κ<br />
eller λ) bundet sammen med disulfidbroer i<br />
en Y-formet struktur (Fig. <strong>2.</strong>3).<br />
På grundlag af antigene forskelle i de såkaldt<br />
konstante områder af de tunge kæder kan<br />
IgG-molekylerne yderligere inddeles i 4 subklasser:<br />
IgG1, IgG2a, IgG2b og IgG3. Med<br />
enzymerne papain og pepsin kan<br />
IgG-molekylet spaltes i flere komponenter.<br />
Papain spalter IgG i to antigen-bindende<br />
fragmenter benævnt fragment antibody (Fab)<br />
og ét fragment benævnt fragment crystalline<br />
eller fragment complement (Fc).<br />
Proteolytisk behandling med pepsin giver et<br />
F(ab’)2 fragment. Fc-fragmentet indeholder<br />
bl.a. bindingssteder for Protein A, complement<br />
og receptorer på makrofager og granulocytter.<br />
Den specifikke antigenbindende<br />
egenskab ligger i den terminale, såkaldt variable<br />
region af Fab.<br />
Figur <strong>2.</strong>3: Model af IgG molekyle. IgG er opbygget af<br />
2 tunge og 2 lette kæder forbundet ved hjælp af disulfidbindinger.<br />
Papain spalter IgG i 2 antigenbindende<br />
fragmenter betegnet Fab og 1 fragment crystalline<br />
benævnt Fc. Pepsin proteolyse giver et F(ab´)2 fragment.<br />
Pepsin<br />
Papain<br />
Fc<br />
Fab<br />
F(ab’) 2
12 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Den variable region indeholder den specielle<br />
aminosyresekvens og rummelige opbygning,<br />
der er komplementær til den epitop på antigenet,<br />
som det pågældende antistofmolekyle<br />
er rejst imod. Rummeligt passer epitop til<br />
antistof som “en nøgle til en lås”. Bindingen<br />
mellem antistof og epitop er en non-covalent<br />
binding, der oftest er en blanding af elektrostatiske<br />
kræfter, hydrogenbindinger, van der<br />
Waalske kræfter og hydrofob interaktion.<br />
Reaktionen mellem antigen og antistof er<br />
reversibel og kan beskrives som:<br />
Ag + Ab ‹―› AgAb kompleks<br />
Ligevægtskonstanten K er herefter defineret<br />
som:<br />
[AbAg] −1<br />
K = M<br />
[Ab]x[Ag]<br />
hvor [Ab] er den molære koncentration af frie<br />
antistofmolekyler, [Ag] er den molære koncentration<br />
af frit antigen, og [AbAg] den molære<br />
koncentration af antistof-antigen komplekser.<br />
Antistoffers bindingsstyrke til antigen<br />
betegnes affinitet. For antistoffer med høj<br />
affinitet er ligevægtskonstanten i størrelsesorden<br />
10 10 til 10 12 . For antistoffer med lav<br />
affinitet ligger ligevægtskonstanten nede<br />
omkring 10 5 . I immunhistokemisk sammenhæng<br />
giver antistoffer med høj affinitet naturligvis<br />
de bedste resultater, bl.a. fordi de i<br />
højere grad er i stand til at forblive bundet til<br />
antigen gennem hele proceduren.<br />
Polyklonale antistoffer<br />
Polyklonale antistoffer (pAbs) er blandinger af<br />
antistoffer fra forskellige kloner. De produceres<br />
ved at immunisere et dyr (kanin, svin,<br />
ged eller lignende) med et oprenset antigen.<br />
Dyret vil rejse et immunrespons, og de producerede<br />
antistoffer kan høstes gennem gentagende<br />
tapninger af blod og efterfølgende<br />
isolering af serum. I dyret vil der oftest opformeres<br />
mange kloner af plasmaceller (polyklonalt<br />
respons), der hver for sig producerer<br />
antistofmolekyler rettet mod én af epitoperne<br />
i antigenet (Fig. <strong>2.</strong>4).<br />
Der vil således til en hver af antigenets epitoper<br />
kunne produceres mange forskellige antistoffer,<br />
der varierer mere eller mindre med<br />
hensyn til affinitet og specificitet.<br />
Blandt disse mange forskellige antistoffer kan<br />
forekomme nogle, der krydsreagerer med<br />
epitoper på andre molekyler, end det antigen,<br />
Figur <strong>2.</strong>4: Polyklonalt antistof (A) og monoklonalt<br />
antistof (B) rettet mod det samme antigen<br />
de er rejst imod. Sådanne krydsreagerende<br />
antistoffer bør fjernes fra antisera ved hjælp<br />
af absorption med det krydsreagerende molekyle.<br />
Kun de færreste kommercielle antistoffer<br />
findes tilgængelige i fuldserumformat.<br />
Risikoen for at det store indhold af<br />
serumproteiner vil give problemer med baggrundsfarvning<br />
er for stor. I stedet sælges de<br />
som en oprenset immunglobulinfraktion. Immunglobulinfraktionen<br />
vil foruden de specifikke<br />
antistoffer også indeholde dyrets “normale”<br />
cirkulerende immunglobuliner. Yderligere<br />
oprensning af antistof kan foretages<br />
ved hjælp af affinitetskromatografi, hvor man<br />
på en antigenkoblet kromatografisøjle kan<br />
isolere de specifikke antistoffer.<br />
Da pAbs består af mange forskellige antistofmolekyler<br />
rettet mod mange forskellige<br />
epitoper på det samme antigen, kan affinitetsbegrebet<br />
ikke direkte anvendes. For disse<br />
beskrives bindingsstyrken ved udtrykket aviditet.<br />
Aviditeten er populært sagt en slags<br />
“affinitetsmiddelværdi” for de forskellige antistoffer,<br />
der indgår i det polyklonale antiserum.<br />
Monoklonale antistoffer<br />
Monoklonale antistoffer (mAbs) er antistoffer,<br />
der alle stammer fra samme celleklon. I modsætning<br />
til et pAb vil mAb udelukkende bestå<br />
af fuldkommen ens antistofmolekyler rettet<br />
mod én og samme epitop på antigenet (Fig.<br />
<strong>2.</strong>4).<br />
mAbs produceres ved hjælp af Köhler og Milstein’s<br />
hybridom<strong>teknik</strong> (1). Teknikken, der<br />
går ud på at fusionere immuniserede<br />
B-lymfocytter med myelomceller, er beskrevet<br />
i detaljer af Gatter et al. (2). Produktionen<br />
af mAbs sker i sin oprindelige form ved,<br />
at en mus immuniseres med antigen, der ikke<br />
nødvendigvis er fuldstændig rent, hvorefter<br />
lymfocytterne isoleres fra milten på den immuniserede<br />
mus. Disse lymfocytter, der naturligt<br />
har en begrænset levetid, fusioneres<br />
derefter med myelomceller, der er maligne og<br />
i principet udødelige celler, og som er blevet<br />
valgt, fordi de har mistet evnen til at producere<br />
og secernere immunglobuliner.<br />
Ved fusionen mellem de to celletyper opstår<br />
der en cellehybrid, der kan secernere immunglobuliner,<br />
hvis specificitet er bestemt af musens<br />
lymfocytter, og som har myelomcellernes<br />
egenskaber med hensyn til neoplastisk<br />
proliferation. Hybridomcellerne klones og<br />
undersøges for antistofproduktion. De antistofproducerende<br />
kloner undersøges herefter<br />
med henblik på at finde dem, der producerer<br />
antistof rettet mod det immuniserende antigen.<br />
De pågældende antistoffer undersøges<br />
dernæst i flere testsystemer, her iblandt immunhistokemi,<br />
for at fastslå forhold omkring<br />
affinitet, specificitet og eventuel krydsreaktivitet<br />
for antistoffet. Når interessante kloner<br />
er identificeret, kan yderligere opformering<br />
foretages. Opformeringen foregår ofte i store<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 13<br />
cellekulturer, hvor antistoffet høstes som<br />
supernatant fra store dyrkningsflasker. En<br />
alternativ måde til opformering er den såkaldte<br />
“ascites produktion”, hvor hybridomceller<br />
sprøjtes ind i peritonealhulen på mus,<br />
hvor der udvikles en antistofproducerende<br />
tumor. Antistoffet høstes ved at tappe ascitesvæske<br />
af musen. Navngivning af mAbs<br />
foregår normalt ved at angive antigenets<br />
navn efterfulgt af en tal- eller bogstavkode,<br />
der refererer til den antistofproducerende<br />
celleklon (fx anti-ERα, klon 1D5).<br />
Kommercielt tilgængelige kanin mAbs<br />
(rmAbs) så først for alvor dagens lys i 2003,<br />
hvor NeoMarker i samarbejde med Epitomics<br />
lancerede en stribe rmAbs, der fungerer glimrende<br />
på paraffinsnit. Blandt de bedste i den<br />
serie kan nævnes anti- cyclin-D1, klon SP4;<br />
anti-ERα, klon SP1; anti-PgR, klon SP2; anti-<br />
Ki67, klon SP6; og anti-COX2, klon SP21.<br />
Andre SP-antistoffer fungerer dog mindre<br />
godt, og et enkelt er trukket tilbage fra markedet.<br />
Produktionen af rmAbs foregår efter<br />
samme princip som for muse mAbs. Når der<br />
tidligere ikke fandtes kommercielt tilgængelige<br />
rmAbs, skyldes det bl.a. problemer med at<br />
finde en passende fusionspartner (myelomcelle)<br />
til kaninlymfocytter, d.v.s. en fusionspartner,<br />
der kunne skabe en stabil hybridomcellekultur<br />
med høj antistofproduktion. Dette<br />
problem og andre produktionstekniske problemer<br />
er nu løst. Da rmAbs byder på fordele<br />
som fx højere affinitet end muse mAbs, vil<br />
fremtiden helt sikkert bringe mange nye<br />
rmAbs på markedet.<br />
<strong>2.</strong>3 Præparation: paraffinsnit<br />
Paraffinsnit fremstilles sædvanligvis ud fra<br />
histologisk materiale. Der er dog tiltagende<br />
interesse for, med henblik på immunhistokemiske<br />
undersøgelser, også at fremstille paraffinsnit<br />
ud fra cytologisk materiale (se afsnit<br />
<strong>2.</strong>4.1).<br />
<strong>2.</strong>3.1 Fiksering<br />
En essentiel del af al histologisk og cytologisk<br />
<strong>teknik</strong> er fikseringen. Ved fiksering forstås<br />
normalt en kemisk behandling, der har til<br />
formål at immobilisere og stabilisere vævets<br />
og cellernes bestanddele. I immunhistokemisk<br />
sammenhæng skal et fiksativ ideelt<br />
kunne:<br />
1. Immobilisere antigener.<br />
<strong>2.</strong> Bevare antigenisitet.<br />
3. Bevare vævs- og cellestruktur.<br />
4. Bevare permeabiliteten for immunreagenser<br />
(antistoffer mv.).<br />
Naturligvis findes det ideelle immunhistokemiske<br />
fiksativ ikke. Specielt kravet om bevarelse<br />
af antigenisitet vil ofte komme i konflikt<br />
med kravene om bevarelse af struktur og<br />
immobilisering af antigener. Med antigenisitet<br />
forstås sædvanligvis tilstedeværelsen af antistofbindende<br />
aktivitet. Da bindingen mellem<br />
antistof og epitop er stærkt afhængig af epi-<br />
Mogens Vyberg 2005<br />
topens rumlige struktur, vil antigenisiteten<br />
næsten altid være under indflydelse af den<br />
kemiske påvirkning, som et hvert fiksativ vil<br />
udøve på antigener. Fiksativer kan inddeles i<br />
2 hovedgrupper:<br />
1. Koagulerende fiksativer<br />
(“non-cross-linking” fiksativer).<br />
<strong>2.</strong> Gelerende fiksativer (“cross-linking” fiksativer).<br />
Koagulerende fiksativer<br />
Til de koagulerende fiksativer hører bl.a. etanol,<br />
metanol, picrinsyre og acetone. Ved den<br />
koagulerende fiksering åbnes proteinernes<br />
tertiære struktur og hydrofobe grupper samt<br />
reaktive grupper blotlægges. Disse blotlagte<br />
grupper vil herefter kunne reagere med<br />
grupper i andre proteinmolekyler under etablering<br />
af større uordnede aggregater (Fig.<br />
<strong>2.</strong>5). På trods af den vidtgående strukturelle<br />
modifikation af antigenerne er antigenisiteten<br />
forbavsende velbevaret for ganske mange<br />
antigeners vedkommende. En af årsagerne til<br />
dette er, at såvel den primære som den sekundære<br />
struktur af antigenerne ikke påvirkes.<br />
Koagulerende fiksativer er således meget<br />
velegnet til fiksering af fx intermediære<br />
filamenter som CK og vimentin. Den morfologiske<br />
bevarelse af væv fikseret i rene koagulerende<br />
fiksativer er dog ikke den bedste.<br />
Samtidig er der en risiko for, at antigener<br />
med en lav molekylvægt vil ekstraheres under<br />
fikseringen. Dette er de væsentligste<br />
årsager til, at koagulerende fiksativer sjældent<br />
bruges rutinemæssigt til fiksering med<br />
henblik på paraffinindlejring. I den forbindelse<br />
er det vigtigt at bemærke, at etanol dehydrering<br />
vil virke som en “koagulerende efterfiksering”<br />
på væv, der kun er fikseret kort tid<br />
i formaldehyd. <strong>Immunhistokemisk</strong>e metoder<br />
optimeret til formalinfikseret væv kan ikke<br />
uden videre anvendes til undersøgelser på<br />
væv fikseret i koagulerende fiksativ. Antigener,<br />
der ikke er fikseret tilstrækkeligt i formalin,<br />
vil blive helt eller delvis fikseret i alkohol<br />
under vævspræparering med risiko for at<br />
blive ekstraheret (fx S-100 protein).<br />
Figur <strong>2.</strong>5: Gelerende og koagulerende fiksativer. Efter<br />
Lyon (3).<br />
Koagulerende<br />
fiksering<br />
Polypeptidkæde<br />
Hydrofobe aminosyreradikaler<br />
Nativt protein<br />
Gelerende fiksering<br />
Hydrofile aminosyreradikaler<br />
Tværbindinger
14 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Gelerende fiksativer<br />
Gelerende fiksativer virker bl.a. ved at etablere<br />
tværbindinger mellem visse aminosyreradikaler<br />
i proteinerne (antigenerne) (Fig.<br />
<strong>2.</strong>5). Foruden at give en glimrende bevarelse<br />
af vævsmorfologien er tværbindingerne med<br />
til at stabilisere antigenerne i en nativ eller<br />
kun svagt modificeret konformation, således<br />
at de ikke koagulerer under den efterfølgende<br />
dehydrering. På trods af en stabilisering i<br />
stort set nativ konformation, påvirkes antigenisiteten<br />
for mange antigener negativt af<br />
gelerende fiksering. Blandt de gelerende fiksativer<br />
er 4% neutral buffet formaldehyd<br />
(NBF) klart det foretrukne fiksativ i diagnostisk<br />
rutinesammenhæng. Formaldehyd menes<br />
at påvirke antigenisiteten på flere måder:<br />
1. Maskering af epitoper.<br />
a. gennem konformative ændringer i antigenet.<br />
b. gennem immobilisation af nabomakromolekyler<br />
(sterisk hindring).<br />
c. gennem compleksbinding af metalioner,<br />
især Ca-ioner<br />
<strong>2.</strong> Kemisk modifikation af reaktive aminosyrer<br />
i epitopen.<br />
3. Ekstraktion af antigener under fikseringen<br />
eller den efterfølgende præparation.<br />
Da fiksering påvirker antigenisiteten, bør<br />
fikseringstiden så vidt mulig standardiseres.<br />
Fikseringstider på 24 - 48 timer i NBF giver<br />
generelt de bedste resultater. Ved for kort<br />
fikseringstid er der som nævnt ovenfor risiko<br />
for, at en del af epitoperne i virkeligheden<br />
bliver alkoholfikserede, hvilket markant kan<br />
ændre betingelserne for immunhistokemisk<br />
påvisning.<br />
Marzo et al. (87) viste i et studie på prostatektomier,<br />
at antallet af p27KIP1 positive<br />
epitelceller i prostata falder, hvis fikseringstiden<br />
i NBF nedsættes. Fikseringstider under 1<br />
døgn gav væsentlig svagere reaktioner end<br />
fikseringstider på 2 døgn eller mere. Antip27<br />
KIP1 , klon 57 fungerer bedst på væv fikseret<br />
mellem 2 og 7 døgn i NBF (87).<br />
Ved for lang fikseringstid ses en tiltagende<br />
maskering af mange epitoper. Da formaldehydbindingen<br />
er delvis reversibel, er det muligt<br />
at rette op på en del af problemerne vedrørende<br />
bevarelse af antigenisitet. Langvarigt<br />
skyl (dage!) i vand efter fiksering af rehydrerede<br />
paraffinsnit kan løse en del af problemerne<br />
vedrørende maskering og kemisk modifikation<br />
af epitoper, men vil sjældent være<br />
relevant på grund af muligheden for epitopdemaskering<br />
(afsn. <strong>2.</strong>6).<br />
<strong>2.</strong>3.2 Afkalkning<br />
Væv, der indeholder større mængder calciumsalte,<br />
fx knoglemateriale, kræver normalt<br />
en afkalkning, for at brugbare paraffinsnit<br />
kan produceres. I praksis benyttes mange<br />
forskellige afkalkningsmedier, som hver for<br />
sig kan påvirke antigenisiteten i vævet.<br />
Afkalkningsmedier kan inddeles i 4 hovedgrupper:<br />
1. Stærke, uorganiske syrer, fx HCl og HNO3 <strong>2.</strong> Kommercielle blandinger indeholdende<br />
bl.a. stærke syrer, fx Decal, New Decal,<br />
RBD, S/P, RDO mv.<br />
3. Svage, organiske syrer, fx myresyre og<br />
eddikesyre<br />
4. Kompleksbindere, fx EDTA.<br />
De stærke syrer og de kommercielle blandingsprodukter<br />
udmærker sig ved at afkalke<br />
vævet hurtigt. De kan dog ikke ubetinget<br />
anbefales til materiale, der efterfølgende skal<br />
anvendes til immunhistokemi. Bruges således<br />
Decal (Histolab, Västra Frölunda) til afkalkning<br />
(4-6h) på NBF fikseret væv, tabes antigenisitet<br />
helt eller delvist for de fleste antigener<br />
(4). Andre kommercielle blandingsprodukter<br />
har vist sig mere anvendelige. Arber<br />
et al. (57) fandt med RBD (Rapid Bone Decal,<br />
USA) og S/P Decal (USA) som afkalkningsmedier<br />
tilfredsstillende resultater med 52 ud<br />
af 57 antistoffer.<br />
Desværre sås med vigtige antistoffer (som<br />
anti-epithelial antigen, Ber-EP4; anti-p53,<br />
klon DO7; anti-ERα, klon 1D5; anti-PgR, klon<br />
ICA; anti-elastase, klon NP57; og anti-Ki67,<br />
klon MIB1) i visse tilfælde svage eller negative<br />
reaktioner sammenlignet med ikke-afkalkede<br />
kontrolpræparater. I samme<br />
undersøgelse farvede alle 57 antistoffer svarende<br />
til eller kraftigere end kontolpræparaterne,<br />
hvis EDTA-baseret afkalkning blev<br />
anvendt. Dette understreger EDTA’s egenskab<br />
som skånsomt afkalkningsmedium.<br />
Ulempen er blot, at afkalkning i EDTA er meget<br />
langsom. Det kan selv for mindre biopsier<br />
være nødvendigt at afkalke i op til flere dage.<br />
Et godt alternativ til både de stærke syrer og<br />
EDTA er derfor de svage organiske syrer.<br />
Specielt gode resultater er opnået med myresyre<br />
(10% myresyre eller Kristensens opløsning,<br />
der er 4 M med hensyn til myresyre og<br />
0,5 M med hensyn til Na-formiat), der afkalker<br />
en hel del hurtigere end EDTA. Knoglebiopsier<br />
kan således afkalkes på 3-6 timer i<br />
Kristensens opløsning. Herefter kan der produceres<br />
paraffinsnit af høj kvalitet, med mulighed<br />
for at påvise de fleste antigener, der<br />
normalt overlever NBF-fiksering og paraffinindlejring.<br />
En forudsætning for de gode resultater<br />
er selvfølgelig, at vævet er fikseret ordentligt<br />
inden afkalkningen påbegyndes. Med<br />
hensyn til bevarelse af antigenisitet afkalker<br />
Kristensens opløsning generelt ligeså skånsomt<br />
som EDTA - også hvad angår nucleære<br />
antigener som p53, Ki67, ERα og PgR (4).<br />
Der ses dog undtagelser. Anti-CD79a, klon<br />
JCB117 giver således efter afkalkning i myresyre<br />
en noget svagere reaktion, end hvad der<br />
opnås efter EDTA afkalkning, mens antielastase,<br />
klon NP57 slet ikke tåler syreafkalkning<br />
(hverken stærke syrer eller myresyre).<br />
Klon NP57 kan således kun anvendes, hvis<br />
afkalkningen foretages i EDTA (4).<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 15<br />
<strong>2.</strong>3.3 Vævsfremføring til paraffin<br />
Forholdsvis få studier har beskæftiget sig<br />
med betydningen af forskellige dehydrerings-,<br />
klarings- og paraffinindlejringsmedier i<br />
forbindelse med immunhistokemiske farvninger.<br />
Meget tyder imidlertid på, at “vævsfremføringen”<br />
i et vist omfang bidrager til maskeringen<br />
af antigene epitoper i paraffinsnit.<br />
Antigener som Ki67 og terminal deoxynucleotidyl<br />
transferase (TdT), der lader sig påvise<br />
umiddelbart i både kryosnit og cytologisk<br />
materiale selv efter 6-24 timers fiksering i<br />
NBF, lader sig ikke uden forudgående demaskering<br />
påvise i paraffinsnit af væv fikseret<br />
den samme tid i NBF. Vævsfremføringens<br />
bidrag til epitopmaskering er på den anden<br />
side konstant og ret uafhængig af, hvilke<br />
dehydrerings- og klaringsmedier (og for den<br />
sags skyld paraffintyper), der anvendes<br />
(4,5,56). Det, der synes vigtigst for bevarelsen<br />
af antigenisiteten, er, at vævet dehydreres<br />
fuldstændigt og at paraffininfiltreringen er<br />
komplet. Forkortelse af tiden til dehydrering<br />
og paraffinindfiltrering har således for visse<br />
antistoffer (fx anti-CD20, klon L26) betydet<br />
nedsat reaktivitet.<br />
<strong>2.</strong>3.4 Skæring, montering, tørring og<br />
opbevaring af snit<br />
Paraffinsnit bør skæres 3-5 µm tykke, strækkes<br />
fuldkommen på varmt vandbad (ca.<br />
45°C) og monteres på glas coatede med fx<br />
poly-L-lysin eller silane, eller på elektrostatisk<br />
behandlede glas som fx SuperFrost®Plus.<br />
Anvendelse af forbehandlede objektglas nedsætter<br />
drastisk risikoen for at miste snit undervejs<br />
i farvningsproceduren. Efter montering<br />
skal snittene tørres, hvorved bindingen<br />
til glasset forstærkes. De fleste epitoper tåler<br />
tørring ved 60°C i 1 time. En mere skånsom<br />
tørring opnås ved 37°C natten over (56),<br />
eventuelt efterfulgt af 60°C i 1 time. Enkelte<br />
antigener (epitoper) er meget varmefølsomme,<br />
det gælder fx proliferating cell nuclear<br />
antigen (PCNA) Ønsker man således at påvise<br />
PCNA i paraffinsnit med fx antistoffet klon<br />
PC10, opnås klart de bedste resultater ved at<br />
tørre snittene natten over ved stuetemperatur.<br />
Velfikseret og velpræpareret materiale indstøbt<br />
i paraffin synes at bevare antigenisiteten<br />
af formalinresistente epitoper godt. Der<br />
er dog undtagelser. Dash et al. (58) har vist,<br />
at androgenreceptor immunreaktiviteten aftager<br />
med tiden i paraffinblokke. Med anvendelse<br />
af mAb F39.4.1 på 9 prostatakarcinomer<br />
registredes ved hjælp af billedanalyse<br />
et tab af immunreaktivitet i paraffinblokkene<br />
svarende til ca. 40% over en<br />
periode på 22 mdr. På trods af disse fund er<br />
den generelle holdning stadig, at antigenisiteten<br />
bevares godt i paraffinblokke, hvad talrige<br />
retrospektive studier baseret på materialer<br />
op til 30-40 år gamle også viser.<br />
Mogens Vyberg 2005<br />
Til gengæld er antigenisiteten i skårne og<br />
glasmonterede paraffinsnit ikke nær så holdbar<br />
som i intakte paraffinblokke. Mange nyere<br />
studier (6,7,59,60,61,62,79,80,81) har vist,<br />
at flere antigener taber antigenisitet som<br />
funktion af snittenes alder og opbevaringstemperatur.<br />
Der har i de forskellige studier<br />
været nogen forskel på, hvilke antigener man<br />
har fundet følsomme. Følgende diagnostisk<br />
vigtige antistoffer har alle i et eller flere studier<br />
vist et varierende tab af reaktivitet i<br />
gamle snit sammenlignet med nye snit af de<br />
samme blokke: Anti-ERα, klon 1D5 og 6F11;<br />
anti-anaplastic lymphoma kinase, klon ALK-1;<br />
anti-cyclin D1, klon P2D11F11; anti-terminal<br />
deoxynucleotidyl transferase, pAb; anti-p53,<br />
klon DO7 og PAb1801; anti-bcl2, klon 124;<br />
anti-chromogranin A, klon LK2H10; anti-factor<br />
VIII, pAb; anti-CD3, pAb; anti-cerbB-2,<br />
klon 3B5; anti-E-cadherin, klon<br />
HECD-1; anti-vimentin, klon V9; anti-<br />
CD45R0, klon UCHL-1; anti-epidermal growth<br />
factor receptor, klon EGFR.113; anti-retinoblastom<br />
gen protein, klon G3-245; anti-<br />
ACTH, pAb og anti-Ki67, klon MIB1.<br />
Årsagen til fænomenet er ukendt, men da<br />
tabet af reaktivitet for nogle antigener (fx<br />
p53 og ERα) ses allerede efter få ugers opbevaring<br />
(59,60,61), er det et problem, der<br />
specielt i store retrospektive studier må tages<br />
højde for. Flere studier har vist (62,79,81), at<br />
tabet af antigenisitet er størst, hvis snittene<br />
opbevares ved stuetemperatur eller højere.<br />
Opbevaret ved 4ºC er tabet væsentlig mindre,<br />
og ved -80ºC ses der intet tab efter 3<br />
års opbevaring (62). Med vekslende held er<br />
tabet af antigenisitet forsøgt restaureret gennem<br />
forstærket epitop retrieval (forlænget<br />
kogetid i HIER-buffer eller brug af alternative<br />
buffere, se afsn. <strong>2.</strong>6.2) eller opvejet ved at<br />
bruge primære antistoffer i højere koncentrationer.<br />
Som en konsekvens af ovenstående må det<br />
anbefales, at paraffinsnit, der skal opbevares<br />
mere end 14 dage, før de skal anvendes (fx<br />
positive kontrolsnit og snit til videnskabelige<br />
studier), som minimum bliver opbevaret ved<br />
4ºC eller endnu bedre ved -20ºC eller -80ºC,<br />
og at man ved hjælp af sammenligning med<br />
friskskårne snit registrerer omfanget af et<br />
evt. tab i antigenisitet.<br />
<strong>2.</strong>3.5 Afparaffinering og hydrering<br />
Som for enhver anden farvemetode er en<br />
komplet fjernelse af paraffin og dernæst afparaffineringsmediet<br />
(xylen, Estisol eller lignende)<br />
og rehydreringsmediet (etanol) vitale<br />
elementer i den immunhistokemiske <strong>teknik</strong>.<br />
De fleste laboratoriers standard afparaffinerings-<br />
og rehydreringsprocedure vil oftest<br />
direkte kunne overføres til immunfarvningerne.
16 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
<strong>2.</strong>4 Præparation: cytologisk<br />
materiale og frysesnit<br />
<strong>2.</strong>4.1 Fremstilling<br />
Cytologiske præparater<br />
En vigtig forudsætning for succes med immuncytokemiske<br />
<strong>teknik</strong>ker er optimal præparering<br />
af materialet. For cytologiske materialer<br />
(smears, cytospin-, monolayer- og duppræparater)<br />
er det vigtigt, at der anvendes<br />
coatede eller elektrostatisk behandlede objektglas,<br />
at cellerne så vidt muligt findes<br />
jævnt fordelt på objektglasset, og at cellerne<br />
er så velbevarede og intakte som muligt.<br />
Disse krav er ikke forskellige fra de præparationsmæssige<br />
krav, der stilles til almindelige<br />
cytologiske farvemetoder som May-Grünwald/Giemsa<br />
og Papanicoulaus. Dog er det<br />
med immuncytokemiske <strong>teknik</strong>ker endnu<br />
vigtigere at anvende præparater, hvor cellerne<br />
ligger i ét lag og ikke for tæt. I celletætte<br />
cytologiske materialer vil der ofte opstå problemer<br />
med “trapping” og uspecifik adhæsion<br />
af antistofferne med baggrundsfarvning til<br />
følge.<br />
Mange problemer med cytologiske præparater<br />
kan løses ved at fremstille celleblokke i<br />
form af formalinfikserede, paraffinindstøbte<br />
centrifugater eller sedimentater, der kan<br />
håndteres som almindeligt histologisk materiale<br />
(jfr. afsnit <strong>2.</strong>3).<br />
Protokol for fremstilling af celleblokke<br />
1. Den ufikserede celleholdige væske centrifugeres<br />
10 min. ved 3000 omdr./min, og supernatanten<br />
hældes fra.<br />
<strong>2.</strong> Bundfaldet tilsættes humant plasma (3 dråber<br />
til ca. ½ ml bundfald). Plasma og bundfald<br />
blandes ved hjælp af pipetten.<br />
3. Der tilsættes bovint trombin* (2 dråber til 3<br />
dråber plasma). Hvis ikke opløsningen koagulerer<br />
inden for ét minut, tilsættes yderligere én<br />
dråbe trombin (gentages efter behov). Herefter<br />
tilsættes neutral buffet formalin, og materialet<br />
føres efter en fikseringstid på 24 h frem til paraffin.<br />
*Bovine Thrombin (Biofac A/S), 1 ampul à 10.000<br />
units opløses i 100 ml 0,9% NaCl. Væsken fordeles<br />
i kryorør og nedfryses ved -20º C.<br />
Frysesnit<br />
Frysesnit skæres normalt 4-6 µm tykke og<br />
monteres på coatede eller eletrostatisk behandlede<br />
glas. Som ved alle undersøgelser på<br />
frysesnit er det vigtigt, at vævet nedfryses<br />
hurtigt, så fryseartefakter undgås. Nedfrysning<br />
i isopentan ved -79ºC giver gode resultater<br />
(3). Det er ligeledes vigtigt, at skæring<br />
foregår ved den temperatur, der er optimal<br />
for den pågældende vævstype (oftest mellem<br />
-12ºC og -18ºC). Efter skæring på cryostat<br />
optøs vævsblokken som regel for at gennemgå<br />
normal fikserings- og præparationsprocedure<br />
mhp fremstilling af paraffinsnit til supplerende<br />
histokemiske evt. immunhistokemiske<br />
analyser.<br />
Ønskes paraffinsnit af tidligere nedfrosset<br />
materiale anvendt til immunhistokemi, bør<br />
fortolkning af farvningsresultaterne foretages<br />
med forsigtighed. Reaktiviteten af en del<br />
antigener har vist sig at være svækket i paraffinsnit<br />
af tidligere nedfrosset væv, i forhold<br />
til hvad den er i paraffinsnit af ikke tidligere<br />
frosset materiale fra samme patienter. Egerton<br />
et al. (82) fandt flere eksempler på betydelig<br />
svækkelse af reaktiviteten på tidligere<br />
nedfrosset materiale når antistoffer mod S-<br />
100, synaptophysin, neuron specific enolase,<br />
carcinoembryonic antigen, chromogranin og<br />
melanosoma specific antigen (HMB45) anvendtes.<br />
Lignende fund er gjort i eget laboratorium<br />
I en række lymfomer er cyclin D1<br />
reaktiviteten set svækket, mens spørgsmålet<br />
om klonalitet i B-lymfomer gennem påvisning<br />
af kappa og lambda kæder i flere tilfælde ikke<br />
kunne besvares, når vævet tidligere havde<br />
været nedfrosset.<br />
CryoJane <strong>teknik</strong><br />
Med introduktionen af ”sentinel node (SN)<br />
proceduren” indenfor operation af mammakancer<br />
og malignt melanom er antallet af<br />
frysesnit på lymfeknuder steget betydeligt på<br />
mange patologiske instituter. Lymfeknuder er<br />
i sig selv ikke vanskellige at producere gode<br />
frysesnit af. Er det lymfatiske væv infiltreret<br />
med store mængde fedtceller, som kan være<br />
tilfældet med SN, er historien dog en ganske<br />
anden. Lymfatisk væv og fedtvæv har meget<br />
forskellige skæreegenskaber, hvilket vanskeliggør<br />
tilfredsstillende snitkvalitet. Til at afhjælpe<br />
disse problemer har en såkaldt ”tape<br />
transfer” <strong>teknik</strong> ved navn ”CryoJane” vist sig<br />
brugbar. Ved hjælp af en speciel tape, der<br />
understøtter vævet under skæring, overføres<br />
snit til specielle objektglas. Disse er coatede<br />
med en UV-sensitiv lim. Efter UV belysning<br />
kan tapen fjernes, efterladende et intakt frysesnit<br />
af høj teknisk kvalitet. CryoJane snit<br />
kan anvendes til HE farvning, div. histokemiske<br />
<strong>teknik</strong>ker og immunhistokemi (evt<br />
Haste-EnVision, se afsnit <strong>2.</strong>10.2). CryoJane<br />
systemet markedsføres af firmaet Instrumedics<br />
(www.instrumedics.com).<br />
<strong>2.</strong>4.2 Tørring og opbevaring<br />
Efter fremstilling af cytologiske præparater og<br />
frysesnit er det i de fleste tilfælde hensigtsmæssigt<br />
at tørre vævet/cellerne på objektglasset.<br />
Tørring inden evt. fiksering (se afsn.<br />
<strong>2.</strong>4.3) er med til at bevare morfologien uden<br />
nævneværdigt tab af antigenisitet. Tørretiden<br />
vil typisk være mellem 1 time og natten over.<br />
Tørringen kan evt. foregå under ventilator<br />
eller lignende. Efter endt tørring er materialet<br />
klar til evt. fiksering og efterfølgende immuncytokemi.<br />
Skal materialet ikke immunfarves<br />
umiddelbart efter tørring, bør opbevaringsformen<br />
overvejes. Opbevaret ukritisk ved<br />
stuetemperatur vil de fleste antigener blive<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 17<br />
tiltagende vanskelige at påvise (sammenlign<br />
afsn. <strong>2.</strong>3.4). For mange antigeners vedkommende<br />
ses der efter 3 dages opbevaring ved<br />
stuetemperatur ingen eller kun marginal<br />
svækkelse af antigenisiteten. For andre antigeners<br />
vedkommende er der allerede efter 3<br />
dages opbevaring set en betydelig svækkelse<br />
af reaktionen. Det drejer sig bl.a. om myosin<br />
af slow og fast type påvist med flere forskellige<br />
kommercielle mAbs (4). Den sikreste<br />
måde at opbevare sine cytologiske materialer<br />
og frysesnit - med henblik på senere immuncytokemi<br />
- er derfor at pakke de tørrede<br />
præparater i stanniol og nedfryse dem. Ved<br />
-18°C vil antigenisiteten bevares i måneder.<br />
Ved -80°C og derunder bevares antigenisiteten<br />
sædvanligvis i årevis. Når de tørrede og<br />
frosne præparater tages ud af fryseren til<br />
immunfarvning, er det vigtigt, at de ikke<br />
pakkes ud af stanniolen, før de har opnået<br />
stuetemperatur. Udpakning af kolde præparater<br />
vil medføre kondensdannelse på materialet,<br />
hvilket kan forringe den cytologiske kvalitet.<br />
<strong>2.</strong>4.3 Fiksering<br />
I modsætning til paraffinsnit har man med<br />
cytologiske materialer og frysesnit alle muligheder<br />
for at optimere fikseringsproceduren<br />
med henblik på optimal bevarelse af netop de<br />
antigener (epitoper) materialet skal undersøges<br />
for. Når der bortses fra epitoper, der<br />
dårligt tåler fiksering (se nedenfor) er der en<br />
lang række forskellige fiksativer til rådighed i<br />
forskellige immunhistokemiske sammenhænge.<br />
Ofte vil det være nødvendigt med en<br />
efterfølgende epitopdemaskering (se afsn.<br />
<strong>2.</strong>6). Blandt de vigtigste fiksativer er:<br />
1. Acetone, 100%<br />
<strong>2.</strong> Acetone/metanol (forhold 1:1)<br />
3. Acetone/metanol/formaldehyd (forhold<br />
19:19:2)<br />
4. Neutral buffet formaldehyd (NBF). 4%<br />
5. Neutral buffet formaldehyd (NBF). 4%,<br />
efterfulgt af detergentbehandling<br />
6. Neutral buffet formaldehyd (NBF) 4%,<br />
efterfulgt af epitopdemaskering (se afsn.<br />
<strong>2.</strong>6)<br />
7. Zambonis fiksativ.<br />
Acetone<br />
Acetone er et “rent” koagulerende fiksativ.<br />
Fiksering af frysesnit i 10 min. (cytologisk<br />
materiale behøver kun fiksering i 90 sek.)<br />
ved stuetemperatur eller ved 4°C bevarer<br />
antigenisiteten udmærket for de fleste antigener.<br />
Acetonefiksering er derfor af mange<br />
det foretrukne til frysesnit og cytologisk materiale,<br />
når det fx drejer sig om påvisning af<br />
overfladeantigener. En ulempe er, at morfologien<br />
ikke altid er optimalt bevaret.<br />
Mogens Vyberg 2005<br />
Der er desuden en række antistoffer, hvortil<br />
acetone ikke kan anvendes som fiksativ.<br />
Blandt disse er følgende diagnostisk vigtige<br />
antistoffer: anti-ERα (mange forskellige kloner);<br />
anti-PgR (mange forskellige kloner);<br />
anti-p53 (mange forskellige kloner); anti-terminal<br />
deoxynucleotidyl transferase<br />
(TdT)(såvel mAbs som pAbs); anti-Ki67, klon<br />
MIB1; anti-PCNA, klon PC10; og anti-C-erbB2,<br />
pAb. For nogle af disse antistoffers<br />
vedkommende er problemet øjensynligt,<br />
at antigenet helt eller delvist ekstraheres i<br />
acetone eller de efterfølgende procedurer.<br />
Acetone/metanol<br />
Acetone/metanol (1:1) er en blanding af koagulerende<br />
fiksativer. Fiksering 30-90 sek<br />
giver en rimelig skånsom fiksering, som kan<br />
anbefales til hæmatologisk materiale i kombination<br />
med en forstærket (repeteret, se nedenfor)<br />
alkalisk phosphatase anti-alkalisk<br />
phosphatase (APAAP)-<strong>teknik</strong>. Acetone/metanol<br />
giver i sammenligning med ren<br />
acetonefiksering en langt bedre cytologisk<br />
bevarelse af cellerne. En væsentlig ulempe<br />
ved acetone/metanol fiksering er, at reaktiviteten<br />
for en del epitopers vedkommende<br />
svækkes i forhold til fiksering alene med acetone.<br />
Svækkelsen af reaktionen kan delvis<br />
kompenseres ved hjælp af et meget følsomt<br />
detektionssystem, fx APAAP med forstærkning.<br />
Der er epitoper, der ikke lader sig påvise<br />
efter acetone/metanol fiksering. Indenfor<br />
hæmatologien kan bl.a. følgende mAbs således<br />
ikke anvendes på acetone/metanol-fik<br />
seret materiale: anti-CD10, klon SS2/36;<br />
anti-CD16, klon VIFcRIII; anti-CD13, klon<br />
My7; anti-CD33, klon VM54; anti-CD103, Ber<br />
ACT8; anti-hairy cell leukemia, klon DBA.44;<br />
og anti-glycophorin A, klon D2-10-<strong>2.</strong><br />
Acetone/metanol/formaldehyd<br />
Acetone/metanol/formaldehyd (19:19:2)<br />
giver en kombineret koagulerende og gelerende<br />
fiksering. Fiksering i 30-90 sek. giver<br />
yderligere forbedringer af den cytologiske<br />
bevarelse i forhold til acetone/metanol fiksering.<br />
Ulempen er, at der samtidig ses en<br />
yderligere svækkelse af immunreaktiviteten<br />
for en del epitopers vedkommende.<br />
Neutral buffet formalin (NBF)<br />
NBF (4%) giver en ren gelerende fiksering.<br />
Fiksering i 2-30 min. giver noget nær optimal<br />
morfologisk bevarelse på frysesnit, samtidig<br />
med at NBF er et fremragende fiksativ til<br />
specielt mange kernelokaliserede og intracytoplasmatiske<br />
antigener. På frysesnit opnås<br />
gode resultater med NBF, også for antigener,<br />
der ikke umiddelbart kan påvises på paraffinsnit.<br />
Dette fænomen er en understregning af,<br />
at ikke kun NBF-fikseringen bidrager til problemer<br />
med tab af antigenisitet i paraffinsnit.
18 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Dehydrerings-, klarings-, og paraffininfiltreringsproceduren<br />
må ligeledes forventes<br />
at bidrage i et vist omfang til maskeringen<br />
af epitoper.<br />
Blandt de mange antigener, hvortil der med<br />
fordel anvendes NBF-fiksering, kan nævnes:<br />
S-100 protein, p53 oncoprotein, C-erbB2<br />
oncoprotein, TdT, ERα og PgR og Ki67 antigen.<br />
Anvendes NBF til fiksering af cytologisk materiale,<br />
vil det i de fleste tilfælde være nødvendigt<br />
at foretage en form for permeabilisering<br />
af cellemembraner inden den immunhistokemiske<br />
farvning. Permeabilisering kan udføres<br />
på flere måder. Det letteste er at efterbehandle<br />
de NBF-fikserede celler med et detergent<br />
(sæbelignende stof)<br />
Protokol for kombineret NBF fiksering og<br />
permeabilisering<br />
1. Fiksering i 4% NBF 15 min.<br />
<strong>2.</strong> Skyl i buffer 2 min.<br />
3. Triton-X-100 (0,05%-0,5% i TBS) 10 min.<br />
4.Skyl i buffer og fortsæt med immunfarvning.<br />
Detergentbehandlingen ekstraherer dele af<br />
lipidmaterialet i cellens membraner, hvilket<br />
gør det lettere for immunreagenserne at penetrere<br />
dem. Effekten af detergentbehandling<br />
på cytologisk materiale vil tydeligt kunne<br />
iagttages ved påvisning af fx p53 oncoprotein<br />
og andre kernerelaterede antigener som TdT,<br />
Ki67 og lignende. Specielt for p53’s vedkommende<br />
giver NBF-fiksering efterfulgt af Triton-X-100<br />
behandling en voldsom forstærkning<br />
af reaktionen sammenlignet med den<br />
“rene” NBF-fiksering.<br />
NBF og varmeinduceret epitopdemaskering<br />
(HIER)<br />
Mange antistoffer giver på cytologisk materiale<br />
fremragende resultater, hvis fiksering i 4%<br />
NBF kombineres med HIER (se afsn. <strong>2.</strong>6.2<br />
inkl. afsn. vedr. HIER protokoller).<br />
Zambonis fiksativ<br />
Zambonis Fiksativ er et blandingsfiksativ<br />
bestående af: 2 g paraformaldehyd i 85 ml<br />
0,15 M fosfatbuffer pH 7,3 tilsat 15 ml vandig<br />
mættet picrinsyre. Fiksativet giver en kombineret<br />
gelerende og koagulerende fiksering.<br />
Det er bl. a. anbefalet ved undersøgelser for<br />
Retinoblastom (RB) gen protein. Flere forskellige<br />
anti-RB mAbs (klon G3-245, R128 og<br />
RB1), giver efter Zamboni-fiksering de bedste<br />
resultater. Tilsvarende er fiksativet anbefalet<br />
ved brug af anti-ERα (klon LH1 og LH2) og<br />
anti-PgR (klon 1A6).<br />
Ingen fiksering<br />
Især inden for muskelpatologien findes en<br />
række antigener, der bedst påvises uden<br />
nogen form for fiksering. Det drejer sig primært<br />
om proteiner med en relativ høj molekylvægt<br />
og/eller med en vis strukturel forankring<br />
i muskelcellens cytoplasma eller cellemembran.<br />
Påvisningen af slow myosin, klon<br />
WBMHCS; fast myosin, klon My32; dystrophin,<br />
klon Dy86C5; og en række<br />
dystrophinrelaterede antigener foregår derfor<br />
i praksis ved at applicere det primære antistof<br />
på de tørre frysesnit uden nogen forudgående<br />
behandling (fiksering eller lignende).<br />
Det skal dog tilføjes, at de fleste af disse<br />
antigener ikke desto mindre kan påvises i<br />
formalinfikserede muskelbiopsier med udmærkede<br />
resultater.<br />
<strong>2.</strong>5 Blokering af “endogen<br />
aktivitet”<br />
<strong>2.</strong>5.1. Endogen enzymaktivitet<br />
De vigtigste immunenzymatiske detektionssystemer<br />
benytter sig af peroxidase, alkalisk<br />
phosphatase, glukose oxidase eller betagalactosidase<br />
som enzymlabel (markør)<br />
Blandt disse enzymer er peroxidase og alkalisk<br />
phosphatase klart de foretrukne. I lighed<br />
med beta-galactosidase forekommer begge<br />
enzymer naturligt (endogent) i en række<br />
celler i humant væv. Det kan derfor være<br />
nødvendigt at blokere eller hæmme den endogene<br />
enzymaktivitet.<br />
Peroxidase (PO)<br />
PO-aktivitet forekommer med varierede styrke<br />
i granulocytter, monocytter og makrofager.<br />
Desuden indeholder erytrocytter såkaldt<br />
pseudoperoxidaseaktivitet, der giver de<br />
samme fortolkningsmæssige problemer. I<br />
paraffinsnit af NBF fikseret materiale er<br />
egentlig peroxidaseaktivitet stort set elimineret,<br />
mens pseudoperoxidaseaktiviteten i<br />
erytrocytter “overlever”.<br />
En lang række forskellige kemiske forbehandlinger<br />
vil være i stand til at blokere den endogene<br />
peroxidaseaktivitet:<br />
Protokoller til blokering af endogen peroxidase<br />
aktivitet<br />
1. 0,5% brintperoxid i metanol<br />
eller<br />
10 min.<br />
<strong>2.</strong> 1% - 3% brintperoxid i TBS<br />
eller<br />
10 min.<br />
3. 0,5% - 3% brintperoxid i etanol<br />
eller<br />
10 min.<br />
4. 0,3% brintperoxid og 0,1% Na-azid i TBS 10 min.<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 19<br />
Alle 4 protokoller kan anbefales til blokering<br />
af endogen peroxidaseaktivitet på<br />
NBF-fikserede paraffinsnit. Protokol 1 og 3<br />
skal altid appliceres før evt. demaskering,<br />
mens protokol 2 og 4 kan appliceres enten<br />
før demaskering eller efter primært antistof<br />
(men før HRP-link!). Ingen af de 4 protokoller<br />
bør anvendes lige efter demaskering, da<br />
mange epitoper er følsomme overfor både<br />
metanol/etanol og brintperoxid. Til gengæld<br />
tyder meget på, at langt de fleste NBFfikserede<br />
epitoper, der ”overlever” fiksering,<br />
vævspræparation og paraffinindlejring, også<br />
klarer en forbehandling med henblik på blokering<br />
af endogen peroxidaseaktivitet, hvis<br />
denne foretages før evt. demaskering. Desværre<br />
er der undtagelser. Anti-CD4, klon 1F6<br />
reagerer med en epitop, der er meget følsom<br />
overfor brintperoxid, også selvom blokeringen<br />
foregår før demaskering. På paraffinsnit, hvor<br />
dette antistof skal anvendes, bør blokering<br />
derfor udelades eller foretages efter det primære<br />
antistof.<br />
På cytologiske materialer og frysesnit er epitoper<br />
generelt mere følsomme overfor kemiske<br />
påvirkninger, end de er i paraffinsnit af<br />
NBF fikserede væv. En del laboratorier undlader<br />
derfor at blokere for endogent peroxidaseaktivitet<br />
i disse materialer. I de fleste tilfælde<br />
lader det sig gøre uden problemer, da<br />
det bl.a. med hjælp fra et negativt kontrolsnit<br />
er muligt at identificere den endogene peroxidaseaktivitet.<br />
I hæmatologisk materiale og<br />
cytologisk materiale med kraftig blodtilblanding,<br />
hvor der kan forudses fortolkningsproblemer<br />
på grund af endogen peroxidaseaktivitet,<br />
kan protokol 4 anbefales. Li et al. (8)<br />
fandt, at der med denne protokol kunne opnås<br />
en effektiv blokering af endogen peroxidaseaktivitet<br />
uden tab af antigenisitet eller<br />
morfologiske detaljer. Undersøgelsen blev<br />
udført med 23 forskellige diagnostisk vigtige<br />
antistoffer inden for hæmatologien. Tilsvarende<br />
gode eller bedre resultater er opnået<br />
ved først at applicere protokol 4 efter det<br />
biotinylerede sekundære antistof i en labelled<br />
streptavidin biotin (LSAB) eller ABC <strong>teknik</strong><br />
(9).<br />
For epitoper der tåler NBF fiksering kan der<br />
være en elegant alternativ løsning på problemet<br />
med endogen peroxidaseaktivitet. På<br />
cryostatsnit og mange cytologisk materialer<br />
vil en kombination af NBF fiksering og en<br />
varmebehandling ved over 95°C i HIER-buffer<br />
blokere effektivt for endogen peroxidaseaktivitet<br />
(se afsn. <strong>2.</strong>6.2 ”NBF-HIER protokoller”<br />
og <strong>2.</strong>10.2 ”Protokol Haste-EnVision+”). I<br />
kombination med NBF fiksering ses således 2<br />
positive effekter af varmebehandling: Dels en<br />
forstærkning af immunreaktionen gennem<br />
demaskering (se afsn. <strong>2.</strong>6.2) og dels en blokering<br />
af endogen enzymaktivitet.<br />
En simpel løsning på problemer med endogen<br />
peroxidaseaktivitet er selvfølgelig at anvende<br />
et detektionssystem, der er baseret på alkalisk<br />
phosphatase som enzym-label (fx APAAP,<br />
se afsnit <strong>2.</strong>10.2).<br />
Mogens Vyberg 2005<br />
Alkalisk phosphatase<br />
Alkalisk phosphatase (AP) aktivitet forekommer<br />
akkurat som PO naturligt i en række<br />
celler i humant væv. AP kan klassificeres i<br />
mindst 5 grupper, alt efter hvilket væv de<br />
stammer fra (10). Den AP, der anvendes til<br />
enzymkonjugater, udvindes fra kalvetyndtarm.<br />
AP i tarm er resistent overfor enzymhæmmeren<br />
levamisol, mens AP i lever og<br />
knoglemarv er følsom for levamisol. Tilsætning<br />
af 1 mM levamisol til kromogen/substratopløsningen<br />
vil derfor effektivt blokere<br />
endogen AP aktivitet relateret til disse celler<br />
og væv, mens enzymlabel ikke påvirkes. Dette<br />
gør AP-baserede detektionsystemer (fx<br />
APAAP) meget anvendelige til hæmatologiske<br />
materialer. Undersøgelser (11) har dog vist,<br />
at tilsætning af 1 mM levamisol i visse detektionssystemer.<br />
(LSAB-AP) kan have en vis<br />
hæmmende effekt på enzymlabel. Afhængig<br />
af graden af endogen AP anbefales det således<br />
at bruge lavere koncentrationer af levamisol<br />
(0,25 mM - 0,5 mM), der ikke har vist<br />
hæmmende effekt på AP-label. Alternativt<br />
kan snittene opvarmes til 65ºC, hvorved APaktiviteten<br />
elimineres.<br />
AP-baserede detektionssystemer har deres<br />
begrænsninger specielt på materiale fra mave-tarmkanalen<br />
og placenta, da levamisol<br />
ikke hæmmer den endogene AP i disse væv.<br />
Der kan også i visse tilfælde ses levamisolresistent<br />
AP i tumorer. I et cytologisk studie af<br />
25 non-hæmopoietiske tumorer fandes levamisolresistent<br />
AP i 4 tilfælde (10), der ikke<br />
udgik fra ventrikel/tarm eller placenta.<br />
<strong>2.</strong>5.2 Endogen biotin<br />
Avidin-biotin og steptavidin-biotin detektionssystemer<br />
(ABC, LSAB mv., se afsn. <strong>2.</strong>10)<br />
benytter sig af den naturlige affinitet, avidin<br />
og steptavidin har for biotin (vitamin H). Biotin<br />
forekommer i store mængder sammen<br />
med enzymet pyruvat carboxylase i mitochondrier.<br />
Det betyder, at der i mitochondrie-rige<br />
celler er risiko for falsk positiv<br />
reaktion svarende til streptavidins eller avidins<br />
reaktion med endogen biotin. Artefaktet<br />
ses specielt i metabolisk aktive celler som fx<br />
lever, nyre, binyre, spytkirtler mv. En del<br />
karcinomer, heriblandt mamma- og colonkarcinomer<br />
vil potentielt også kunne give anledning<br />
til denne falske positive reaktion. Sædvanligvis<br />
forekommer endogen biotin intracytoplasmatisk,<br />
men kan også ses intranucleært.<br />
I graviditetsrelateret endometrium<br />
er der således i 32 af 69 prøver set biotinholdige<br />
intranucleære inklusioner (12), der selvfølgelige<br />
ikke må forveksles med virus inklusioner<br />
(fx herpes simplex). Problemet med<br />
endogen biotin er naturligvis kun relateret til<br />
de biotinbaserede detektionssystemer og har<br />
tidligere kun været et reelt problem på cytologisk<br />
materiale og kryostatsnit. I paraffinsnit<br />
maskeres det meste biotin nemlig effektivt og<br />
gav således sjældent problemer med falsk
20 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Figur <strong>2.</strong>6: Blokering af endogen biotin.<br />
positiv reaktion i ikke-demaskerede snit. Med<br />
introduktionen af varmeinduceret epitopdemaskering<br />
(se afsn. <strong>2.</strong>6) er problemet vokset,<br />
og specielt efter den tiltagende brug af<br />
mere effektive kogemedier som EDTA/EGTA<br />
og Tris-HCl ved højt pH er problemet blevet<br />
påtrængende. Giver endogen biotin fortolkningsmæssige<br />
problemer, bør der enten vælges<br />
alternativt detektionssystem (fx APAAP<br />
eller et af de mange polymersystemer - se<br />
afsn. <strong>2.</strong>10.2) eller en forbehandling med blokering<br />
af endogen biotin for øje (Fig. <strong>2.</strong>6).<br />
Protokol til blokering af endogen biotin<br />
1. Avidin 0,1% 10 min.<br />
<strong>2.</strong> PBS eller TBS 2 min.<br />
3. Biotin 0,01% 10 min.<br />
4. PBS eller TBS 2 min.<br />
Blokeringen iværksættes umiddelbart før<br />
blokering af uspecifik antistofadhæsion, hvilket<br />
for paraffinsnit selvfølgelig betyder, at<br />
biotinblokeringen udføres efter evt. epitop<br />
demaskering.<br />
Protokollen (evt. udført med kit) giver i de<br />
fleste tilfælde en tilfredsstillende blokering af<br />
biotin i paraffinsnit og frysesnit. Udover den<br />
ekstra håndtering af glassene er også prisen<br />
en væsentlig ulempe ved denne protokol.<br />
Anvendes kommercielle kits, er prisen generelt<br />
høj: blokering ved hjælp af DakoCytomations<br />
kit koster således 4,69 kr. pr. glas og<br />
Vectors kit koster 3,31 kr. Zymeds kit koster<br />
“kun” 2,16 kr. pr. glas, men er ikke helt så<br />
effektivt til at blokere endogent biotin som de<br />
to øvrige (4).<br />
Det er ikke væsentlig billigere at købe de<br />
rene varer selv, da rent avidin er forbavsende<br />
kostbart. Miller et al. (63) har beskrevet et<br />
simpelt og brugbart alternativ til de dyre kits.<br />
I stedet for at bruge ren avidin kan man an-<br />
vende fortyndede æggehvider, der indeholder<br />
store mængder avidin. Prisen bringes hermed<br />
ned på 10 øre pr. glas. Da de fortyndede<br />
æggehvider og biotinopløsningen (0,2% i<br />
PBS) tilmed er holdbare og kan genbruges<br />
(æggehvider 1 uge, biotin 1 måned), kan<br />
hele proceduren foregå i farveskåle uden<br />
krævende håndtering af de enkelte glas.<br />
Millers protokol til blokering af endogen biotin<br />
1. Skyl i dest vand 5 min.<br />
<strong>2.</strong> Fortyndede æggehvider (2 æggehvider,<br />
fyld op til 200 ml med dest vand) 15 min.<br />
3. Grundigt skyl i flere hold dest vand 5 min.<br />
4. Biotin (Merck No. 500030) 0,2% i PBS,<br />
pH 7,2 med 15mM natriumazid 15 min.<br />
5. PBS eller TBS 2 min.<br />
Ved kontakt med buffersalte er der risiko for,<br />
at æggehvide-protein vil udfælde i snittene,<br />
hvorfor der skal skylles grundigt i destilleret<br />
vand.<br />
<strong>2.</strong>6 Epitop demaskering<br />
(retrieval)<br />
I paraffinsnit af NBF-fikseret materiale vil<br />
mange antigene epitoper ikke eller kun dårligt<br />
kunne påvises. Det har vist sig, at en stor<br />
del af disse epitoper ikke er ødelagte, men<br />
blot er maskerede. Mange maskerede epitoper<br />
kan demaskeres og dermed gøres “immunreaktive”<br />
igen. De to vigtigste, principielt<br />
forskellige <strong>teknik</strong>ker, der i dag bruges til demaskering<br />
af antigene epitoper er:<br />
1. Forbehandling med proteolytiske enzymer.<br />
<strong>2.</strong> Varmeinduceret epitop demaskering (HIER<br />
= heat-induced epitop retrieval).<br />
Hertil kommer andre metoder, der er nødvendige<br />
til specielle antigener, fx behandling<br />
med 100% myresyre til amyloider, samt diverse<br />
kombinationer af proteolyse og HIER<br />
(se tabel <strong>2.</strong>2)<br />
Ultralyd har ligeledes været anvendt til epitop<br />
retrieval. For enkelte antigener synes ultralyd<br />
at have en vis demaskerende effekt, men dog<br />
væsentlig mindre effekt end HIER (86). Som<br />
generel demaskerings<strong>teknik</strong> synes ultralyd<br />
derfor uinteressant.<br />
<strong>2.</strong>6.1 Proteolytiske enzymer<br />
Anvendelsen af proteolytiske enzymer til demaskering<br />
af antigene epitoper blev introduceret<br />
i 70’erne (13,14) og har siden vundet<br />
stor udbredelse. Teknikken gjorde det muligt<br />
at påvise et stort antal antigener, der tidligere<br />
var vanskelige eller umulige at påvise i<br />
paraffinsnit af NBF fikseret materiale. Mange<br />
forskellige enzymer kan anvendes. Trypsin,<br />
pepsin eller pronase E er de mest populære.<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 21<br />
Protokoller til proteolytisk forbehandling<br />
a. Trypsin protokol:<br />
Trypsin 250, Difco 0152-13 0,050 g<br />
Tris-buffer 0,05M, pH 7,8 med<br />
0,1% CaCl2 37° 50 ml<br />
Afhængig af fikseringstiden i NBF forbehandles<br />
5-20 min. ved 37°C. Inden inkubation i enzymopløsning<br />
forvarmes snittene 5 min. i destilleret vand<br />
ved 37°C.<br />
b. Pepsin protokol:<br />
Pepsin, Sigma No. P7012 0,160 g<br />
HCl, 0,01 M 37°C 40 ml<br />
Afhængig af fikseringstiden i NBF forbehandles<br />
10-120 min. ved 37°C. Inden inkubation i enzymopløsning<br />
forvarmes snittene 5 min. i destilleret<br />
vand ved 37° C.<br />
c. Pronase E (Protease type 14) protokol:<br />
Protease type XIV,Sigma No. P5147 0,025 g<br />
TBS 0,05M, pH 7,4 37°C 50 ml<br />
Afhængig af fikseringstiden i NBF forbehandles<br />
5-15 min. ved 37°C. Inden inkubation i enzymopløsning<br />
forvarmes snittene 5 min. i destilleret<br />
vand ved 37°C.<br />
d. Proteinase K protokol*:<br />
Proteinase K, DakoCytomation S3004 40 µl<br />
Tris-buffer 0,05M, pH 7,5 stuetemp. 50 ml<br />
Afhængig af fikseringstiden i NBF forbehandles<br />
5-15 min. ved stuetemperatur. Denne protokol kan<br />
med fordel appliceres immunostainere som Tech-<br />
Mate og Autostainer.<br />
*Proteinase K opløsningen kan købes klar til brug.<br />
Biokemisk er enzymernes reaktivitet og specificitet<br />
velkendt. Trypsin katalyserer således<br />
spaltningen af peptidbindinger i hvilke aminosyrerne<br />
arginin og lysin forekommer. Chymotrypsin,<br />
som findes i de fleste kommercielle<br />
trypsinprodukter, hydrolyserer navnligt<br />
peptidbindinger, hvor de aromatiske aminosyrers<br />
carboxylsyrer indgår. Pepsin angriber<br />
en del forskellige peptidbindinger, men peptidbindinger,<br />
hvor de aromatiske aminosyrers<br />
aminogrupper indgår, spaltes hurtigst. Pronase<br />
E, der udvindes fra Streptomyces griseus,<br />
er som de fleste andre bakterielle proteaser<br />
meget lidt specifik med hensyn til hvilke peptidbindinger,<br />
der angribes. Pronase E er således<br />
i stand til at katalysere spaltningen af<br />
størstedelen af de typer peptidbindinger, der<br />
forekommer i humant væv. Tilsvarende gælder<br />
proteinase K.<br />
Er enzymernes biokemiske reaktivitet og<br />
specificitet velkendt, så er baggrunden for<br />
deres demaskerende effekt i immunhistokemisk<br />
sammenhæng til gengæld noget uklar.<br />
Den positive effekt på muligheden for at påvise<br />
maskerede epitoper beror givet vis på<br />
flere faktorer. Blandt de vigtigste er:<br />
1. Evnen til spaltning af peptidbindinger i<br />
umiddelbar nærhed af de NBF-inducerede<br />
Mogens Vyberg 2005<br />
tværbindinger (methenbroer). Dette er<br />
med til at åbne op for en del af de “skjulte”<br />
epitoper. En direkte spaltning af<br />
methenbroerne synes mindre sandsynligt.<br />
<strong>2.</strong> Fraspaltning af blokerende nabomolekyler.<br />
3. Permeabiliteten af vævet øges gennem<br />
spaltningen af proteinerne.<br />
Selvom trypsin, pepsin og pronase biokemisk<br />
er forskellige med hensyn til hvilke peptidbindinger<br />
de spalter i proteinerne, vil der i mange<br />
tilfælde kun ses mindre forskelle i deres<br />
evne til at demaskere en given epitop. I de<br />
fleste tilfælde er pronasen dog mest effektiv,<br />
hvilket forklarer dette enzyms popularitet.<br />
Pepsin har vist sig særlig velegnet til demaskering<br />
af epitoper i extracellulære strukturproteiner<br />
som collagen III, collagen IV, fibronectin,<br />
laminin og P-component. De gode<br />
resultater opnås specielt, hvis inkubationen i<br />
pepsin forlænges til 1-2 timer. Pronase E er<br />
især velegnet anti-LMW-CK, klon CAM 5.2, og<br />
anti-CD21, klon 1F8.<br />
Udover den positive effekt er der også væsentlige<br />
ulemper forbundet med forbehandlingen<br />
med proteolytiske enzymer. For<br />
det første er der en hel del epitoper, der ikke<br />
tåler enzymforbehandling, hvilket naturligvis<br />
udelukker <strong>teknik</strong>ken som universel demaskerings<strong>teknik</strong>.<br />
For det andet er der alvorlige<br />
problemer med standardisering af metoden.<br />
Problemerne stammer væsentligst fra det<br />
faktum, at inkubationstiden for den proteolytiske<br />
forbehandling er stærkt afhængig af<br />
fikseringstiden i NBF. Alle undersøgelser viser,<br />
at jo længere tids fiksering der er anvendt<br />
i NBF, jo længere tids proteolytisk forbehandling<br />
skal iværksættes for at opnå den<br />
ønskede epitop-demaskering. Omvendt skal<br />
enzymforbehandlingstiden nedsættes for<br />
væv, der kun er fikseret i kort tid i NBF. For<br />
lang tids enzymforbehandling i forhold til fikseringstiden<br />
vil give en gradvis “fordøjelse” af<br />
vævssnittet med tab af morfologiske detaljer<br />
til følge. For at optimere den enzymatiske<br />
forbehandling er det med andre ord nødvendigt<br />
at kende fikseringstiden på det væv,<br />
man ønsker at behandle. Standardisering af<br />
den proteolytiske forbehandling kompliceres<br />
yderligere ved, at den optimale proteolysetid<br />
også kan variere fra celletype til celletype.<br />
For keratinpåvisning i forskellige epiteltyper<br />
er således beskrevet en betydelig tidsvariation<br />
for optimal proteolysetid (15). Endelig<br />
skal det nævnes, at falsk positiv reaktion kan<br />
ses ved anvendelse af anti-CK20, klon<br />
Ks20.8, hvis der anvendes proteolytisk forbehandling,<br />
specielt hvis vævet kun er kortvarigt<br />
fikseret (
22 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
skering (Heat-Induced Epitop Retrieval -<br />
HIER). Teknikken har på dramatisk vis forbedret<br />
mulighederne for immunhistokemi på<br />
paraffinsnit. HIER åbner mulighed for at anvende<br />
antistoffer på paraffinsnit, som tidligere<br />
med konventionel <strong>teknik</strong> (proteolyse mv.)<br />
kun gav svagt positiv reaktion eller slet ingen<br />
(20-23,76). Blandt de vigtigste antistoffer i<br />
denne gruppe, der omfatter mere end 40,<br />
kan nævnes: anti-Ki67, klon MIB1; anti-ERα,<br />
klon 1D5; anti-PgR, klon ICA og 1A6; anti-bcl-2,<br />
klon 124; anti-CD5, klon 4C7; anti-CD8,<br />
klon C8/144B; anti-CD 23, klon 1B12;<br />
anti-CD44, klon DF1485; anti-CD44v6, klon<br />
2F10; anti-CD79a, klon JCB117; anti-RB, klon<br />
G3-245; anti-CD4, klon 1F6; anti-E-Cadherin,<br />
klon HECD-1; anti-TdT, pAb; anti-dystrophin,<br />
klon Dy4; og anti-Cyclin D1, klon DSC-6,<br />
P2D11F11 og SP4 samt pAb fra Biocare.<br />
Der findes en endnu større gruppe antistoffer,<br />
omfattende 50-80% af de på patologiafdelinger<br />
anvendte, som før introduktionen af HIER<br />
gav åbenlyst svagere reaktioner på paraffinsnit<br />
end frysesnit. Efter HIER kan der nu for<br />
denne store gruppe antistoffer opnås resultater<br />
på paraffinsnit, der med hensyn til farvningsintensitet<br />
og detektionsgrænser modsvarer,<br />
hvad der optimalt kan opnås på frysesnit.<br />
Til denne gruppe hører mange antistoffer<br />
mod bl.a. CK’er og CD-markører (fx anti-CD3,<br />
anti-CD20, antiCD30, anti-CD45,<br />
anti-CD54 og anti-CD68) samt de fleste p53<br />
antistoffer.<br />
HIER-<strong>teknik</strong>ken bygger på opvarmning af<br />
afparaffinerede og rehydrerede paraffinsnit i<br />
passende buffer eller saltopløsning. Shi’s<br />
originale metode benyttede sig af mikrobølgeovn<br />
(MBO) som varmekilde og af en mættet<br />
blythiocyanatopløsning eller rent destilleret<br />
vand som “kogemedium”. Siden Shi’s<br />
originale arbejde er talrige modifikationer<br />
blevet publiceret. Cattoretti et al (20) introducerede<br />
i 1993 citratbuffer 0,01 M, pH 6,<br />
som kogemedium. Citratbuffer har siden været<br />
det mest benyttede kogemedium i HIER<br />
<strong>teknik</strong>ken, men afløses nu i tiltagende omfang<br />
af alternative buffere (se nedenfor).<br />
Den præcise mekanisme bag HIER <strong>teknik</strong>ken<br />
er ikke kendt. Meget tyder dog på at varmepåvirkningen<br />
af vævssnittene bl.a. har følgende<br />
indvirkning:<br />
a. Formaldehydinducerede tværbindinger<br />
(methenbroer) brydes.<br />
b. Komplekst bundne og epitopmaskerende<br />
Ca-ioner fjernes.<br />
c. Vævet rehydreres med forbedret penetration<br />
til følge.<br />
d. En vis proteindenaturering forekommer,<br />
hvilket kan blotlægge skjulte epitoper.<br />
Det skal her bemærkes, at formalinfiksering<br />
synes at have en beskyttende virkning mod<br />
denaturering af proteiner ved opvarmning -<br />
en proces, der ville denaturere ikke-fikserede<br />
proteiner.<br />
Der indgår i HIER-<strong>teknik</strong>ken en række variabler,<br />
nogle med stor betydning og andre med<br />
mindre betydning for epitop demaskeringen:<br />
Varmekilde, temperatur og tid<br />
Som varmekilde er flere alternativer afprøvet.<br />
Mikrobølgeovn (MBO) med eller uden trykkoger,<br />
almindelig kogeplade, autoklave, ”steamer”,<br />
vandbad og trykkoger<br />
(19,20,24,25,68,69) er alle varmekilder, der<br />
med succes har været anvendt i HIER-<strong>teknik</strong>ken.<br />
Det synes således ikke særligt kritisk,<br />
hvilken varmekilde der anvendes. Vigtigere<br />
end selve varmekilden er temperaturen i<br />
kogemediet, og den tid, snittene befinder sig<br />
deri (26,69).<br />
I den traditionelle HIER-<strong>teknik</strong>, hvor mikrobølgeovnen<br />
anvendes, opnås sædvanligvis tilfredsstillende<br />
epitopdemaskering efter kogning<br />
ved 100°C i 10 til 15 min. I autoklave,<br />
trykkoger, eller MBO-trykkoger er det p.g.a.<br />
trykket muligt at bruge temperaturer over<br />
100°C (115-120°C). Dette kan for visse epitoper<br />
give en mere effektiv demaskering.<br />
Leong et al (86) sammenlignede på 42 diagnostiske<br />
rutineantistoffer såkaldt ”superheating”<br />
(5 min. 120°C ved 1,9 bar i Milestone<br />
Mega T/T) med traditionel kogning i mikrobølgeovn.<br />
De fandt for ca. 30 af antistofferne<br />
kraftigere reaktioner efter ”superheating” end<br />
efter mikrobølgekogning. Lignende forsøg i<br />
eget lab (4) har ikke afsløret samme tydelige<br />
fordele ved ”superheating”. Mulige årsager<br />
kan være, at Leong primært brugte citratbuffer<br />
som kogebuffer og at kogetiden i mikrobølgeovn<br />
kun var på 10 min. I modsætning<br />
hertil har egne forsøg (4) været baseret på T-<br />
EG buffer pH9 (se afsn. vedr. kogemedium)<br />
og en kogetid på 15 min. i mikrobølgeovnen.<br />
En mindre forlængelse af kogetiden (samlet<br />
kogetid 15-20 min.) i mikrobølgeovnen kan<br />
øjensynligt give samme resultat som anvendelsen<br />
af ”superheating” (4,69) og være mere<br />
skånsomt ved vævet.<br />
”Cyklisk” kogning i form af 3-4 x 5 min hævdes<br />
for visse epitoper ligeledes at være mere<br />
effektiv end én sammenhængende kogeperiode<br />
(75), mens andre ikke har fundet nogen<br />
fordel herved.<br />
Det forhold, at lavere temperatur (T) kræver<br />
længere “kogetid” (t), understreges af Shi et<br />
al.’s (70) resultater med anti-Ki67, klon MIB1<br />
på tonsilvæv. Identisk og optimal demaskering<br />
af MIB1 epitopen blev opnået under følgende<br />
varmebehandlingsforhold (T x t):<br />
100°C x 20 min., 90°C x 30 min., 80°C x 50<br />
min., 70°C x 10 timer. Udover at kaste lys<br />
over nogle meget centrale forhold omkring<br />
HIER antyder disse resultater desuden, at<br />
epitopdemaskering ikke nødvendigvis altid<br />
behøver at foregå under egentlig kogning,<br />
men også kan foregå ved lavere temperaturer.<br />
Koopal et al.’s resultater (77) understøtter<br />
dette. I deres undersøgelse gav 16 af 16<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 23<br />
antistoffer identiske eller kraftigere reaktioner,<br />
når demaskering blev foretaget natten<br />
over ved 80°C i Tris-HCl pH 9<br />
(“low-temperature HIER”) sammenlignet med<br />
MBO-kogning i Tris-HCl pH 9,5 + 5% urea.<br />
Den morfologiske bevarelse angives som<br />
værende god efter behandlingen natten over<br />
ved 80°C, men desværre uden nogen detaljeret<br />
sammenligning til de MBO-behandlede<br />
snit. Når HIER-behandling ved lavere temperaturer<br />
- på trods af en voldsom forlængelse<br />
af inkubationstiden i “kogemediet” - alligevel<br />
kan være interessant, hænger det netop<br />
sammen med problemer med den morfologiske<br />
bevaring af visse væv. Kogning og<br />
høje temperaturer i øvrigt får kollagene fibre<br />
til at “kvælde op” og dermed løsne sig fra<br />
glasset. Det er et fænomen, der ind i mellem<br />
kan give visse fortolkningsmæssige problemer<br />
specielt i bindevævsrige tumorer. Da<br />
tendensen til “kvældning” af kollagen aftager<br />
med faldende HIER-temperatur, er demaskering<br />
ved lavere temperatur som alternativ til<br />
MBO-kogning ikke uinteressant. Undersøgelser<br />
i eget laboratorium har vist (4), at<br />
kvældning af kollagen helt kan undgås, hvis<br />
HIER-behandlingen foregår ved max. 60ºC.<br />
Forlænges behandlingen samtidig til 20-24<br />
timer, opnås resultater, der oftes er lig med<br />
eller kun marginalt svagere end, hvad der<br />
opnås efter kogning. Disse fund er gjort med<br />
TEG-buffer som ”kogemedium” (se afsn.<br />
vedr. kogemedium) og har medført, at ved<br />
receptor undersøgelser (ER og PgR påvisning)<br />
på mammacancer har denne ”lowtemperature<br />
HIER” (se afsn. vedr. HIERprotokoller)<br />
været anvendt som rutinemetode<br />
i Odense siden 2000. Shi et al (88) viste, at<br />
HIER ved lavere temperaturer end 100°C ikke<br />
blot er et spørgsmål om at forbedre morfologien<br />
i snittene. Det kan også være nødvendigt<br />
for at opnå optimal demaskering af specielt<br />
”varme-sensitive” antigener/epitoper.<br />
Shi et al fandt med et pAb mod COX-2<br />
(PG27), at traditionel kogningsdemaskering i<br />
citrat buffer pH 6 gav negative resultater.<br />
Ved at sænke temperaturen i citrat bufferen<br />
til 90°C opnåedes derimod en meget god<br />
demaskering. Optimal demaskering blev opnået<br />
med inkubationstider på 30-120 min.,<br />
mens inkubation natten over svækkede reaktionen<br />
voldsomt. Som konsekvens af disse<br />
fund anbefaler Shi et al. at inkludere en eller<br />
flere varianter af ”low-temperature HIER” i<br />
”test-batteriet” til sceening for optimal epitop<br />
demaskering (Tabel <strong>2.</strong>1 og <strong>2.</strong>2).<br />
Som nævnt synes valg af varmekilde ikke<br />
særlig kritisk. Den mikrobølgeinducerede<br />
varmebehandling er dog på mange måder<br />
den hurtigste og letteste måde at udføre<br />
HIER på. Da almindelige husholdnings-mikrobølgeovne<br />
er anvendelige, kræver<br />
denne <strong>teknik</strong> heller ikke den store investering.<br />
Problematikken omkring “hot-spots” og<br />
“cold-spots” i MBO-<strong>teknik</strong>ken har været diskuteret,<br />
men synes uden betydning for reproducerbarheden,<br />
hvis den praktiske udførsel<br />
af HIER metoden standardiseres (se HIERprotokoller<br />
nedenfor).<br />
Mogens Vyberg 2005<br />
Figur <strong>2.</strong>7: Intensiteten af immunreaktioner relateret<br />
til pH i kogemediet. Tre forskellige mønstre af<br />
pH-afhængighed har vist sig: Én gruppe antistoffer<br />
udviser kun ringe pH-relateret variation (A). En<br />
anden gruppe viser i svagt sure medier et dramatisk<br />
fald i intensitet (B), mens en tredje gruppe giver<br />
kraftigere reaktioner med et stigende pH. Efter Shi<br />
et al. (27).<br />
Firmaet BioCare har gennem udviklingen af<br />
deres såkaldte Decloaker bidraget til at gøre<br />
trykkogning til et attraktivt alternativ til mikrobølgekogning.<br />
Decloaker’en består af et<br />
lille trykkammer med indbygget elektrisk<br />
kogeplade. Den simple konstruktion gør instrumentet<br />
meget billigere end de fleste mikrobølgetrykkogere.<br />
Decloaker’en er til gengæld<br />
noget dyrere end både husholdningsmikrobølgeovne<br />
og traditionelle husholdnings-trykkogere.<br />
I forhold til traditionelle<br />
trykkogere burde resultaterne være mere<br />
reproducerbare med Decloaker på grund af<br />
det indbyggede program for opvarmning.<br />
Erfaringer i Aalborg tyder dog på, at en præcis<br />
kalibrering og dermed stabilitet kan være<br />
vanskelig at opnå med Decloaker.<br />
DakoCytomation har for nylig lanceret en<br />
tilsvarende trykkoger, Pascal.<br />
Uanset hvilken metode der anvendes til opvarmning,<br />
skal snittene efter kogning køle af i<br />
kogemediet, idet en direkte placering af glassene<br />
i kold PBS/TBS kan skade både<br />
vævsmorfologi og antigenisitet.<br />
Kogemedium<br />
Mange forskellige kogemedier har været afprøvet<br />
og anbefalet til HIER (26-29). Specielt<br />
2 generelle egenskaber ved kogemedierne<br />
synes at have en stor betydning for, hvor<br />
effektivt de fungerer i HIER-<strong>teknik</strong>ken. Disse<br />
egenskaber er:<br />
1. Kogemediets pH.<br />
<strong>2.</strong> Kogemediets evne til at kompleksbinde<br />
eller udfælde calciumioner.<br />
Shi et al (27) fandt, at ændringer i kogemediets<br />
pH kan resultere i dramatiske forskelle i<br />
den demaskerende effekt. Efter at have undersøgt<br />
immunfarvning med et panel af mAbs<br />
(ialt 9) efter HIER i forskellige kogemedier<br />
med pH variende fra 1 til 10, fandt man tre<br />
forskellige mønstre af pH-afhængighed (Fig.<br />
<strong>2.</strong>7).
24 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
En gruppe på fem antistoffer viste ingen<br />
nævneværdig variation i farvningsintensiteten<br />
inden for hele pH-området. To antistoffer<br />
(anti-Ki67, klon MIB1; og anti-ERα, klon 1D5)<br />
viste en V-formet kurve med et dramatisk<br />
fald i farvningsintensitet efter HIER i buffer<br />
med pH 3-5. Ved lavt pH og højt pH var reaktionen<br />
kraftig. Endelig viste to antistoffer<br />
(anti-CD43, klon MT1; og anti-melanosoma<br />
specific antigen, klon HMB45) ingen reaktion<br />
ved lavt pH, men herefter en gradvis forstærkning<br />
af reaktionen med stigende pH i<br />
kogemediet. Undersøgelsen viste, at Tris-HCl<br />
ved højt pH er langt mere velegnet som generelt<br />
kogemedium end citratbuffer pH 6.<br />
Lignende resultater kommer andre studier til<br />
(28,70,72), omend det er værd at bemærke,<br />
at Tris-HCl ved pH 1 med nogle antistoffer<br />
(ex: anti-Ki67, klon MIB1) giver endnu bedre<br />
demaskering end Tris-HCl ved pH 10 (70) En<br />
kedelig ulempe ved Tris-HCl pH 1 er, at der<br />
ikke sjældent ses en svag falsk positiv reaktion<br />
i en del kerner! Ydermere synes den generelle<br />
morfologiske bevaring at være ringere<br />
efter kogning ved pH 1 end ved pH 10.<br />
Morgan et al (29,71) fandt, at kompleksbinding<br />
eller udfældning af vævsbundne calciumioner<br />
og muligvis andre divalente metal<br />
kationer er et kritisk step i HIER-<strong>teknik</strong>ken.<br />
Som en konsekvens af dette må det antages,<br />
at en medvirkende årsag til maskering af<br />
epitoper er en tæt kompleksbinding af calciumioner<br />
og/eller andre divalente metal kationer<br />
til antigener (proteiner) under<br />
NBF-fiksering. Undersøgelsen viste med<br />
Ki67-antigenet og mAb MIB1 som udgangspunkt,<br />
at stærke kompleksbindere som EGTA<br />
og EDTA anvendt ved pH 8 er mere effektive<br />
til epitopdemaskering end den noget svagere<br />
kompleksbinder citrat.<br />
EDTA’s effektivitet på NBF- og B5-fikseret<br />
materiale er tydeligt blevet dokumenteret af<br />
Pileri et al. (72) Ud af 55 antistoffer, der<br />
kræver HIER, gav 1mM EDTA pH 8 i sammenligning<br />
med Tris-HCl pH 8 og citratbuffer<br />
pH 6 de bedste resultater med de 49.<br />
Siden 1996 er 2 modifikationer af Morgan’s<br />
EGTA/EDTA-HIER metode, gennem 2 uafhængige<br />
udviklingsarbejder, blevet rutine-demaskeringsmetode<br />
for flere og flere antistoffer.<br />
Brugen af T-EG buffer pH 9 (10mM<br />
Tris-base + 0,5mM EGTA) udspringer fra<br />
Patologisk Institut i Odense, mens TE buffer<br />
pH 9 (10mM Tris-HCl pH 9 + 1 mM EDTA)<br />
stammer fra Patologisk Institut i Aalborg. De<br />
2 buffere er uhyre effektive og giver stort set<br />
identiske resultater. I direkte sammenligning<br />
på 33 forskellige rutineantistoffer har T-EG<br />
buffer pH 9 og 1mM EDTA pH 8 givet noget<br />
nær den samme meget effektive demaskering<br />
(4). En uheldig egenskab, T-EG/TE bufferne<br />
deler med 1mM EDTA pH 8 og 0,1M<br />
Tris-HCl pH 10, er en voldsom forstærkning<br />
af falsk positiv reaktion som følge af endogen<br />
biotin. EGTA/EDTA-holdige buffere og Tris--<br />
HCl ved højt pH er alle meget effektive til at<br />
demaskere endogen biotin. Det skal dog understreges,<br />
at problemet synes mindre med<br />
T-EG/TE end med 1mM EDTA pH 8. Dette<br />
sammen med en lidt bedre morfologi er de<br />
vigtigste argumenter for at vælge T-EG- eller<br />
TE-bufferen fremfor 1mM EDTA pH 8.<br />
Mange af de større antistofproducenter fremstiller<br />
og sælger HIER-buffere produceret ud<br />
fra mere eller mindre hemmelige recepter.<br />
Med én undtagelse synes ingen af disse “miksturer”<br />
at kunne noget i HIER-henseende,<br />
som ikke kan opnås ved anvendelse af<br />
T-EG/TE buffer, citrat buffer eller Tris-HCl<br />
buffer ved pH 1 eller pH 10. Undtagelsen er<br />
DakoCytomations “Target Retrieval Solution,<br />
pH 6,1” kode S1699/S1700 (TRS). Denne<br />
modificerede citratbuffer er med de fleste<br />
antistoffer mere effektiv med hensyn til demaskering<br />
end standard citratbuffer pH 6. Til<br />
gengæld er den overfor de fleste antistoffer<br />
langt mindre effektiv end specielt T-EG/TE<br />
buffer og Tris-HCl pH 10. Når TRS alligevel er<br />
værd at nævne, skyldes det, at det for et<br />
mindre antal antistoffer har vist sig, at være<br />
den eneste HIER buffer, der giver brugbare<br />
resultater (4, 74). Blandt disse antistoffer kan<br />
nævnes: anti-CD5, klon Leu-1; anti-CD21,<br />
klon 1F8; anti-CD27 klon 137B4; antiepithelial<br />
antigen, klon Ber-EP4; antiepithelial-related<br />
antigen, klon MOC-31; antiepidermal<br />
growth factor receptor, klon E30,<br />
og anti-serotonin, klon 5HT-H209. TRS har på<br />
nuværende tidspunkt været testet på i alt ca.<br />
350 forskellige primære antistoffer. I godt 20<br />
tilfælde er de bedste resultater opnået med<br />
netop TRS (4).<br />
TRS bør derfor indgå i det batteri af buffere,<br />
som afprøves når et nyt antistof tages i anvendelse<br />
(se afsn. <strong>2.</strong>8.2). TRS er dyrere end<br />
både citrat og T-EG/TE buffer. Dog kan opløsningen<br />
angiveligt genbruges op til 20 gange<br />
(74).<br />
Flere studier har vist, at en kombination af<br />
proteolytisk forbehandling og HIER for nogle<br />
epitoper giver en mere effektiv demaskering,<br />
end hvis HIER eller proteolyse anvendes alene<br />
(74). Lignende fund er gjort i eget laboratorium<br />
(4). En del diagnostisk vigtige muskelmembran<br />
relaterede antigener er vanskellige<br />
at detektere tilfredsstillende i paraffinsnit.<br />
Epitoper på nogle af disse antigener<br />
har gavn af kombinations-demaskeringer som<br />
angivet i Tabel <strong>2.</strong><strong>2.</strong> Følgende antistoffer giver<br />
de bedste resultater med mild proteolyse<br />
efterfulgt af HIER i T-EG buffer (<strong>teknik</strong> 11):<br />
Anti-dystrophin klon DY4/6D3 og klon 34C5;<br />
anti-sarcoglycan delta, klon δ-Sarc/12C1;<br />
anti-myosin neonatal, klon WB-MHCn; antisarcoglycan<br />
beta, klon β-SARC/5B1; antisarcoglycan<br />
gamma, klon 35DAG/21B5; antispectrin,<br />
klon R8C2/3D5. Følgende antistoffer<br />
giver til gengæld de bedste resultater hvis<br />
HIER i citrat pH 6 efterfølges af mild proteolyse<br />
(<strong>teknik</strong> 12): Anti-caveolin 3, klon 26;<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 25<br />
anti-dysferlin, klon Ham1/7B6; anti-laminin<br />
alfa5, klon 4C7; anti-myosin developmental,<br />
klon RNMy2/9D2 og anti-sarcoglycan alfa,<br />
klon Ad1/20A6.<br />
Det er således ved kombinationsdemaskeringerne<br />
ikke ligegyldigt, hvilken<br />
HIER buffer der anvendes, og hvilken rækkefølge<br />
de 2 demaskeringer gøres i!<br />
Både for HIER-<strong>teknik</strong>ken og den proteolytiske<br />
forbehandling gælder, at der er en teoretisk<br />
risiko for at introducere nye krydsbindende<br />
sites i det forbehandlede væv. I praksis har<br />
det vist sig, at der sjældent introduceres<br />
krydsbindinger, der volder fortolkningsmæssige<br />
problemer.<br />
Forinden et nyt antistof med tilhørende epitopdemaskerings<strong>teknik</strong><br />
tages i brug i rutinesammenhæng,<br />
er en kritisk vurdering af positive<br />
reaktioner nødvendig, herunder evt.<br />
sammenligning med resultater opnået på<br />
frysesnit af de samme væv. For pAbs skal<br />
man også være opmærksom på, at forskellige<br />
demaskerings<strong>teknik</strong>ker kan favorisere forskellige<br />
af antistoffets kloner. Man kan således<br />
opleve, at S-100 pAb giver forskellige<br />
farveresultater efter proteolytisk og HIER<br />
forbehandling: Mens de fleste celler viser<br />
samme farveintensitet uanset forbehandlingen,<br />
vil nogle, fx follikulære dendritiske celler<br />
ved de almindeligt anvendte antistofkoncentrationer<br />
være S-100 negative efter proteolytisk<br />
forbehandling, men positive efter HIER.<br />
Tilsvarende forskel er set efter farvning af<br />
forskellige tumorer, fx gastrointestinal stromal<br />
tumor.<br />
HIER på cytologisk materiale<br />
Brugen af HIER-<strong>teknik</strong>ken er ikke begrænset<br />
til paraffinsnit. Også inden for cytologien er<br />
der store anvendelsesmuligheder. Reynolds<br />
et al (30) fandt på smears og imprints, at<br />
reaktionen for 12 af 14 antistoffer kunne<br />
forstærkes ved HIER efter formalinfiksering.<br />
Blandt antistofferne, der gav kraftigere reaktioner,<br />
var vigtige antistoffer som anti-ERα,<br />
klon 1D5; anti-p53, klon PAb1801; anti-C-erbB2,<br />
pAb; anti-CD20, klon L26; og<br />
anti-CD45 (LCA), klon 2B11 og PD7/26. Undersøgelser<br />
i Odense og Aalborg føjer yderligere<br />
til denne liste: anti-PgR, klon ICA og<br />
klon PgR636; anti-CyclinD1, klon P2D11F11;<br />
og anti-Ki67, klon MIB1, anti-vimentin, klon<br />
3B4, anti-pan-CK, klon AE1/AE3, antimelanosoma<br />
specific antigen, klon HMB45;<br />
og anti-melan A, klon A103. Undersøgelserne<br />
viste også, at de bedste resultater som regel<br />
opnås på cytologisk materiale efter NBF fiksering,<br />
og at fikseringstid bør være minimum<br />
15 min. Ved kortere fikseringstid i NBF eller<br />
ved brug af svagere fiksativer som acetone<br />
og etanol er der en risiko for tab af cytologiske<br />
detaljer.<br />
Det gælder for det cytologiske materiale som<br />
for det histologiske, at der med alternative<br />
Mogens Vyberg 2005<br />
kogemedier kan opnås yderligere forbedringer<br />
sammenlignet med citratbuffer. Kogning i<br />
TRS giver for mange antistoffer betydeligt<br />
bedre resultater end citrat. Anvendes T-<br />
EG/TE buffer kan opnås yderligere forbedring<br />
mht demaskerende effekt. Desværre er den<br />
cytologiske bevaringsgrad efter kogning i en<br />
af disse buffere ikke god. Foretages demaskering<br />
i stedet ved lavere temperatur svarende<br />
til TEG95 protokollen (se nedenfor<br />
vedr. HIER protokoller) opnås foruden en<br />
yderst effektiv demaskering også god cytologisk<br />
bevarelse. I TEG95 protokollen bringes<br />
T-EG bufferen i kog i MBO, hvorefter bufferen<br />
tages ud af ovnen og prøvematerialet anbringes<br />
i den varme buffer 15 min. Specielt gode<br />
resultater er bl.a. opnået med anti-PgR, klon<br />
PgR 636; anti-ERα, klon 1D5 og klon 6F11;<br />
anti-tyrosinase, klon T311; anti-TTF-1, klon<br />
SPT24 og anti-synaptophysin klon snp88 (4).<br />
Væskebaseret cytologi (Liquid based cytologi,<br />
LBC) vinder i disse år mere og mere indpas<br />
indenfor patologien. I stedet for manuelt at<br />
udstryge prøvematerialet opsamles det i en<br />
alkoholbaseret præserveringsvæske, hvorfra<br />
der maskinelt kan produceres meget ensartede<br />
”aftryk” (ThinPrep eller AutoCytePrep),<br />
som efter alkoholfiksering (96% etanol eller<br />
spray-fix) kan anvendes til analyse. Teknologien<br />
er primært udviklet til cervix-cytologisk<br />
materiale, men kan anvendes til de fleste<br />
cytologiske materialer. Immuncytokemiske<br />
undersøgelser kan med fordel udføres på<br />
ThinPrep og AutoCytePrep. En forudsætning<br />
er naturligvis for de enkelte antistoffer at<br />
finde de optimale fikserings- og HIERbetingelser.<br />
Forsøg i eget laboratorium med<br />
21 diagnostiske rutineantistoffer og 6 forskellige<br />
”fikserings-HIER” protokoller viste, at<br />
TEG100 protokollen for de 19 antistoffer gav<br />
klart de bedste resultater. Blandt de 19 antistoffer<br />
var anti-ERα, klon 6F11; anti-Ki67,<br />
klon MIB1; anti-TTF1, klon SPT24; anti-CK,<br />
klon AE1+AE3: anti-vimentin, klon V9; anti-<br />
CD45, klon 2B11+PD7/26. Cellernes ophold<br />
(fra timer til dage) i præserveringsvæsken og<br />
den efterfølgende alkoholfiksering nødvendiggør<br />
en mere effektiv HIER behandling end<br />
blot kogning i citratbuffer eller behandling i<br />
95°C varm T-EG buffer. I TEG100 protokollen<br />
koges materialet 15 min i T-EG buffer. Den<br />
forlængede fiksering i alkohol gør, at den<br />
cytologiske bevaringsgrad af cellerne er god,<br />
selv efter kogning i T-EG buffer.<br />
HIER <strong>teknik</strong>ken kan også med nogen succes<br />
anvendes som forbehandling til immuncytokemiske<br />
undersøgelser på Papanicolau- eller<br />
Giemsafarvede smears. HIER er i stand til at<br />
demaskere en del antigener i de farvede<br />
smears, samtidig med at den er effektiv til at<br />
affarve cellerne. Identifikation af Ki67antigenet<br />
med klon MIB1 i Papanicolaufarvede<br />
smears har bl.a. vist sig nyttig til at<br />
skelne mellem normale celler og carcinoma in<br />
situ i atrofiske cervix smears (31). For at<br />
bevare cytologiske detaljer i smearet anbefales<br />
det at fiksere de rehydrerede celler i 4%<br />
NBF i 15 min. før HIER iværksættes (4).
26 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Tabel <strong>2.</strong>1: ”Test-battery” til screening for optimal<br />
HIER-<strong>teknik</strong>, efter Shi et al. (73).<br />
Buffer a pH1 pH6 pH10<br />
120ºC, 10 min b Snit#1 Snit#4 Snit#7<br />
100ºC, 10 min. Snit#2 Snit#5 Snit#8<br />
90ºC, 10 min. Snit#3 Snit#6 Snit#9<br />
a10mM Tris-HCl anvendes ved pH 1, 10mM Citrate<br />
ved pH 6 og 100 mM Tris-HCl ved pH 10.<br />
b 120ºC opnås ved hjælp af autoklave eller trykkoger.<br />
Samme effekt kan opnås ved forlænget MBO-kogning<br />
(20 min.).<br />
I tidligere Giemsa farvede præparater er<br />
mange antigener specielt vanskelige at påvise.<br />
Her kan citratbufferen med fordel erstattes<br />
med TE/T-EG buffer. Tilfredsstillende resultater<br />
er således opnået på Giemsapræparater<br />
med anti-Ki67, klon MIB1; og anti-ERα,<br />
klon 1D5; efter 15 min. MBO-kogning i T-EG<br />
buffer (med forfiksering 15 min. i 4% NBF).<br />
Der er dog ved denne <strong>teknik</strong> risiko for falsk<br />
negative reaktioner, som kan være vanskelige<br />
at identificere!<br />
HIER og standardisering<br />
Med introduktionen af varmebaseret epitop<br />
demaskering først i 90’erne og specielt med<br />
lanceringen af den citratbuffer-baserede <strong>teknik</strong><br />
syntes mulighederne gode for en øget<br />
standardisering indenfor immunhistokemien.<br />
Der var en overgang et begrundet håb om, at<br />
én standard HIER procedure kunne konstrueres.<br />
Denne skulle udviske alle fikseringsprocedurens<br />
varierende påvirkninger (maskeringer)<br />
af antigene epitoper og hermed fjerne et<br />
væsentlig grundlag for de resultatmæssige<br />
uoverensstemmelser, som den immunhistokemiske<br />
litteratur desværre er præget af. Nu<br />
5-6 år senere synes udviklingen ikke entydigt<br />
at have bragt os nærmere en standard HIER<br />
<strong>teknik</strong>, der kan bruges til alle antistoffer -<br />
tværtimod er udbuddet af HIER modifikationer<br />
næsten endeløs. Når vi alligevel i dag er<br />
tættere på en vis form for standardisering<br />
indenfor HIER-<strong>teknik</strong>kerne end for 5-6 år<br />
siden, skyldes det især et par forskergruppers<br />
ihærdige og metodiske arbejde med at afdække<br />
de enkelte parametres betydning for<br />
HIER-<strong>teknik</strong>ken (27,29). I dag bør HI-<br />
ER-standardiseringen tage udgangspunkt i, at<br />
der ikke findes én HIER metode, der er optimal<br />
for alle antistoffer (epitoper). I stedet bør<br />
de enkelte laboratorier i højere grad standardisere<br />
måden hvorpå de tester nye (og gamle!)<br />
antistoffer på. Shi et al (70, 73) anbefaler<br />
at HIER-standardisering tager udgangspunkt i<br />
at fastlægge, hvad de betegner som “maximal<br />
retrieval” (maksimal demaskering) for et<br />
givet antistof ved hjælp af et “HIER<br />
test-battery” omfattende de vigtigste HIER<br />
parametre: pH, temperatur og tid (Tabel<br />
<strong>2.</strong>1). Den HIER-<strong>teknik</strong>, der giver maximal<br />
retrieval, bør herefter anvendes rutinemæssigt<br />
til det pågældende antistof.<br />
Et lignende “test-batteri” har været i brug i<br />
eget laboratorium siden 1996 med succes<br />
(Tabel <strong>2.</strong>2). “Test batteriet” til sceening for<br />
optimal epitop retrieval indeholder foruden de<br />
vigtigste elementer fra Shi’s “test batteri”<br />
også non-HIER <strong>teknik</strong>ker og vigtige HIER<br />
parametre ( bl.a. calcium kompleksbinding),<br />
der ikke er med i Shi’s initiale batteri.<br />
HIER protokoller - MBO-<strong>teknik</strong><br />
Protokol A - Traditionel “cyklisk” kogning af 1<br />
slideholder (24 glas).<br />
1. Snit anbringes i grå 24 stk’s Tissue—Tek slideholders.<br />
Evt. tomme pladser fyldes med blanke<br />
objektglas. Slideholder anbringes i Tissue-Tek<br />
farveskål med 250 ml kogemedium.<br />
<strong>2.</strong> Farveskål med snit anbringes centralt i mikrobølgeovnen.<br />
Der koges 5 min. med effekt på<br />
600 - 700 W<br />
3. Fordampet medium erstattes ved efterfyldning<br />
med destilleret vand. Der koges 5 min.<br />
4. Trin 3 gentages (ved forlænget kogetid gentages<br />
trin 3 det nødvendige antal gange).<br />
5. Efter kogning anbringes kogemedium med snit<br />
på bordet til nedkøling 15 min.<br />
6. Skyl i buffer og fortsæt farvningsproceduren.<br />
Protokol B - Kogning af 3 slideholders (72<br />
glas).<br />
Protokol B foretages med 3 fyldte Tissue Tek<br />
slideholders i 3 Tissue Tek farveskåle med<br />
250 ml kogemedium. Protokol B gør det muligt<br />
at foretage 3 forskellige kogeprocedurer<br />
på én gang. Det være sig kogning i 3 forskellige<br />
buffere eller kombinationen af 2 farveskåle<br />
med en rutinemæssig 15 min. kogning<br />
og 1 farveskål med en forlænget 25 min.<br />
kogning. I tilfælde hvor der ikke er behov for<br />
3 farveskåle med kogebuffer, “fyldes der op”<br />
med farveskål(e) med dest vand og slideholder(s)<br />
med blanke glas således, at mængden<br />
af kogemedium og glas altid er den samme.<br />
Protokol B kræver at mikrobølgeovnen er<br />
udstyret med drejeplade.<br />
1. Snit anbringes i grå 24 stk’s<br />
Tissue—Tek slideholders. Evt.<br />
tomme pladser fyldes med<br />
blanke objektglas. Slideholder<br />
anbringes i Tissue-Tek farveskål<br />
med 250 ml kogemedium.<br />
3 farveskåle anbringes<br />
perifert på drejepladen i mikrobølgeovnen,<br />
som angivet på figuren.<br />
<strong>2.</strong> Start mikrobølgeovnen på fuld effekt (700-<br />
900W) med drejepladen aktiveret. Notér tidspunktet<br />
for hvornår kogemedierne kommer i<br />
kog. Dette gøres de første gange metoden bruges,<br />
herefter kendes opvarmningtiden, der er<br />
nødvendig for den enkelte ovn. Denne tid kan<br />
bruges efterfølgende. For en Moulinex Y51 med<br />
effekt 900W skal bruges 11 min. for at bringe 3<br />
farveskåle i kog.<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 27<br />
3. Når alle 3 kogemedier er bragt i kog, nedsættes<br />
effekten således, at væskerne “simrekoger”,<br />
kogningen fortsætter i 15 min. For hver enkelt<br />
mikrobølgeovn må dette effekttrin fastlægges<br />
via forsøg med blanke glas. Målet er, at væskerne<br />
koger mest muligt uden at koge for meget<br />
over (tab af væske). For en Moulinex Y51 er<br />
det optimale effektrin for “simrekogning” 400W.<br />
4. Efter kogning anbringes kogemedium med snit<br />
på bordet til nedkøling 15 min. Fortsæt til trin<br />
7.<br />
5. En evt. farveskål med snit, der skal koges 25<br />
min., flyttes nu til midten af ovnen og der koges<br />
yderligere 10 min. på et extra nedsat effektrin<br />
(skal igen fastlægges via forsøg for den<br />
enkelte ovn). For en Moulinex Y51 er det optimale<br />
effekttrin 170W.<br />
6. Efter kogning anbringes kogemedium med snit<br />
på bordet til nedkøling 15 min.<br />
7. Skyl i buffer og fortsæt farvningsproceduren.<br />
Protokol C - 24 timers “Low-temperature<br />
HIER”<br />
1. Snit anbringes i grå 24 stk’s Tissue-Tek slideholder.<br />
Evt. tomme pladser fyldes med blanke<br />
objektglas. Slideholder anbringes i Tissue-Tek<br />
farveskål med 250 ml kogemedium.<br />
<strong>2.</strong> Farveskål med snit anbringes i varmeskab ved<br />
60°C. Inkubationtid 24 timer.<br />
3. Efter varmebehandlingen anbringes farveskål<br />
med snit på bordet til nedkøling 15 min.<br />
4. Skyl i buffer og fortsæt farvningsproceduren.<br />
NBF-HIER protokoller til cytologisk materiale<br />
”Citrat protokol” og ”TRS protokol”<br />
1. NBF 4% 15 min<br />
<strong>2.</strong> Ethanol 96% skyl 15 sek<br />
3. Ethanol 96% 10 min<br />
4. Rindende vand 5 min<br />
5. Kogning i citratbuffer eller TRS<br />
(Protokol B)<br />
15 min<br />
”TEG100 protokol”<br />
1. NBF 4% 15 min<br />
<strong>2.</strong> Ethanol 96% skyl 15 sek<br />
3. Ethanol 96% 10 min<br />
4. Rindende vand 5 min<br />
5. Kogning i T-EG buffer<br />
(Protokol B)<br />
15 min<br />
”TEG95 protokol”<br />
1. NBF 4% 15 min<br />
<strong>2.</strong> Ethanol 96% skyl 15 sek<br />
3. Ethanol 96% 10 min<br />
4. Rindende vand 5 min<br />
5. Demaskering i T-EG buffer ved 95°C (a) 15 min<br />
(a) Objektglas anbringes i grå 24 stk’s Tissue-Tek<br />
slideholder.<br />
Mogens Vyberg 2005<br />
Evt. tomme pladser fyldes med blanke objektglas.<br />
250 ml T-EG buffer i Tissue-Tek farveskål bringes<br />
til kogning i mikrobølgeovn. Farveskålen fjernes fra<br />
ovnen og stilles på bordet og slideholder med præparaterne<br />
anbringes straks i den varme buffer (ca.<br />
95°C). Efter demaskering skylles i rindende vand.<br />
Dehydreringen/fikseringen i ethanol efter NBF<br />
betyder, at chromogen-udfældningen i cellerne<br />
bliver mere homogen (ligner hvad der<br />
opnås på paraffinsnit) end, hvis dette trin<br />
udelades. Uden ethanol bliver reaktionsproduktet<br />
specielt med AEC meget granulært!<br />
Udvalgte HIER buffere<br />
T-EG buffer pH 9, 10mM+0,5mM<br />
Tris (Sigma T-1378) 1,211 g<br />
EGTA “Titriplex VI” (Merck 8435) 0,190<br />
Dest. vand 1000 ml<br />
Opløsningen behøver ingen pH-justering. pH er<br />
normalt mellem 8,95 og 9,1<br />
TE buffer pH 9, 10mM+1mM<br />
Tris (Sigma T-1378) 1,211 g<br />
EDTA ”Titriplex III” (Merck 8418) 0,372 g<br />
Dest. vand 1000 ml<br />
Opløsningen behøver ingen pH-justering. pH er<br />
normalt mellem 8,90 og 9,05<br />
Citrat buffer 10mM, pH 6<br />
Citronsyre, monohydrat 2,1 g<br />
Dest. vand 00 ml<br />
pH justeres til 6,0 med 2M NaOH.<br />
Tilsæt destilleret vand til 1000 ml<br />
EDTA 1mM, pH 8<br />
EDTA ”Titriplex III” (Merck 8418) 0,372 g<br />
Dest. vand 1000 ml<br />
pH justeres til pH 8,0 med 1M NaOH.<br />
<strong>2.</strong>7 Blokering af uspecifik<br />
antistofadhæsion<br />
Såkaldt uspecifik baggrundsfarvning kan i<br />
visse tilfælde volde problemer i immunhistokemiske<br />
<strong>teknik</strong>ker. Problemet ses oftest<br />
ved anvendelse af pAb med ringe aviditet<br />
(“affinitet”). Årsagen til denne baggrundsfarvning<br />
er, at immunglobuliner udover den<br />
specifikke interaktion med antigene epitoper<br />
også er i stand til at binde sig til vævsproteiner<br />
ved hjælp af svagere, uspecifikke bindinger.<br />
Antistofmolekyler vil specielt kunne adhærere<br />
til vævssnittet gennem elektrostatisk<br />
tiltrækning og hydrofob interaktion.<br />
Den traditionelle måde at imødegå uspecifik<br />
antistofadhæsion er dels gennem forbehandling<br />
med “blocking protein” og dels tilsætning<br />
af “blocking protein” til antistofopløsningerne.
28 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Ved at præinkubere med proteinopløsning<br />
opnås en blokering af vævsproteinernes mulighed<br />
for bl.a. hydrofob interaktion med antistofmolekyler.<br />
Valg af proteinopløsning er<br />
naturligvis vigtig. Proteinet skal være i stand<br />
til at konkurrere effektivt med IgG-molekyler<br />
med hensyn til hydrofob interaktion. Tidligere<br />
anvendtes næsten udelukkende sera fra ikke-immuniserede<br />
dyr (“normal sera”) til denne<br />
forbehandling. Betydningen af denne forbehandling<br />
er aftaget i takt med udviklingen<br />
af bedre antistoffer og visualiserings<strong>teknik</strong>ker.<br />
I nogle tilfælde ses normalserum faktisk<br />
at give en forøgelse af baggrundsfarvningen!<br />
I dag anvendes i vid udstrækning bovint serum<br />
albumin (BSA), casein opløsninger<br />
og/eller detergentia (fx Triton X-100 og<br />
Tween 20), ikke alene som forbehandling,<br />
men også som tilsætning til fortynderbuffere.<br />
Casein synes specielt at være et godt og effektivt<br />
universalmiddel til blokering af uspecifik<br />
antistofadhæsion (32).<br />
Protokoller til blokering af uspecifik antistofadhæsion:<br />
1. Casein 0,5 % i PBS eller TBS 10-20 min.<br />
eller<br />
<strong>2.</strong> Normal serum, 5 % i PBS eller TBS 10 min.<br />
eller<br />
3. BSA, 2 % i PBS eller TBS 10 min.<br />
eller<br />
4. Detergent (Tween 20 eller Triton X-100), 0,25 %<br />
- 1 % i PBS eller TBS 10 min.<br />
Ved brug af mAbs og gode oprensede pAbs<br />
(Ig-fraktion eller bedre) i de gængse detektionssystemer<br />
er BSA forbehandling eller<br />
grundig vask i buffer med detergent (jvf.<br />
protokol 4) sædvanligvis fuldt tilstrækkeligt.<br />
Disse forbehandlinger kombineres sædvanligvis<br />
med tilsætning af 1 % BSA til antistof<br />
opløsningerne. Anvendes fuldsera antistoffer<br />
eller benyttes ekstremt følsomme detektionssystemer<br />
som TSA (afsn. <strong>2.</strong>10.2) stilles ofte<br />
større krav til blokering af antistof-adhæsion.<br />
I disse tilfælde bør casein anvendes.<br />
Blokering af Fc-receptorer<br />
Fc-receptorer er membranproteiner, der binder<br />
sig til Fc-delen på antistofmolekyler med<br />
en forholdsvis høj bindingsstyrke.<br />
Fc-receptorer findes fortrinsvis på granulocytter<br />
og makrofager. Uspecifik baggrundsfarvning<br />
på grund af antistoffers binding til<br />
Fc-receptorer ses normalt ikke på paraffinsnit.<br />
Formalinfiksering og vævspræparation<br />
ændrer Fc-receptorerne, således at de normalt<br />
ikke længere er i stand til at binde antistofferne.<br />
På acetonefikserede frysesnit og<br />
cytologisk materiale kan problemet til gengæld<br />
ses. Generelt volder det ikke de store<br />
problemer, men i makrofag-rige cytologiske<br />
materialer såsom bronkio-alveolær lavage<br />
(BAL) væsker kan den Fc-receptor betingede<br />
reaktion være generende. Problemet er især<br />
tydeligt, hvis der anvendes mAbs af subklasserne<br />
IgG2a (fx anti-CD20, klon L26; og anti-CK20,<br />
klon Ks20.8) eller IgG3. Dette skyldes,<br />
at især disse subklasser af muse IgG<br />
bindes til visse humane Fc-receptorer (52).<br />
Problemet med Fc-receptorer kan undgås ved<br />
at anvende F(ab’)2 fragmenter af antistofferne<br />
(både primære og sekundære antistoffer) i<br />
stedet for hele IgG-molekyler. En simpel alternativ<br />
løsning på problemet, der normalt<br />
virker tilfredsstillende, er at forbehandle med<br />
5% humant immunglobulin inden inkubation<br />
med primært antistof. Fc-receptorerne i prøvematerialet<br />
binder Ig og blokeres herved. I<br />
visse tilfælde kan det være nødvendigt også<br />
at inkludere 1% humant Ig i antistofopløsningerne.<br />
<strong>2.</strong>8 Primært antistof<br />
<strong>2.</strong>8.1 Valg af antistof<br />
Udbudet af kommercielle antistoffer er<br />
enormt, og der kommer hver dag nye til. Det<br />
kan derfor være vanskeligt at vælge hvilke(t)<br />
antistof(fer), man skal købe til påvisning af et<br />
givet diagnostisk interessant antigen. Gennem<br />
opslagsværker som Linscott’s Directory<br />
(33) og Manufacture’s Specifikations & Reference<br />
Synopsis (”MSRS”) (34) vil det være<br />
muligt at få et rimeligt overblik over udbudet<br />
og hvem, der producerer/forhandler de pågældende<br />
antistoffer. På trods af opdateringsblade<br />
mv. forældes disse opslagsværker<br />
hurtigt. On-line versionerne på internettet er<br />
derfor at foretrække.<br />
www.antibodies-probes.com<br />
På denne adresse finder man MSRS’s on-line<br />
database med data på mere end 165.000<br />
kommercielle primære antistoffer. Databasen<br />
er brugervenlig med i alt 11 forskellige søgefelter.<br />
Den opdateres løbende og kan på trods<br />
af et årligt abonnement på 98 USD anbefales.<br />
En gratis demo-version af databasen er tilgængelig<br />
på samme adresse. Linscott’s Directory’s<br />
on-line version findes på adressen:<br />
www.linscottsdirectory.co.uk<br />
Databasen indeholder mere end 100.000<br />
forskellige produkter, overvejende primære<br />
antistoffer. Det koster på årsbasis 75 USD at<br />
abonnere på den service. En gratis demoversion<br />
af databasen er tilgængelig på adressen.<br />
Databasen er ikke så stor og knap så<br />
brugervenlig som MSRS databasen. Til gengæld<br />
indeholder den andet end primære antistoffer.<br />
Blandt internettets mange gratis glæder findes<br />
også mange websites, der mere eller<br />
mindre er helliget antistoffer og immunhistokemi.<br />
Blandt disse kan følgende varmt anbefales:<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 29<br />
SciQuest er et internetfirma, der har specialiseret<br />
sig i formidling af køb og salg af ”Scientific<br />
Products”. På firmaets website:<br />
www.sciquest.com<br />
findes on-line databasen ”AntibodyResource”<br />
med mere end 120.000 antistoffer fra de<br />
fleste større antistofproducenter. Tjenesten<br />
er gratis, men kræver log in med bruger id og<br />
password. Firmaet abcam,<br />
www.abcam.com<br />
der bl.a. lever af at sælge antistoffer over<br />
internettet, har en meget kraftfuld søgetjeneste,<br />
der ikke alene søger hos abcam selv,<br />
men også i andre antistofproducenters online<br />
kataloger. Denne søgemaskine er meget<br />
enkel og populær.<br />
Et par meget brugbare databaser hver med<br />
40-60.000 antistoffer findes hos:<br />
BioCompare:<br />
www.biocompare.com<br />
LabVelocity:<br />
www.researchlink.labvelocity.com<br />
Bag adressen:<br />
www.antibodyresource.com<br />
gemmer sig en privat hjemmeside med et<br />
væld af nyttige links til andre internetadresser<br />
med antistoffer som hovedemne. Der er<br />
således links til mere end 250 on-line firmaer,<br />
der sælge antistoffer. Hos de fleste af disse<br />
firmaer er det muligt via lokale databaser at<br />
finde datablade og andre oplysninger frem på<br />
firmaets produkter.<br />
Også adressen<br />
www.immunoquery.com<br />
giver mulighed for at finde antistoffer i forbindelse<br />
med opstilling af immunhistokemiske<br />
algoritmer. Den er gratis at bruge, men kræver<br />
password (der fås på samme adresse).<br />
På <strong>NordiQC</strong>’s hjemmeside:<br />
www.nordiqc.org<br />
publiceres resultaterne af de kvalitetssikrings<br />
runder, som IHC-laboratorier i Norden tilbydes<br />
at deltage i. Hvert år tilbydes 3 runder,<br />
hver med detektion af ca. 5 forskellige epitoper.<br />
Hjemmesiden indeholder en hastigt voksende<br />
database med detaljerede beskrivelser<br />
af diagnostisk vigtige epitoper. Optimale protokoller<br />
fra de enkelte kvalitetssikringsrunder<br />
kan frit downloades. Denne hjemmeside er et<br />
”must” for laboratorier, der beskæftiger sig<br />
med diagnostisk immunhistokemi.<br />
Med datablade, litteratur-referencer og anden<br />
information om de pågældende antistoffer i<br />
hånden er det så op til den enkelte bruger at<br />
vurdere, hvilke af antistofferne der kan være<br />
Mogens Vyberg 2005<br />
brugbare til den påtænkte applikation. Blandt<br />
de brugbare antistoffer skal herefter vælges<br />
det ”bedste” antistof. Det sidste er ofte umuligt<br />
at få en uvildig vurdering af. Er ressourcerne<br />
tilstede, er det bedste, man kan gøre,<br />
at kontakte producenterne med henblik på at<br />
få en lille gratis prøve. Man kan således uden<br />
omkostninger til antistof-indkøb teste og<br />
eventuelt sammenligne flere forskellige antistoffer<br />
mod det antigen, der ønskes undersøgt.<br />
<strong>2.</strong>8.2 Afprøvning af antistoffer<br />
Erhverves et nyt antistof, skal der altid foretages<br />
en grundig afprøvning, inden det anvendes<br />
i diagnostisk sammenhæng. Der bør<br />
være to klare mål med afprøvningen af antistoffet:<br />
1. Procedureteknisk optimering (fortynding,<br />
epitop demaskering, fiksering, mv).<br />
<strong>2.</strong> Vurdering af antistoffets reaktivitet og<br />
specificitet.<br />
Afprøvningen af antistoffet bør foretages med<br />
det eller de detektionssystemer, som laboratoriet<br />
normalt anvender og tage udgangspunkt<br />
i de præparationstyper, som antistoffet<br />
tænkes anvendt på. Paraffinsnit vil i de fleste<br />
tilfælde være det primære applikationsområde,<br />
alligevel må det anbefales også at inkludere<br />
frysesnit af relevante væv, især når det<br />
drejer sig om antistoffer, der ikke er veldokumenterede.<br />
Dette åbner mulighed for en<br />
sammenligning af resultaterne på de to forskellige<br />
præparationstyper. Det er selvfølgelig<br />
vigtigt, at reaktiviteten af antistoffet er den<br />
samme på de to præparationstyper. Er dette<br />
ikke tilfældet, skal det registreres og årsagen<br />
evt. findes. I praksis vil en del antistoffer give<br />
svagere reaktioner på paraffinsnit end på<br />
frysesnit. Ligeledes vil nogle antistoffer give<br />
svagere reaktioner på cryosnit end på paraffinsnit.<br />
Et mindre antal nyere mAbs (bl.a.:<br />
anti-CD5, klon 4C7; anti-CD2, klon AB75;<br />
anti-CD13, klon 38C12 og anti-CD14, klon 7),<br />
der fungerer godt på paraffinsnit, kan således<br />
ikke anvendes på cryosnit.<br />
Intensitetsforskelle i reaktionen i de to præparationstyper<br />
er i sig selv ikke nødvendigvis<br />
nogen katastrofe. Det vigtigste er, at der<br />
opnås det samme reaktionsmønster på de to<br />
præparationstyper (de samme celler/strukturer<br />
skal være positive/negative) og at<br />
reaktionsmønstret sammenholdes med og<br />
fortolkes i sammenhæng med de i litteraturen<br />
beskrevne resultater.<br />
Materiale til antistofafprøvninger<br />
1. Paraffinsnit af multiblokke/tissue<br />
microarrays<br />
<strong>2.</strong> Frysesnit<br />
3. Cytologisk materiale.
30 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Anvendelsen af større multiblokke (35-38)<br />
eller tissue microarrays (91) giver gode muligheder<br />
for på én gang at optimere den tekniske<br />
brug af antistoffet og samtidig vurdere<br />
antistoffets reaktivitet overfor en lang række<br />
normale og patologiske væv. Anvendelse af<br />
multiblokke i afprøvningen af nye antistoffer<br />
er derfor meget vigtig.<br />
Parametre til afprøvning på paraffinsnit<br />
1. Fikseringstiden i NBF (6 - 168 timer)<br />
<strong>2.</strong> Epitop demaskering.<br />
Medtages tonsilvæv fikseret henholdsvis 6,<br />
24, 48 og 168 timer i multiblokkene, er det<br />
muligt for de fleste antigeners vedkommende<br />
at undersøge fikseringstidens betydning for<br />
antigenisiteten. Et brugbart alternativ til tonsilvæv<br />
er fx tyndtarm.<br />
Det er uhyre vigtigt at få fastlagt den optimale<br />
epitop demaskering for alle nye antistoffer<br />
(Tabel <strong>2.</strong>2 og afsn. <strong>2.</strong>6.2).<br />
Parametre til afprøvning på frysesnit og<br />
cytologisk materiale<br />
a. Acetone 10 min.<br />
b. 4% NBF 2 - 30 min.<br />
c. Acetone/metanol (1:1) 30 - 90 sek.<br />
d. På cytologisk materiale bør NBF-fiksering<br />
kombineret med detegent forbehandling<br />
(se afsn. <strong>2.</strong>4.3) og NBF-fiksering kombineret<br />
med HIER (se afsn. <strong>2.</strong>6.2) også afprøves.<br />
På frysesnit og cytologisk materiale er det<br />
vigtigt at finde den fikseringsprotokol og forbehandlingsprotokol,<br />
der giver de bedste<br />
resultater med det pågældende antistof. De<br />
nævnte fikseringer samt producentens anbefalede<br />
protokol bør som minimum afprøves.<br />
Opnås der ikke tilfredsstillende resultater<br />
med en af disse protokoller, må alternative<br />
fiksativer undersøges (se afsn. <strong>2.</strong>4.3).<br />
<strong>2.</strong>8.3 Antistof-inkubation<br />
Inkubation med primært antistof og de øvrige<br />
immunoreagenser foregår normalt ved at<br />
pådryppe horisontalt lejrede materialer en<br />
passende mængde reagens (50-200µl). Før<br />
antistoffet appliceres, tørres overskydende<br />
væske bort omkring materialet og der etableres<br />
evt. en hydrofob barriere ved hjælp af<br />
fedtstift (DAKO-Pen eller lignende). Den hydrofobe<br />
barriere sikrer, at antistoffet ikke<br />
“løber af”. For at undgå fordampning og udtørring<br />
skal inkubationen foregår i fugtkammer.<br />
Materialet må på intet tidspunkt udtørre.<br />
Selv udtørring af paraffinsnit umiddelbart<br />
efter endt afparaffinering har vist en tydelig<br />
negativ effekt på flere membranlokaliserede<br />
antigener.<br />
Den traditionelle “dråbe-inkubation” er, på<br />
grund af den gentagende håndtering af det<br />
enkelte præparat, meget arbejdskrævende,<br />
men kan ikke for det primære antistof undgås<br />
uden automatisering (se nedenfor). Derimod<br />
kan man ved daglig farvning af store batches<br />
opnå en rationalisering ved at applicere detektionssystemet<br />
via farvevugger (racks) i<br />
større farveskåle (39,40).<br />
Automatisering<br />
Automatisering af hele farvningsproceduren<br />
er selvfølgelig den ultimative løsning på den<br />
omfattende håndtering af præparaterne.<br />
Mange firmaer tilbyder forskellige løsninger,<br />
der automatiserer mere eller mindre af farvningsproceduren.<br />
Fire firmaer dominerer pt<br />
verdensmarkedet for immunostainers: Bio-<br />
Genex, LabVision, Ventana og Dako-<br />
Cytomation.<br />
LabVision og DakoCytomations ”AutoStainer”<br />
og BioGenexs ”i6000” minder meget om hinanden.<br />
Begge er åbne systemer, der arbejder<br />
med horisontalt lejrede objektglas og en<br />
computerstyret robotarm med dispensor, der<br />
applicerer alle immunoreagenserne. Fælles<br />
for disse immunostainers er desuden, at de<br />
ikke kræver specielle reagenser eller utensiler.<br />
Kapaciteten på instrumenterne er moderat:<br />
BioGenex i6000 kan håndtere 60 objektglas.<br />
DakoCytomations Autostainer klarer 48<br />
glas ad gangen, mens LabVisions Autostainer<br />
fås til 36, 48 eller 72 glas. Eridan - et helt nyt<br />
fuldautomatisk instrument fra DakoCytomation<br />
med introduktion i 2005 - fås med en<br />
kapacitet på 60 glas.<br />
Ventana har flere instrumenter: TechMate500,<br />
NexES, BenchMark og Discovery.<br />
BenchMark og Discovery er avancerede instrumenter<br />
med en kapacitet på henholdsvis<br />
30 og 20 glas. Kapaciteten er ikke høj, til<br />
gengæld kan hele den immunhistokemiske<br />
protokol (og ISH protokoller) automatiseres.<br />
Begge instrumenter har separat temperaturregulering<br />
af objektglas, hvilket gør såvel<br />
afparaffinering som epitopdemaskering mulig.<br />
Ulempen ved disse instrumenter er dels, at<br />
man mere eller mindre er bundet til at bruge<br />
Ventanas reagenser, hvilket betyder, at analyseprisen<br />
bliver noget højere end på de konkurrerende<br />
”åbne systemer”, dels har vanskeligere<br />
ved at optimere sine protokoller.<br />
TechMate500 er en helt anden type instrument.<br />
TechMate500, der i Europa tidl. blev<br />
forhandlet af DakoCytomation, virker efter<br />
kapillærprincippet (7). Dette system kræver,<br />
at vævssnit eller cytologisk materiale monteres<br />
på specielle ”capillary—gap” slides, og at<br />
man bruger specielle ”pads” (filtrerpapir) til<br />
at fjerne immunoreagenser fra kapillærrummet<br />
igen. Nødvendigheden af specielle glas<br />
og pads er med til at fordyre analysen på<br />
dette instrument. TechMate500 er i stand til<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 31<br />
samtidigt at håndtere 2-4 ”slideholders” med<br />
hver max. 60 glas. Farvningskapaciteten er<br />
med andre ord væsentlig højere på Tech-<br />
Mate500 end på de øvrige instrumenter.<br />
Hvilken immunostainer, et laboratorium bør<br />
vælge, hænger naturligvis sammen med laboratoriets<br />
størrelse og struktur, samt hvor<br />
mange og hvilke analyser maskinen dagligt<br />
skal udføre.<br />
<strong>2.</strong>8.4 Antistoftiter, inkubationstid og<br />
temperatur<br />
Den optimale antistoftiter (fortynding) er -<br />
foruden detektionssystemet (se afsn. <strong>2.</strong>10)<br />
og kromogenet (se afsn. <strong>2.</strong>11) - stærkt afhængig<br />
af inkubationstiden, samt af den<br />
temperatur hvorved inkubationen foregår.<br />
Mange laboratorier inkuberer 30-60 min ved<br />
stuetemperatur, nogle bruger 16-20 timer<br />
(natten over) ved 4° C. Der er en klar økonomisk<br />
fordel at inkubere længere end 30<br />
min, idet de fleste antistoffer kan fortyndes<br />
yderligere. Fortyndingen ved 30 min’s -<br />
inkubation kan multipliceres med 2-5 ved<br />
forøgelse af inkubationstiden til 1-2 timer, og<br />
med 4-10 ved 16 timers inkubation. Ydermere<br />
vil signal/støjforholdet, specielt for<br />
mange pAbs, forbedres betydeligt ved længere<br />
inkubation. Den yderligere fortynding af<br />
antistoffet nedsætter nemlig risikoen for<br />
uspecifik adhæsion til vævsproteiner. Endelig<br />
medfører en længere inkubationstid, at den<br />
variation i inkubationstiden, der nødvendigvis<br />
opstår ved manuel pådrypning af antistof, får<br />
relativt mindre betydning.<br />
Fordelen ved at anvende en relativt kort inkubationstid<br />
er naturligvis, at immunfarvningen<br />
kan færdiggøres hurtigere, ideelt samme<br />
dag som den er rekvireret. Da de fleste immunostainere<br />
samtidig fungerer bedst med<br />
inkubationstider på maksimalt 60 min, er det<br />
ikke overraskende, at de fleste diagnostiske<br />
rutinelaboratorier anvender inkubationstider<br />
på 30-60 min.<br />
Inkubationstider på væsentligt under 30 min.<br />
kan opnås ved at hæve inkubationstemperaturen<br />
til 37° C eller mere - ikke alene<br />
for det primære antistof, men også for visualiseringssystemet.<br />
Dette kan dog være forbundet<br />
med en større risiko for uspecifik<br />
baggrundsfarvning.<br />
Interessen for at nedsætte inkubationstiden<br />
til et minimum er tæt forbundet med ønsket<br />
om - i specielle tilfælde - at kunne supplere<br />
traditionel frysesnitsundersøgelse med immunhistokemi.<br />
Listen over haste<strong>teknik</strong>ker,<br />
der kan anvendes peroperativt, er forholdsvis<br />
lang. Blandt de mest interessante er klart<br />
metoderne fra Chilosi et al. (41) og Kämmerer<br />
et al. (83). Chilosi’s <strong>teknik</strong> er en simpel<br />
og hurtig ét steps metode, der bygger på<br />
anvendelsen af ”Enhanced Polymer One-step<br />
Staining” (EPOS, se afsn. <strong>2.</strong>10.1) reagenser<br />
og opvarmning i mikrobølgeovn. Teknikken<br />
Mogens Vyberg 2005<br />
Tabel <strong>2.</strong>3: Fortyndervæsker til primære<br />
antistoffer<br />
a. 1% BSA i 0,05 M tris-HCl-buffer pH 7,4 med<br />
0,15 M NaCl og 15 mM Na-azid.<br />
b. 1% BSA i 0,05 M tris-HCl-buffer pH 6,0 med<br />
15 mM Na-azid.<br />
c. 1% BSA i 0,05 M tris-HCl-buffer pH 8,6 med<br />
15 mM Na-azid.<br />
d. 1% BSA i 0,05 M tris-HCl-buffer pH 7,4 med<br />
0,50 M NaCl og 15 mM Na-azid.<br />
e. 0,5% Casein i 0,05 M tris-HCl-buffer pH 7,4 med<br />
0,15 M NaCl og 15 mM Na-azid.<br />
f. 1% BSA i 0,05 M tris-HCl-buffer pH 7,4 med<br />
0,075 M NaCl og 15 mM Na-azid.<br />
Detergent i form af Tween20, 0,05%-0,1% kan med<br />
fordel tilsættes.<br />
gør det muligt på frysesnit fx at skelne lymfomer<br />
fra lavt differentierede carcinomer ved<br />
hjælp af CD45- og CK-farvninger udført på<br />
under 10 min! Ulempen ved metoden er, at<br />
den i sagens natur kun kan udføres med primære<br />
antistoffer, der findes i EPOS format<br />
(kun ca. 30 forskellige primære antistoffer<br />
findes i EPOS format). Kämmerer et al.’s<br />
metode er en 2-lags EnVision+ baseret metode<br />
(se afsnit <strong>2.</strong>10.2) og dermed langt mere<br />
fleksibel, hvad angår valgt af primære antistoffer.<br />
Alle inkubationer foregår på varmeplade<br />
ved 37°C. Herved nedbringes den samlede<br />
farvetid til ca. 15 min. I forhold til Chilosis<br />
metode svarer dette dog til en forlængelse<br />
på ca. 5 min. Til gengæld er Kämmerers metode<br />
mere sensitiv (4) og pt det bedste bud<br />
på en peroperativ haste<strong>teknik</strong> (se Haste-<br />
EnVision+, afsnit <strong>2.</strong>10.2).<br />
Før et nyt antistof kan tages i brug, skal det<br />
titreres. En række forskellige fortyndinger af<br />
antistoffet skal afprøves i det detektionssystem,<br />
som antistoffet skal anvendes i.<br />
Normalt vil producenten anbefale, at antistoffet<br />
anvendes i en given fortynding (fx 1:10)<br />
eller indenfor et givet fortyndingsområde (fx<br />
1:10 - 1:40). Titreringen kan derfor med<br />
fordel tage udgangspunkt i producentens<br />
angivelser, men naturligvis omfatte både<br />
højere og - især - lavere koncentrationer af<br />
antistoffet. Da producentens angivelser oftest<br />
tager udgangspunkt i et “standard” visualiseringssystem,<br />
kan man, når man har optimereret<br />
sit system jfr. ovenstående regne<br />
med, at mange antistoffer skal benyttes i en<br />
fortynding, der er 5-50 x den oplyste! Når<br />
den primære titrering tager udgangspunkt i<br />
producentens anbefalinger, vil “dobbelt op”<br />
fortyndinger som oftest være tilstrækkelige<br />
(fx 1:10, 1:20, 1:40, 1:80 etc.). Er der ingen<br />
anbefalinger fra producenten, er det nødvendigt<br />
at afsøge et større koncentrationsområde<br />
og derfor også have større afstand mellem de<br />
enkelte fortyndinger. I stedet for “dobbelt op”<br />
fortyndinger kan fortyndingstrin på gange 4<br />
anvendes (fx 1:10, 1:40, 1:160, 1:640 ect.).
32 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
I anden omgang kan “dobbelt op” fortyndinger<br />
så anvendes omkring den fortynding, der<br />
i første omgang gav de bedste resultater.<br />
Den optimale titer for pAbs ligger normalt<br />
mellem 1:100 og 1:10.000. mAbs, der leveres<br />
som supernatantantistoffer, har oftest en<br />
titer på mellem 1:5 og 1:200, mens mAbs i<br />
form af ascitesvæske kan have en optimal<br />
titer på op til 1:1.000.000. “Rå” ascites-Abs<br />
er sjældent kommercielt tilgængelige, idet de<br />
normalt altid fra producentens side vil være<br />
fortyndet til en titer, der svarer til supernatant-antistofferne.<br />
<strong>2.</strong>8.5 Fortyndervæske<br />
Den væske/buffer, der anvendes til at fortynde<br />
antistofferne, har ikke blot til formål at<br />
regulere koncentrationen af antistoffet under<br />
inkubationen. Fortyndervæsken bør vælges<br />
således, at den besidder flere andre kvaliteter.<br />
Fortyndervæsken skal således have et<br />
passende pH og saltindhold, så risikoen for,<br />
at antistoffet adhærerer uspecifikt til<br />
vævsproteiner, er minimal, samtidig med at<br />
antistof-antigen reaktionen ikke påvirkes<br />
negativt. Fortyndervæsken bør ligeledes indeholde<br />
et såkaldt carrierprotein, der skal<br />
beskytte antistofopløsninger med lavt proteinindhold<br />
mod antistofpolymerisation og antistofadsorbtion<br />
til overfladen af reagensglas.<br />
Tilsætning af 1% BSA vil have denne beskyttende<br />
effekt på antistofopløsninger. Samtidig<br />
virker BSA som ”blocking protein” og vil<br />
dermed nedsætte risikoen for uspecifik antistofadhæsion<br />
via hydrofob interaktion. En<br />
god universal fortyndervæske er derfor buffer<br />
a (Tabel <strong>2.</strong>3). Den har i mange år været den<br />
foretrukne buffer til fortynding af både mAbs<br />
of pAbs. Nyere undersøgelser tyder dog på at<br />
buffere med neutralt pH som buffer a ikke<br />
nødvendigvis giver de bedste betingelser for<br />
mAbs. Boenisch (84,85) fandt i forsøg med<br />
14 forskellige mAbs, at de fleste - på HIERbehandlede<br />
paraffinsnit - gav de kraftigste<br />
reaktioner i Tris buffer ved pH 6,0 mens et<br />
enkelt (klon BLA.36, B-celle markør) gav de<br />
bedste resultater i Tris buffer ved pH 8,6.<br />
Boenisch fandt ligeledes at tilsætningen af<br />
0,15M NaCl svækkede reaktiviteten af en del<br />
af de testede mAbs.<br />
Konklusionen, Boenisch drog af sine arbejder,<br />
var bl.a.<br />
1. At PBS ikke bør anvendes som fortynderbuffer<br />
til mAbs.<br />
<strong>2.</strong> At buffer b ( 0,05M Tris pH 6,0) er mere<br />
velegnet som generel fortyndervæske til<br />
mAbs end buffer a.<br />
3. At optimeringen af brugen af et (nyt) mAb<br />
altid bør inkludere testning af minimum buffer<br />
a, b og c som fortynderbuffer.<br />
Forsøg i eget laboratorium har kun delvist<br />
kunne reproducere Boenischs fund. Vi finder<br />
(4) også at PBS generelt giver svagere reaktioner<br />
med en del mAbs, end TBS gør.<br />
Ligeledes ses pH og saltkoncentrationen i<br />
fortynderbuffer at påvirke immunreaktionerne,<br />
men hvor Boenisch kun noterer sig fordele<br />
ved manipulering af disse parametre, ser vi<br />
også væsentlig ulemper, der i mange tilfælde<br />
overskygger evt. fordele. Problemet med de<br />
radikale ændringer i pH og saltkoncentration<br />
som foreslået af Boenisch er, at langt de fleste<br />
antistoffer, vi har testet under disse forhold,<br />
giver tiltagende problemer med baggrundssværtning,<br />
hvilket vanskeliggør fortolkning<br />
af farvningsresultaterne. Årsagen til<br />
denne diskrepans er uklar. En del af forklaringen<br />
kan være, at Boenisch primært har<br />
benyttet sig af meget korte inkubationstider<br />
(10 min.), hvor vi har benyttet os af længere<br />
inkubationstider (60 min.). Ændringer i pH og<br />
saltkoncentration ændrer ladningsforholdene<br />
på såvel antistof som antigen. Målet er at<br />
genskabe det oprindelige forhold, hvor antigen<br />
og antistof oftest har modsat ladning.<br />
Herved vil elektrostatisk tiltrækning (ionbinding)<br />
i højere grad bidrage ved antistofantigen<br />
reaktionen. Elektrostatisk tiltrækning<br />
sikrer hurtigere binding af antistof til antigen,<br />
hvilket specielt ses tydeligt ved korte inkubationstider,<br />
omvendt vil uspecifik elektrostatisk<br />
tiltrækning til modsat ladede proteiner generelt<br />
favoriseres ved en forlænget inkubationstid.<br />
Bedre resultater er i rutinediagnostisk praksis<br />
opnået ved anvendelse af buffer f (4,89),<br />
hvor saltkoncentrationen i forhold til buffer a<br />
er halveret. Dette giver for mange mAbs lidt<br />
kraftigere reaktioner (mAbs kan ofte fortyndes<br />
lidt ekstra) uden problemer med baggrundssværtning.<br />
Buffer d og e er alternativer, der med fordel<br />
kan tages i anvendelse, hvis der arbejdes<br />
med Abs, der giver specielt mange problemer<br />
med uspecifik baggrundsfarvning. Bemærk,<br />
at Na-azid hæmmer peroxidase og derfor ikke<br />
må være tilstede i for høje koncentrationer i<br />
visualiseringens sidste lag.<br />
<strong>2.</strong>8.6 Opbevaring og holdbarhed af<br />
antistoffer<br />
De fleste antistofproducenter anbefaler at<br />
opbevare antistoffer ved 4°C eller -20°C. Da<br />
antistofopløsninger ikke tåler gentagende<br />
cykler af nedfrysning og optøning deles antistoffer,<br />
der skal opbevares ved -20°C i små<br />
portioner i fx eppendorf-rør. Holdbarheden af<br />
koncentrerede antistofopløsninger er generelt<br />
god. Opbevaret under de anbefalede betingelser<br />
er antistofferne holdbare i årevis. Specielt<br />
vil opbevaring ved -20°C eller ved -80°C<br />
betyde, at antistofferne kun taber minimalt i<br />
aktivitet over en lang årrække. Antistofkonjugater<br />
og fortyndede antistofopløsninger bør<br />
generelt opbevares ved 4°C. De fleste fortyndede<br />
antistoffer vil ved denne temperatur<br />
have en holdbarhed på adskillige måneder,<br />
forudsat at en passende bufferopløsning inkluderende<br />
15 mM Na-azid er anvendt til<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 33<br />
fortyndingen (Tabel <strong>2.</strong>3) I praksis betyder<br />
dette, at arbejdsopløsninger af mange antistoffer<br />
kan fremstilles i større mængder, fx<br />
hvad der svarer til 4-6 ugers forbrug.<br />
<strong>2.</strong>8.7 Kontrolprocedurer<br />
Den initiale afprøvning af et nyt antistof kan<br />
betragtes som en overordnet reagenskontrol.<br />
En kontrol, der i alle tilfælde er nødvendig<br />
for, at et givet antistof kan tages i anvendelse.<br />
Herefter kræver enhver immunhistokemisk<br />
analyse med det pågældende antistof en<br />
sideløbende kontrolprocedure, der kan vise,<br />
at et evt. negativt resultat skyldes fravær af<br />
antigen i det undersøgte præparat og ikke en<br />
fejl i analysen (falsk negativ reaktion). Kontrolproceduren<br />
skal ligeledes kunne vise, at<br />
et evt. positivt analyseresultat skyldes et<br />
reelt indhold af antigen og ikke krydsreagerende<br />
substanser, endogen enzymaktivitet,<br />
endogen biotin eller lignende (falsk<br />
positiv reaktion). En tilfredsstillende grad af<br />
kontrol på disse forhold opnås gennem:<br />
1. kontrolsnit med kendt positivt/negativt<br />
reaktionsmønster inkluderet i analysen<br />
<strong>2.</strong> substitution af det primære antistof på<br />
nabosnit med “non-immun” reagens.<br />
Ad 1) De bedste kontrolmuligheder opnås<br />
klart ved at anvende snit fra en multiblok.<br />
Multiblokken bør indeholde en række normalvæv<br />
og tumorvæv, der er præpareret som<br />
testpræparatet. Vævene til multiblokken bør<br />
endvidere vælges således, at antigenet forekommer<br />
i varierende koncentrationer. Inkluderes<br />
snit fra en “veldesignet” multiblok, vil<br />
det være muligt at vurdere antistoffets reaktionsmønster<br />
i den aktuelle analyse, samtidig<br />
med at sensitiviteten af analysen kan monitoreres.<br />
Kontrolsnit og testsnit monteres på<br />
samme glas!<br />
Ad 2) Der er flere muligheder for substitution<br />
af primært antistof:<br />
a. med primært antistof, der er absorberet<br />
med oprenset antigen<br />
b. med et andet irrelevant antistof<br />
c. med non-immun serum fra den samme<br />
dyre art hvori det primære antistof er rejst<br />
d. med fortynderbuffer.<br />
Den immunologisk mest korrekte substitutionskontrol<br />
er den første (a). Tilgængeligheden<br />
af (eller mangel på samme) og prisen på<br />
rene antigener gør dog denne form for kontrol<br />
urealistisk ved almindelige diagnostiske<br />
rutineundersøgelser. Den anden mulighed (b)<br />
for substitution er næsten altid tilstede ved<br />
diagnostiske undersøgelser, da der her traditionelt<br />
appliceres større eller mindre paneler<br />
af antistoffer rettet mod forskellige antigener.<br />
Substitution med fortynderbuffer (d) er simpel<br />
og altid mulig at udføre, og den gør det<br />
let at registrere<br />
Mogens Vyberg 2005<br />
reaktivitet, der kan tilskrives detektionssystemet<br />
og/eller kromogen/substratopløsningen<br />
(endogen enzymaktivitet,<br />
endogen biotin, krydsreaktivitet af sekundært<br />
antistof eller lignende).<br />
Vel vidende, at de beskrevne kontroller langt<br />
fra er fyldestgørende med hensyn til en præcis<br />
karakterisering af et antistofs specificitet<br />
(42), kan følgende kontrolforanstaltninger<br />
anbefales til sikring af den daglige kvalitet på<br />
de immunhistokemiske analyser:<br />
1. Der bruges kun primære antistoffer, der er<br />
procedureteknisk optimeret. Antistoffernes<br />
reaktivitet og specificitet skal være veldokomenteret<br />
og reproduceret i eget laboratorium.<br />
<strong>2.</strong> Snit monteres på glas med positive kontrolsnit<br />
(gerne fra multiblokke).<br />
3. Antistofundersøgelser bør altid laves som<br />
“panelundersøgelser”.<br />
4. Det primære antistof erstattes med fortynderbuffer<br />
på nabosnit til de snit, der<br />
skal immunfarves. Der skal medtages ét<br />
snit for hver demaskeringsprocedure.<br />
Vimentin kontrol<br />
På arkivmaterialer (paraffin), hvor kendskabet<br />
til fikseringstid og præparationsprotokolen<br />
i det hele taget er sparsomt, kan det være<br />
nyttigt at inkludere en såkaldt “vimentin<br />
kontrol” (43).<br />
Vimentin hører til de intermediære filamenter.<br />
Det findes i næsten alle mesenkymale<br />
celler. Påvisning af vimentin, der således<br />
findes stort set i alle væv, kan bruges til at<br />
vurdere graden af fikserings- og præparationsmæssige<br />
ændringer (maskering - evt.<br />
destruktion) af epitoper i et givet vævssnit. I<br />
praksis gøres dette ved at påvise vimentin<br />
ved hjælp af et mAb, klon V9, som detekterer<br />
en epitop på vimentin, der bl.a. er følsom<br />
overfor forlænget fikseringstid i formaldehyd.<br />
Det har vist sig, at mange epitoper på andre<br />
antigener viser fikserings- eller præparationsmæssigt<br />
betingede ændringer i antigenisiteten,<br />
der er analoge med ændringer i “V9<br />
epitopens” antigenisitet. Kvaliteten af farvningsresultaterne<br />
opnået med V9 kan derfor<br />
til en vis grad extrapoleres til andre antistoffer<br />
og dermed være til hjælp ved fortolkningen<br />
af farvningsresultaterne for disse. Betydningen<br />
af at inddrage en vimentin kontrol er<br />
dog aftaget i takt med udviklingen af HIER<br />
<strong>teknik</strong>ken. Demaskeringsproblemet er forskelligt<br />
for de antistoffer, der kræver proteolytisk<br />
forbehandling og dem, der kræver varmeforbehandling.<br />
<strong>2.</strong>9 Skylleprocedure<br />
Før applikation af detektionssystem skylles<br />
(“vaskes”) grundigt i buffer med henblik på at<br />
fjerne overskydende antistof.
34 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Figur <strong>2.</strong>8: Signaturforklaring til Fig. <strong>2.</strong>9-<strong>2.</strong>15<br />
<strong>2.</strong>9.1 Skyllebuffer<br />
TBS og PBS er de foretrukne skyllebuffere.<br />
Der er ikke beskrevet væsentlige kvalitative<br />
forskelle på disse to, men egne erfaringer<br />
(Aalborg) peger på TBS som den bedste. PBS<br />
bør undgås ved AP-baserede detektionssystemer,<br />
da phosphationer virker hæmmende<br />
på alkalisk phosphatase aktivitet.<br />
Azid-tilsætning til skyllebuffer og fortynderbuffer<br />
har været mistænkt for at hæmme<br />
peroxidaseaktivitet. Tilsætning af detergent<br />
til skyllebuffer anbefales af flere. På paraffinsnit<br />
vil tilsætning af Triton X-100 eller Tween<br />
20 i op til 1% nedsætte risikoen for uspecifik<br />
antistofadhæsion, samtidig med at penetrationen<br />
af immunreagenserne forbedres. Tilsætning<br />
af detergent til skyllebuffer er obligatorisk<br />
for immunostainere.<br />
<strong>2.</strong>9.2 Skylletid<br />
De fleste immunhistokemiske farvningsprotokoller<br />
opererer med skylletider mellem antistofinkubationerne<br />
på ialt 5 til 20 min. Meget<br />
tyder på, at selv ialt 5 min.’s skyl i flere hold<br />
Figur <strong>2.</strong>9: Direkte <strong>teknik</strong>.<br />
buffer er mere end tilstrækkelige til at undgå<br />
problemer med baggrundsfarvning. Brigati et<br />
al. (7) fandt, at 3 gange 30 sek. skyl med<br />
detergentholdig buffer er tilstrækkelig til at<br />
undgå misfarvning af glas og væv ved immunfarvning<br />
efter “kapillærkræfternes princip”,<br />
der anvendes i de automatiske immunostainer<br />
som TechMate og CodeOn. Det skal<br />
dog bemærkes, at skylletider på under 5 min.<br />
efter inkubation med polymerkonjugater bør<br />
undgås, da der er risiko for, dette vil efterlade<br />
overskydende konjugat i prøvematerialet.<br />
Da antigen-antistof bindingen er reversibel,<br />
bør ukritisk forlængelse af skylleproceduren<br />
(timer) undgås, specielt vis antistoffer med<br />
lav affinitet anvendes. Forsøg med forlængelse<br />
af skylleproceduren til 16 timer har vist en<br />
tydelig svækkelse af farvningsintensiteten i<br />
forhold til det normale 5 min. skyl (4).<br />
<strong>2.</strong>10 Detektionssystemer<br />
Teknikker til detektion at antigenbundet antistof<br />
kan principielt inddeles i de direkte og de<br />
indirekte <strong>teknik</strong>ker. Teknikkerne er illustreret<br />
i Figg. <strong>2.</strong>9 - <strong>2.</strong>15. Signaturforklaring til disse<br />
er givet i Fig. <strong>2.</strong>8.<br />
<strong>2.</strong>10.1 Direkte <strong>teknik</strong>ker<br />
I de direkte <strong>teknik</strong>ker (Fig. <strong>2.</strong>9) er det primære<br />
antistof direkte konjugeret til label<br />
(enzym eller fluorokrom). Detektion af antigenet<br />
kan derfor foregå via et enkelt step.<br />
Den type <strong>teknik</strong>ker er simple og hurtige at<br />
udføre, men ikke særlig sensitive. Traditionelle<br />
direkte immunenzymatiske <strong>teknik</strong>ker bruges<br />
stort set ikke længere. Direkte immunfluorescens<strong>teknik</strong>ker<br />
bruges til gengæld stadig i<br />
et vist omfang ved påvisning af immunglobulinaflejringer<br />
ved glomerulonefritis og<br />
bulløse hudlidelser. Den direkte immunflourescens<strong>teknik</strong><br />
er også indenfor immun-dobbeltfarvning<br />
meget anvendt, specielt i<br />
studier af co-lokalisation af to eller flere antigener<br />
i samme celle.<br />
Direkte polymerforstærknings<strong>teknik</strong><br />
Den direkte immunenzymatiske <strong>teknik</strong> har for<br />
nylig fået en renæssance gennem den såkaldte<br />
polymerforstærknings<strong>teknik</strong> lanceret af<br />
DakoCytomation under navnet EPOS (Enhanced<br />
Polymer Onestep Staining) (Fig. <strong>2.</strong>10).<br />
Systemet søger at løse de direkte <strong>teknik</strong>kers<br />
ringe sensitivitet gennem kobling af et større<br />
antal antistofmolekyler og peroxidase- eller<br />
phospatasemolekyler til den samme fleksible<br />
polymerforbindelse (dextran). Uden helt at nå<br />
de følsomme multistep-detektionssystemers<br />
sensitivitet har EPOS-<strong>teknik</strong>ken bragt den<br />
direkte immunenzymatiske <strong>teknik</strong> tilbage som<br />
et alternativ indenfor specielle applikationer.<br />
EPOS kan således på frysesnit i en 10 min’s<br />
<strong>teknik</strong> bruges til at skelne lymfomer (CD45+)<br />
fra carcinomer (CK+) (41).<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 35<br />
Figur <strong>2.</strong>10: Enhanced Polymer One-step Staining<br />
(EPOS).<br />
På baggrund af deres egen polymerteknologi<br />
har firmaet Zymed ligeledes udviklet en direkte<br />
<strong>teknik</strong>. Zymed anvender polypeptider<br />
som ”backbone” i deres polymer. P.t. har<br />
firmaet kun et produkt byggende på denne<br />
teknologi: ”Sentinel Lymph Node Rapid IHC<br />
Kit”, hvormed det er muligt at detektere cytokeratin<br />
i cryosnit på under 10 min. Se også<br />
nedenfor om indirekte polymerforstærknings<strong>teknik</strong>.<br />
<strong>2.</strong>10.2 Indirekte <strong>teknik</strong>ker<br />
Antallet af forskellige indirekte detektionssystemer<br />
er meget stort.<br />
Den drivende kraft for udviklingen af de<br />
mange modifikationer har været ønsket om<br />
at kombinere den specifikke detektion af antigenbundet<br />
primært antistof med en så stor<br />
amplifikation (forstærkning) af signalet som<br />
muligt. I dag findes således mange kommercielt<br />
tilgængelige, robuste og meget sensitive<br />
detektionsystemer. De vigtigste systemer er:<br />
a. 2- og 3-lags <strong>teknik</strong>ker<br />
b. Peroxidase anti-peroxidase (PAP) og Alkalisk<br />
phosphatase anti-alkalisk phosphatase<br />
(APAAP).<br />
c. Avidin-biotin systemer<br />
d. Polymerforstærknings<strong>teknik</strong>.<br />
e. Tyramid Signal Amplifikation (TSA).<br />
Figur <strong>2.</strong>11: Tolags<strong>teknik</strong> (A) og trelags<strong>teknik</strong> (B)<br />
Mogens Vyberg 2005<br />
Figur <strong>2.</strong>12: APAAP-<strong>teknik</strong> (A) og PAP-<strong>teknik</strong> (B).<br />
2- og 3-lags <strong>teknik</strong>ker<br />
2-lags <strong>teknik</strong>ken (Fig. <strong>2.</strong>11) er det simpleste<br />
indirekte detektionssystem. I denne <strong>teknik</strong><br />
inkubers først med umærket primært antistof,<br />
fulgt af sekundært antistof rettet mod<br />
immunglobulin fra den dyreart, hvorfra det<br />
primære antistof stammer (fx mus). Det sekundære<br />
antistof er konjugeret med den ønskede<br />
label: horse radish [=peberrod] peroxidase<br />
(HRP), alkalisk phosphatase (AP) eller<br />
lignende. En fordel ved dette system er, at<br />
det enzymkonjugerede sekundære antistof<br />
kan anvendes til detektion af alle primære<br />
antistoffer, der er produceret i den pågældende<br />
dyreart (mus). Da der til hvert primære<br />
antistofmolekyle vil kunne bindes flere<br />
sekundære antistofmolekyler, er dette system<br />
væsentlig mere sensitivt end det direkte<br />
system. Sensitiviteten kan yderligere forbedres,<br />
hvis der efter det sekundære antistof<br />
inkuberes med et tertiært antistof (3-lags<br />
<strong>teknik</strong>, se Fig. <strong>2.</strong>11) rettet mod immunglobulin<br />
fra dyrearten, der leverer det sekundære<br />
antistof (fx ged eller kanin).<br />
Peroxidase anti-peroxidase (PAP) og<br />
alkalisk phosphatase anti-alkalisk<br />
phosphatase (APAAP)<br />
PAP og APAAP benytter sig begge af præformerede,<br />
opløselige immunkomplekser dannet<br />
udfra en blanding af enzym (HRP eller AP) og<br />
antistof rettet mod det pågældende enzym<br />
(Fig. <strong>2.</strong>12). Det er vigtigt for begge <strong>teknik</strong>kerne,<br />
at antistoffet, der anvendes i immunkomplekset,<br />
er rejst i samme dyreart som det<br />
primære antistof, da det sekundære antistof<br />
(“link-antistof”) skal kunne binde de to sammen.<br />
Link-antistoffet skal nødvendigvis anvendes<br />
i overskud, således at det, efter binding<br />
til det primære antistof med den ene<br />
“Fab-arm”, har den anden “Fab-arm” fri til<br />
binding af antistoffet, der indgår i immunkomplekset.<br />
Protokol for APAAP med repeat<br />
1. Inkubation med primært museantistof.<br />
<strong>2.</strong> Skyl med TBS fra sprøjteflaske.<br />
3. Skyl i 2 hold TBS i alt 4 min.<br />
4. Inkubér med Rabbit anti-mouse Ig (DakoCytomation<br />
Z259) fortyndet 1:25 i 1%<br />
BSA/TBS med 15 mM Na-azid. Inkubationstid<br />
30 min.
36 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Figur <strong>2.</strong>13: ABC-<strong>teknik</strong> (A) og LSAB-<strong>teknik</strong> (B)<br />
5. Skyl med TBS fra sprøjteflaske.<br />
6. Skyl i 2 hold TBS i alt 4 min.<br />
7. Inkubér med APAAP-compleks (DakoCytomation<br />
D651) fortyndet 1:50 i 1% BSA/TBS<br />
med 15 mM Na-azid. Inkubationstid 30 min.<br />
8. Skyl med TBS fra sprøjteflaske.<br />
9. Skyl i 2 hold TBS i alt 4 min.<br />
10. Gentag step 4 til 9. Inkubationstider for<br />
antistofopløsningerne medsættes til 10 min.<br />
11. Fremkald AP-aktivitet med Fast Red TR, New<br />
Fuchsin eller BCIP-NBT.<br />
1<strong>2.</strong> Skyl, kernefarvning, dækglas.<br />
Avidin-biotin systemer<br />
Disse systemer bygger på den høje affinitet,<br />
avidin og streptavidin har for det lille protein<br />
biotin (Fig. <strong>2.</strong>13). (Stept-)avidin har 4 binding<br />
sites for biotin og binder molekylet med<br />
en styrke, der langt overgår den styrke, hvormed<br />
antigen og antistof bindes til hinanden.<br />
Avidin er et basisk glycoprotein, der findes i<br />
store mængder i æggehvide. Ved neutralt pH<br />
vil nativt avidin have en positiv ladning, der<br />
vil kunne tiltrækkes stærke negative ladninger<br />
i vævet. Der er ligeledes en risiko for, at<br />
oligosaccharidkæder i molekylet kan bindes<br />
til lectinlignende substanser i vævet. Disse<br />
forhold gør, at man i avidin-biotin systemer<br />
oftest benytter sig af kemisk modificeret avidin<br />
eller af streptavidin. Den kemiske modifikation<br />
af avidinet går ud på at regulere det<br />
isoelektriske punkt for molekylet til neutralområdet<br />
(pH 7), samtidig med at de fleste<br />
oligosaccharidkæder fraspaltes. Streptavidin<br />
besidder de samme kemiske egenskaber<br />
overfor biotin som avidin, men det savner<br />
indhold af oligosaccharidkæder, samtidig med<br />
at molekylet har et neutralt isoelektriske<br />
punkt. Disse egenskaber har gjort streptavidin<br />
til et populært alternativ til avidin i<br />
immunhistokemisk sammenhæng. Streptavidin<br />
udvindes af bakterien Streptomyces avidinii.<br />
Alle (strept)avidin-biotin <strong>teknik</strong>ker bygger<br />
sædvanligvis på anvendelsen af biotinylerede<br />
sekundære antistoffer. Det lille biotin<br />
molekyle (vitamin H) konjugeres i stort antal<br />
let og skånsomt til antistofmolekyler. For at<br />
forbedre (strept)avidinets mulighed for at<br />
binde biotin, konjugeres dette via en såkaldt<br />
“spacer-arm” til antistofmolekylet. Specielt 2<br />
varianter af (strept)avidin-biotin <strong>teknik</strong>kerne<br />
har vundet stor udbredning.<br />
Labelled (strept)avidin biotin<br />
Labelled (strept)avidin biotin (LSAB/LAB)<br />
(44) er en meget populær <strong>teknik</strong>, i hvilken<br />
(strept)avidinet er direkte konjugeret med<br />
label (Fig. <strong>2.</strong>13). Som label anvendes oftest<br />
HRP eller AP, men principielt kan alle typer<br />
labels anvendes. LSAB/LAB <strong>teknik</strong>kerne udmærker<br />
sig ved at være meget sensitive og<br />
forholdsvis billige og simple at udføre, hvorfor<br />
<strong>teknik</strong>ken på mange laboratorier er den foretrukne<br />
til rutinediagnostik. Eneste væsentlige<br />
ulempe ved systemet er problemerne med<br />
endogen biotin i visse væv. Ligesom med<br />
APAAP-<strong>teknik</strong>ken kan inkubationsproceduren<br />
repeteres. Dette kan være nyttigt, hvis et<br />
eller andet går galt i første runde med en<br />
svag eller falsk negativ reaktion til følge, eller<br />
hvis man generelt ønsker at forbedre sensitiviteten.<br />
Protokol LSAB-HRP. Universalmetode for primære<br />
antistoffer fra kanin og mus<br />
1. Inkubation med primært antistof (kanin eller<br />
mus)<br />
<strong>2.</strong> Skyl med TBS fra sprøjteflaske<br />
3. Skyl i 2 hold TBS i alt 4 min.<br />
4. Inkubation med blanding af biotinyleret ged<br />
anti-kanin Ig (DakoCytomation E432) og<br />
biotinyleret ged anti-mus Ig (DakoCytomation<br />
E433) E432 og E433 kan anvendes i fortynding<br />
1:100 -> 1:200 Antistofferne fortyndes<br />
i 1% BSA/TBS med 15 mM Na-azid.<br />
Inkubationstid 30 min.<br />
5. Skyl med TBS fra sprøjteflaske<br />
6. Skyl i 2 hold TBS i alt 4 min.<br />
7. Inkubation med HRP-conjugeret streptavidin<br />
(DakoCytomation P397) P397 fortyndes<br />
1:100 - 1:300 i TBS. Inkubationstid 30 min.<br />
8. Skyl i 2 hold TBS i alt 5 min.<br />
9. Fremkald HRP med Diaminobenzidin eller<br />
Aminoethylcarbazol.<br />
10. Skyl, kernefarvning, dækglas.<br />
Avidin-Biotin-Complex <strong>teknik</strong>ken (ABC)<br />
I ABC-<strong>teknik</strong>ken (45) appliceres et kompleks<br />
bestående af (strept)avidin og en biotinyleret<br />
label (HRP eller AP), indeholdende frie bindingssteder<br />
for biotin (Fig. <strong>2.</strong>13). Komplekset<br />
binder sig til biotinmolekyler på det sekundære<br />
antistof. Den præcise sammensætning og<br />
størrelse af komplekset kendes ikke. Hsu’s<br />
(45) originale <strong>teknik</strong> benytter sig af en molær<br />
ratio mellem avidin og biotin-HRP på 2:1,<br />
hvilket teoretisk giver et stort overskud af<br />
avidin i complekset. Ændringer i ratio påvirker<br />
metodens sensitivitet. Det meget sensitive<br />
kommercielle kit “Vector Elite ABC-Kit”<br />
anvender således en ratio på 1:1 (46). Elite<br />
ABC complekserne indeholder sandsynligvis<br />
flere labelmolekyler end det originale ABC-<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 37<br />
kompleks. En lovende ny modifikation på<br />
ABCsystemet er den såkaldte “StreptAvidin/reverse<br />
molar ratio ABC” (SA/rABC) (46).<br />
Teknikken benytter sig af komplekser med en<br />
omvendt (reverse) avidin biotin-HRP ratio. I<br />
praksis betyder dette, at complekset har et<br />
stort overskud af label og bindingssteder for<br />
avidin. For at få optimalt udbytte af komplekset<br />
inkuberes efter det biotinylerede sekundære<br />
antistof med streptavidin (SA). Med<br />
SA/rABC er opnået en væsentlig forbedring af<br />
sensitiviteten i forhold til den traditionelle<br />
ABC <strong>teknik</strong>. I ELISA assays er registreret en<br />
3-folds sensitivitetsforbedring. Lignende forbedringer<br />
er tillige opnået på semi-tynde<br />
plastsnit (46).<br />
Animal research kit (ARK) systemet<br />
Hovedparten af de kommercielle mAbs<br />
stammer fra mus. Dette er af stor betydning<br />
for dyreekperimentelle studier på mus. Skal<br />
immunhistokemiske studier foregå på denne<br />
type materiale vil man derfor ofte være nødsaget<br />
til at bruge primære museantistoffer.<br />
Anvendelsen af museantistoffer på musevæv<br />
stiller specielle krav til detektionssystemet.<br />
Traditionelle indirekte <strong>teknik</strong>ker, hvor sekundære<br />
antistoffer (biotinylerede, enzymkonjugerede<br />
eller lign.) rettet mod muse Ig<br />
indgår, kan i sagens natur ikke anvendes, da<br />
disse antistoffer binder sig lige effektivt til<br />
endogent muse Ig som til det primære museantistof.<br />
En løsning på dette problem kan<br />
være at benytte direkte <strong>teknik</strong>ker eller hapten-mærkede<br />
primære antistoffer (f.eks. FITC<br />
eller biotin). Ulempen ved direkte <strong>teknik</strong>ker<br />
er manglende følsomhed (med mindre EPOS<br />
anvendes), samt det faktum at kun ganske få<br />
primære antistoffer findes enzymkonjugerede.<br />
Langt flere primære antistoffer findes<br />
hapten-mærkede. Specielt FITC- og biotinmærkede<br />
antistoffer findes der en del af. Det<br />
er dog stadig sådan, at hovedparten af de<br />
primære antistoffer ikke kan findes i en hapten-mærket<br />
variant. Det er derfor nødvendigt<br />
selv at foretage biotinylering eller lign. Det er<br />
Fig <strong>2.</strong>14: EnVision <strong>teknik</strong><br />
Mogens Vyberg 2005<br />
dog ikke alle laboratorier, der råder over den<br />
nødvendige teknologi til på traditionel vis at<br />
biotinylere. Ydermere kræver den traditionelle<br />
biotinylering ofte mere primært antistof,<br />
end der måske er til rådighed. DakoCytomations<br />
ARK-system er derfor et fortrinligt alternativ.<br />
Systemet benytter sig af, hvad man<br />
kunne kalde, en immunologisk biotinylering.<br />
Biotinyleringen foregår i reagensglas ved at<br />
blande eget primært muse antistof med et<br />
overskud af biotinyleret Fab sekundært antistof<br />
(anti-mus Ig) fra ARK-kittet. Det sekundære<br />
biotinylerede anti-mus antistof binder<br />
sig til det primære antistof, som herved indirekte<br />
biotinyleres. Overskydende biotinyleret<br />
Fab sekundært antistof bindes efterfølgende<br />
ved at tilsætte muse serum Ig til opløsningen.<br />
Opløsningen er herefter klar til brug<br />
(inkubation). Denne biotinyleringens-metode<br />
stiller ikke store krav til mængden af primært<br />
antistof, men forudsætter kendskab til Igkoncentrationen<br />
af det primære antistof. ARK<br />
<strong>teknik</strong>ken består således af følgende trin:<br />
1. Biotinylering af primært antistof.<br />
<strong>2.</strong> Biotinyleret primært antistof appliceres på<br />
snit eller celler.<br />
3. Detektion af primært antistof vha. Strept-<br />
Avidin-HRP, efterfulgt af DABfremkaldning.<br />
ARK systemet udemærker sig ved stort set at<br />
eliminere problemet med endogent Ig i muse<br />
væv. I sammenligning (4) med alternative<br />
systemer som HistoMouse fra Zymed og MOM<br />
fra Vector giver ARK systemet klart det bedste<br />
signal/støjforhold.<br />
Indirekte polymerforstærknings<strong>teknik</strong><br />
EnVision<br />
EnVision (Fig. <strong>2.</strong>14) er en indirekte polymerforstærknings<strong>teknik</strong>.<br />
Den er udviklet af DakoCytomation<br />
og bygger - som EPOS systemet<br />
- på en nyudviklet polymerteknologi. I<br />
EnVision-systemet anvendes en fleksibel polymer<br />
(dextran), hvortil HRP eller AP og ged<br />
anti-mus og/eller ged anti-kanin immunglobuliner<br />
er koblet. Efter inkubation med primære<br />
antistoffer fra mus eller kaniner kan<br />
den efterfølgende detektion og amplifikation<br />
opnås gennem inkubation med denne mærkede<br />
polymer. Systemet er derfor meget<br />
enkelt og brugervenligt at arbejde med. Systemet<br />
har angiveligt en sensitivitet, der ligger<br />
på linje med mange kommercielle LSAB-<br />
og ABC-kits (47). Et nyt EnVision system, En-<br />
Vision+ blev lanceret i 1998. Systemets reaktivitet<br />
er blevet forbedret i forhold til det oprindelige<br />
system bl.a. gennem anvendelse af<br />
en blanding af dextran polymerer med forskellig<br />
molekylvægt. EnVision+ systemet er<br />
sammenlignet med en lang række detektionssystemer<br />
og fundet mere følsom end de<br />
fleste (64,65). Ofte kan de primære antistoffer<br />
fortyndes 2-4 gange mere ved anvendelse<br />
af EnVision+ sammenlignet med et traditio-
38 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
nelt non-kit LSAB system (64). I sammenligning<br />
med Vectors meget følsomme Elite ABC<br />
Kit er der med få undtagelser opnået identiske<br />
resultater hvad angår følsomhed (64).<br />
EnVision+ systemets store fordel er, at det<br />
udover at eliminere problemerne med endogen<br />
biotin også kombinerer høj følsomhed<br />
med nedsat assay-tid og reduceret håndtering.<br />
Den eneste væsentlige ulempe ved<br />
EnVision+ systemet synes at være prisen. På<br />
trods af den, i forhold til non-kit LSAB og Elite<br />
ABC, høje pris er systemet de senere år med<br />
rette blevet et meget populært detektionssystem<br />
inden for immunhistokemien. Erfaringer<br />
i eget laboratorium har kun været positive,<br />
med én undtagelse. EnVision+ systemet<br />
har givet problemer indenfor muskelpatologien.<br />
Immunhistokemien anvendes på muskelbiopsier<br />
i høj grad til at påvise normal eller<br />
aberrerende forekomst af en lang række muskelmembran<br />
relaterede antigener<br />
(dystrophiner, sarcoglycaner, lamininer mv.).<br />
Disse undersøgelser kan foretages både på<br />
cryosnit og paraffinsnit. Forsøg med 18 forskellige<br />
muskelmembran relaterede antigener<br />
viste, at EnVision+ på cryosnit i alle 18 tilfælde<br />
gav markant svagere reaktion i sammenligning<br />
med eget non-kit LSAB system. Dette<br />
var tilfældet uanset om snittene var ufikserede<br />
eller fikserede i acetone. På paraffinsnit af<br />
NBF fikseret muskel sås ligeledes de kraftigste<br />
reaktioner med LSAB systemet, men forskellen<br />
var generelt mere beskeden. Årsagen<br />
til dette fænomen skal sikkert søges i det<br />
faktum, at EnVision molekylerne er ganske<br />
store og muskelmembraner er meget tætte<br />
strukturer. Som konsekvens af den forholdsvis<br />
ringe følsomhed på muskelsnit, er EnVision+<br />
på dette område erstattet med Power-<br />
Vision+ (se nedenfor).<br />
Kämermerer et al. beskrev i 2001 (83) en<br />
speciel haste-variant af Envision+, der kan<br />
anvendes peroperativt på cryosnit. Den samlede<br />
farvetid for metoden er ca. 15 min. I<br />
modsætning til haste-metoder baseret på<br />
EPOS metoden er det her muligt at anvende<br />
alle primære kanin og muse antistoffer. Gennem<br />
brug af primære antistoffer i højere koncentrationer<br />
end normalt (2-10 x højere koncentrationer)<br />
og en generel inkubationstemperatur<br />
på 37°C lykkes det at opnå forbavsende<br />
høj følsomhed. Følsomheden er<br />
naturligvis lavere end hvis traditionel EnVision+<br />
protokol anvendes, men ikke voldsomt<br />
meget. I den originale protokol anvendes<br />
acetone fiksering i 1 min. efterfulgt af en kort<br />
tørring af snittene.<br />
En modificeret fikseringsprotokol (4, 92) har<br />
givet forbedret morfologisk og cytologisk<br />
bevarelse af såvel traditionelle cryosnit som<br />
CryoJane snit (se afsnit <strong>2.</strong>4.1), samtidig med<br />
at problemer med endogen peroxidaseaktivitet<br />
stort set er elimineret. Denne fikseringsprotokol<br />
benytter en kombination af fiksering<br />
i 4 % NBF i 2 min. efterfulgt af demaskering i<br />
TEG/TE-buffer ved 95° C i 30 sek. Den forbedrede<br />
morfologiske og cytologiske bevarelse<br />
af cryosnittene har specielt været<br />
tydelig på lymfatisk materiale (Sentinel Node<br />
mv.). Mange antistoffer synes at give kraftigere<br />
reaktioner efter denne kombinationsfiksering<br />
end efter acetone fiksering alene. På<br />
traditionelle cryosnit af meget kollagenrige<br />
væv som hud og mamma kan der desværre<br />
være en risiko for tab af snit. På CryoJane<br />
snit ses dette problem ikke, da vedhæftningen<br />
af snittene her er meget stærkere. For<br />
laboratorier, der ikke har CryoJane teknologien<br />
til rådighed, kan det således være nødvendigt<br />
– på nogle væv - at sænke temperaturen<br />
i TEG/TE-bufferen til 60° C. Herved<br />
bevares alle væv, men man får desværre ikke<br />
hæmmet den endogene peroxidaseaktivitet.<br />
Protokol EnVision+<br />
1. Inkubation med primært antistof (kanin eller<br />
mus). Inkubationtid 30-60 min.<br />
<strong>2.</strong> Skyl med TBS fra sprøjteflaske<br />
3. Skyl i 2 hold TBS i alt 4 min.<br />
4. Inkubation med peroxidasemærket ”Ready-to-use”<br />
EnVision+ polymer. Til primære<br />
kanin antistoffer anvendes DakoCytomation<br />
K4003. Til muse antistoffer anvendes DakoCytomation<br />
K4001. Inkubationstid 30 min.<br />
5. Skyl med TBS fra sprøjteflaske<br />
6. Skyl i 2 hold TBS i alt 4 min.<br />
7. Fremkald HRP med Diaminobenzidin eller Aminoethylcarbazol.<br />
8. Skyl, kernefarvning, dækglas.<br />
Protokol Haste-EnVision+<br />
1. Cryosnit skæres og monteres på SuperFrost<br />
Plus glas. Snit tørres minimum 60 sek.<br />
<strong>2.</strong> NBF 4% 2 min.<br />
3. Skyl i TBS 10 sek.<br />
4. TEG-buffer ved 95°C 30 sek.<br />
5. Skyl i TBS 10 sek.<br />
6. Primært antistof ved 37°C 3 min.<br />
7. Skyl i TBS 20 sek.<br />
8. EnVision+ (DakoCytomation K4001 eller<br />
K4003) ved 37°C 3 min.<br />
9. Skyl i TBS 20 sek.<br />
10. DAB+ (DakoCytomation K3468) ved 37°C 3<br />
min.<br />
11. Skyl i postevand 10 sek.<br />
1<strong>2.</strong> Dest. vand 5 sek.<br />
13. Mayers Hæmatoxylin 15 sek.<br />
14. Skyl i postevand ved ca. 42°C 30 sek.<br />
15. Dækglas monteres med Aquatex<br />
PowerVision/PowerVision+<br />
Firmaet ImmunoVision Technologies bragte i<br />
1999 et nyt 2-lags detektionssystem på markedet<br />
ved navn PowerVision. PowerVision<br />
tilhører som EnVision og EPOS polymerforstærknings<strong>teknik</strong>kerne.<br />
Hvor polymeren i<br />
EnVision er forholdsvis store dextran molekyler,<br />
benytter man sig i PowerVision af små<br />
såkaldte ”multifunktionelle polymeriserbare<br />
molekyler”, muligvis acrylsyre, biacrylsyre eller<br />
disses derivater, til at skabe nogle mere<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 39<br />
Fig <strong>2.</strong>15: PowerVision <strong>teknik</strong><br />
kompakte polymerer, hvori der indgår enzymmolekyler<br />
(HRP) og link-antistofmolekyler<br />
i en passende ratio (mange enzymmolekyler<br />
pr. link-antistof) (Fig <strong>2.</strong>15).<br />
I teorien skulle disse meget kompakte polymerer<br />
eliminere de steriske og penetrationsmæssige<br />
problemer, som polymerforstærkningssystemerne<br />
ellers kan være forbundet<br />
med (78).<br />
Shi et al testede systemet og sammenlignede<br />
det med 3 kommercielle avidin-biotin baserede<br />
3-lags metoder (men ikke med EnVision!)<br />
(78). PowerVision viste sig at være meget<br />
mere følsom (faktor 4-8 med hensyn til fortynding<br />
af primære antistof) end de øvrige<br />
systemer. I direkte sammenligning med EnVision+<br />
synes PowerVision en smule mere følsom<br />
i detektionen af kerneantigener, mens<br />
EnVision+ er en smule mere effektiv i detektionen<br />
af membran- og cytoplasmatiske antigener<br />
(4). I 2002 blev en forbedret udgave af<br />
systemet lanceret, det såkaldte PowerVision+<br />
kit (Fig. <strong>2.</strong>16). I plus-versionen er sensitiviteten<br />
væsentlig forbedret for detektionen af<br />
primære museantistoffer. Den forbedrede<br />
sensitivitet opnås gennem inkubation med en<br />
såkaldt ”Post Antibody Block”, der i praksis er<br />
et sekundært link antistof (kanin anti-mus<br />
Ig). Inkubationstiden i ”Post Antibody Block”<br />
er 20 min. PowerVision+ må derfor nu betragtes<br />
som en 3-lags polymerforstærknings<strong>teknik</strong>.<br />
I sammenligning med 2-lags polymerforstærknings<strong>teknik</strong>kerne<br />
EnVision+ (Dako-<br />
Cytomation), MACH2 (BioCare) og Picture<br />
(Zymed). giver PowerVision+ med alle testede<br />
mAbs klart de kraftigste reaktioner. I forhold<br />
til EnVision+ giver PowerVision+ en sensitivitetsforbedring,<br />
der målt på fortynding af<br />
primært antistof ligger på en faktor 2-8<br />
(4,90). Et lignende 3-lags polymer system<br />
blev lanceret af BioGenex i 2003. Dette system<br />
går under betegnelsen: ”Super Sensitive<br />
Non-Biotin HRP Detektion System” og er<br />
hvad angår følsomhed på højde med Power-<br />
Vision+ (4).<br />
Mogens Vyberg 2005<br />
Fig <strong>2.</strong>16: PowerVision+ <strong>teknik</strong><br />
En general ulempe ved alle 3-lags polymer<strong>teknik</strong>kerne<br />
er naturligvis den forlængede<br />
analysetid på ca. 25 min. i forhold til 2-lags<br />
<strong>teknik</strong>kerne.<br />
Protokol PowerVision+<br />
1. Inkubation med primært antistof (kanin eller<br />
mus) Inkubationtid 30-60 min.<br />
<strong>2.</strong> Skyl med TBS fra sprøjteflaske<br />
3. Skyl i 2 hold TBS i alt 4 min.<br />
4. Inkubation med ”Post-antibody Blocking”.<br />
inkubationstid 20 min.<br />
5. Skyl med TBS fra sprøjteflaske<br />
6. Skyl i 2 hold TBS i alt 4 min.<br />
7. Inkubation med Poly-HRP anti-Mus/Kanin<br />
IgG Inkubationstid 30 min.<br />
8. Skyl med TBS fra sprøjteflaske<br />
9. Skyl i 2 hold TBS i alt 4 min.<br />
10. Fremkald HRP med Diaminobenzidin eller<br />
Aminoethylcarbazol.<br />
11. Skyl, kernefarvning, dækglas.<br />
Figur <strong>2.</strong>17: Tyramid signal amplifikations-<strong>teknik</strong>.
40 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
Advance<br />
“Advance” er DakoCytomations svar på konkurrenternes<br />
meget følsomme 3-lags polymer<br />
systemer. Advance er en 3-lags <strong>teknik</strong> byggende<br />
på DakoCytomations egen dextran<br />
teknologi. Advance matcher de øvrige 3-lags<br />
polymer <strong>teknik</strong>ker, hvad angår sensitivitet<br />
ved anvendelse af mAbs (4), men er mere<br />
følsom ved anvendelse af pAbs.<br />
Tyramid signal amplifikation<br />
Tyramid signal amplifikation (TSA) (Fig. <strong>2.</strong>17)<br />
er i sig selv ikke et egentligt detektionssystem,<br />
men derimod et uhyre effektiv metode<br />
til at forstærke alle HRP-baserede detektionssystemer.<br />
Metoden er første gang beskrevet<br />
af Bobrow et al. i 1989 (48) til solid-phase<br />
immunoassays. Bobrow kaldte sin<br />
originale metode for “catalyzed reporter deposition”<br />
(CARD). Siden har modifikationer af<br />
metoden fået mange forskellige betegnelser.<br />
Blandt disse er TSA, som i dag nok er den<br />
mest anvendte. Adams (54) modificerede i<br />
1992 den oprindelige metode med henblik på<br />
brug ved immunhistokemiske <strong>teknik</strong>ker. Teknikken<br />
benytter sig af HRP’s evne til oxidativ<br />
kondensering, herunder specielt dimerisering,<br />
af phenolforbindelser gennem en fri radikal<br />
mekanisme.<br />
Efter en traditionel peroxidase<strong>teknik</strong> (fx<br />
LSAB) inkuberes med biotinyleret tyramid<br />
(phenolforbindelse) og brintperoxid. HRP i det<br />
vævsbundne immunkompleks katalyserer<br />
aktiveringen af tyramidet (til et fri radikal).<br />
Passende fortynding af det biotinylerede tyramid<br />
gør, at det frie radikal mellemprodukt<br />
vil bindes til elektronrige aminosyreradikaler<br />
(tyrosin, tryptophan, phenylanalin mv.) fremfor<br />
at dimerisere. Da det frie radikal er uhyre<br />
reaktivt, vil reaktionen foregå i umiddelbar<br />
nærhed af katalysatoren HRP. Man opnår<br />
med andre ord, at store mængder biotin - via<br />
tyramidet – bindes covalent til vævsproteiner<br />
i nærheden af det antigen, der undersøges.<br />
Biotinet kan herefter påvises på normal vis<br />
ved hjælp af fx HRP-konjugeret streptavidin.<br />
Alt i alt forlænges den samlede farvetid med<br />
ca. 45 min. ved at anvende TSA <strong>teknik</strong>ken, til<br />
gengæld forbedres sensitiviteten dramatisk.<br />
Merz et al. (49) beskriver, at sensitiviteten<br />
forbedres så voldsomt, at primære antistoffer<br />
kan fortyndes 500-1000 gange mere og stadig<br />
give identiske resultater sammenlignet<br />
med en standard ABC-<strong>teknik</strong>. Nyere undersøgelser<br />
(4,66,67) bekræfter metodens kolossale<br />
følsomhed, omend 500-1000 folds fortyndinger<br />
af primære antistoffer hører til<br />
sjældenhederne. Mere end 100 antistoffer er<br />
blevet afprøvet, de fleste kan fortyndes 5 til<br />
50 gange yderligere i TSA-systemet og stadig<br />
give identiske eller bedre resultater end standard<strong>teknik</strong>ker<br />
som LSAB og ABC. Tillige er en<br />
række antistoffer, der ikke tidligere er beskrevet<br />
til paraffinsnit, med TSA<strong>teknik</strong>ken<br />
fundet brugbare (fx anti-CD6, klon ST23; anti-CD7,<br />
klon IOT7; anti-CD9, klon P-1/33;<br />
anti-CD11a, klon MHM24; anti-CD16, klon<br />
DJ130; anti-CD22, klon 4KB128; anti-CD23,<br />
klon MHM6; anti-CD33, klon WM54; anti-CD68,<br />
klon T-1/82a; anti-E-cadherin, klon<br />
36).<br />
Der er set en ganske stor variation i effekten<br />
af forstærkningen for de forskellige antistoffer<br />
(67) Anti-EBV-LMP, klon C1-4 kan således<br />
fortyndes 500 gange ekstra i TSA-systemet,<br />
mens anti-CD41, klon 5B12 kun kan fortyndes<br />
2,5 gange. Årsagen til de store forskelle<br />
hænger muligvis sammen med forskelle i det<br />
kemiske “mikromiljø”, der omgiver de enkelte<br />
epitoper (67). Bindingen af aktiveret tyramid<br />
til vævet kræver forekomst af elektronrige<br />
substanser som bl.a. tyrosin- og tryptophan-<br />
-aminosyreradikaler. Variationer i forekomsten<br />
af disse substanser formodes at påvirke<br />
effektiviteten af tyramid amplifikationen.<br />
TSA-teknologien udnyttes af 2 kommercielle<br />
kits. Catalyzed Signal Amplifikation (CSA) fra<br />
DakoCytomation og TSA fra NEN Life Science.<br />
Begge kit er relativt dyre. I forhold til non-kit<br />
LSAB skal beregnes 8-10 kr ekstra pr. glas.<br />
En væsentlig billigere løsning er at biotinylere<br />
tyramidet selv. Følges Adams’ (54) simple<br />
anvisninger, kan der for ca. 1500 kr fremstilles<br />
biotinyleret tyramid nok til ca. 10.000<br />
snit!<br />
NEN Life Science producerer foruden biotinyleret<br />
tyramid også en række fluorochromkonjugerede<br />
tyramid varianter. Med anvendelse<br />
af henholdvis fluorescein-, tetramethylrhodamine-,<br />
coumarin-, eller cyanin3-konjugeret<br />
tyramid istedet for biotinyleret tyramid kan<br />
opnås meget intens fluororescens. Fluororescens-TSA<br />
er langt mere følsom end fx en<br />
LSAB baseret fluororescens<strong>teknik</strong>. Primære<br />
antistoffer vil kunne fortyndes 5-20 gange<br />
mere.<br />
TSA protokol<br />
NEN’s TSA-Indirect-kit i kombination med et<br />
velfungerende non-kit LSAB system, danner<br />
basis for nedenstående protokol for paraffinsnit.<br />
Afparaffinering, hydrering og epitop<br />
demaskering foretages som sædvanlig, hvorefter<br />
metoden er:<br />
1. Blokering af endogen biotin med DakoCytomation<br />
Kit X0590<br />
<strong>2.</strong> Skyl med 0,05% Tween20 i TBS (TBST) 3<br />
hold i alt 6 min.<br />
3. Inkubation med 0,5% Blocking Reagent i<br />
TBS (TNB-buffer) 25 min.<br />
4. Inkubation med primært antistof fortyndet i<br />
TNB-buffer.<br />
5. Skyl med TBST fra sprøjteflaske<br />
6. Skyl i 3 hold TBST i alt 9 min.<br />
7. Inkubation med biotinyleret sekundært antistof.<br />
Til primære kanin antistoffer anvendes<br />
biotinyleret ged anti-kanin Ig (DakoCytomation<br />
E432) og til primære muse antistoffer<br />
biotinyleret ged anti-mus Ig (DakoCytomation<br />
E433). Begge antistoffer fortyndes<br />
1:200 i TNB-buffer. Inkubationstid 30 min.<br />
8. Skyl med TBST fra sprøjteflaske<br />
9. Skyl i 3 hold TBST i alt 9 min.<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 41<br />
10. Blokering af endogen peroxidaseaktivitet.<br />
Inkubation med ChemMate Peroxidase<br />
Blocking Solution (DakoCytomation S2023)<br />
10 min.<br />
11. Skyl med TBST fra sprøjteflaske<br />
1<strong>2.</strong> Skyl i 3 hold TBST i alt 9 min.<br />
13. Inkubation med HRP-konjugeret streptavidin<br />
(DakoCytomation P397) P397 fortyndes<br />
1:300 i TNB-buffer. Inkubationstid 30 min.<br />
14. Skyl med TBST fra sprøjteflaske<br />
15. Skyl i 3 hold TBST i alt 9 min.<br />
16. Inkubation med Biotinyleret Tyramid fortyndet<br />
1:50 i “Amplification Diluent”. Inkubationstid<br />
5-10 min.<br />
17. Skyl med TBST fra sprøjteflaske<br />
18. Skyl i 3 hold TBST i alt 9 min.<br />
19. Inkubation med HRP-konjugeret streptavidin<br />
(DakoCytomation P397) P397 fortyndes<br />
1:300 i TNB-buffer. Inkubationstid 30 min.<br />
20. Skyl med TBST fra sprøjteflaske<br />
21. Skyl i 3 hold TBST i alt 9 min.<br />
2<strong>2.</strong> Skyl i TBS 2 min.<br />
23. Fremkald HRP med Diaminobenzidin eller<br />
Aminoethylcarbazol.<br />
24. Skyl, kernefarvning, dækglas.<br />
Modifikation med hjemmelavet biotinyleret<br />
tyramid - efter Adams (54).<br />
40 ml boratbuffer, 50mM, pH 8,0 tilsættes under<br />
omrøring 100 mg Sulfo-NHS-LC-Biotin (Pierce<br />
21335). Herefter tilsættes 31,2 mg Tyramine Hydrochlorid<br />
(Sigma T2879). Opløsningen omrørres<br />
natten over. Opløsningen bliver tiltagende mælket<br />
og viskøs. Næste dag filtreres opløsningen gennem<br />
0,45µm syringe filter. Opløsningen opbevares i<br />
Eppendorf- eller Nunc-rør ved -80°C. Før brug<br />
optøs stamopløsningen og fortyndes 1:100 (1:50 -<br />
1:200) i 50mM TBS, pH 8,0 indeholdende 0,0005 -<br />
0,001% brintperoxid.<br />
Blocking reagent fra NEN-kittet kan ligeledes<br />
erstattes uden konsekvens for kvaliteten.<br />
Casein (Sigma C-5890) er en fuldgod og billig<br />
erstatning.<br />
DakoCytomation Kit til blokering af endogen<br />
biotin kan erstattes af Miller’s (63) protokol,<br />
der er mindst ligeså effektiv. Med hensyn til<br />
blokering af endogen biotin er det dog værd<br />
at bemærke, at ingen af de 2 protokoller er i<br />
stand til at blokere den endogene biotin forekomst<br />
100% ved TSA <strong>teknik</strong>ken. Der vil som<br />
regel restere en smule reaktion i de mest<br />
biotinrige væv som nyre, lever og binyre.<br />
Denne reaktion vil kun sjældent give fortolkningsmæssige<br />
problemer. Udelades blokeringen<br />
af endogen biotin vil mange normalvæv<br />
og tumorvæv til gengæld give en voldsom<br />
baggrundsfarvning, der vil vanskeliggøre<br />
identifikation og fortolkning af den specifikke<br />
immunreaktion.<br />
Mogens Vyberg 2005<br />
TSA-Plus<br />
Problemer med endogent biotin kan i TSA<br />
systemet nu helt undgås ved at anvende det<br />
såkaldte TSA Plus kit (NEN Life Science).<br />
Dette system baserer amplifikationen på<br />
DNP-tyramid og anti-DNP antistoffer. Systemet<br />
er således helt biotin-frit, hvorved blokering<br />
af endogent biotin helt kan undgås. Systemet<br />
er oprindeligt udviklet til In Situ Hybridisering,<br />
men kan med fordel anvendes til<br />
IHC, hvor det ifølge fabrikanten leverer en<br />
højere sensitivitet end den traditionelle TSA<br />
<strong>teknik</strong>. Et lignende biotin-frit system fås hos<br />
DakoCytomation under navnet CSA-II. Tyramidet<br />
er her mærket med FITC. DakoCytomation<br />
anbefaler CSA-II til immunhistokemi<br />
med mAbs.<br />
<strong>2.</strong>11 Kromogen/substratopløsning<br />
<strong>2.</strong>11.1 Horse radish peroxidase<br />
Indenfor immunhistokemien er horse radish<br />
peroxidase (HRP, horse radish = peberrod)<br />
den foretrukne enzymlabel. HRP er i sig selv<br />
usynlig, men kan visualiseres gennem flere<br />
simple histokemiske <strong>teknik</strong>ker anvendende<br />
brintperoxid som substrat og adskellige forskellige<br />
kromogener. Blandt kromogenerne<br />
skiller 3-Amino-9Ethyl-Carbazol (AEC) og<br />
3,3’-Diaminobenzidin (DAB) sig klart ud som<br />
de foretrukne.<br />
Protokoller til visualisering af horse radish<br />
peroxidase (HRP) aktivitet<br />
a. AEC protokol:<br />
AEC 0,8% i acetone 10 ml<br />
Acetatbuffer 0,05 M pH 5,0 200 ml<br />
30% H2O2 100 µl<br />
Opløsningen filtreres før brug. Inkubationstid: 20<br />
min. Opløsningen kan genbruges flere gange inden<br />
for 60 min. AEC stamopløsning (0,8% AEC i acetone)<br />
er holdbar minimum 1 mdr. ved stuetemperatur.<br />
b. DAB protokol:<br />
Diaminobenzidin 50 mg<br />
TBS 0,05M, pH 7,4 100 ml<br />
30% H2O2<br />
50 µl<br />
Opløsningen filtreres før brug. Inkubationstid:<br />
10 min. Opløsningen kan genbruges flere<br />
gange inden for 60 min. For at undgå gentagne<br />
afvejninger af DAB-pulver, der er under<br />
mistanke for at være carcinogent, kan man<br />
anvende DAB-tabletter (fx DakoCytomation<br />
S3000). Desværre er det en ret kostbar løsning.<br />
Langt billigere er det at købe 5 g (på<br />
forhånd afvejet) DAB og opløse det hele på<br />
én gang i 100 ml dest. vand. Herved fremkommer<br />
en x100 koncentreret stamopløsning,<br />
der opbevares ved - 20°C i passende<br />
små portioner (fx 1 ml). Stamopløsningen<br />
kan så efter optøning fortyndes 1:100<br />
i buffer og tilsættes brintperoxid (se også<br />
nedenfor om kommercielle kit til HRP påvisning).
42 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
AEC og DAB fungerer som elektrondonor i<br />
den enzymkatalyserede omsætning af brintperoxid.<br />
Begge oxideres til farvede tungtopløselige<br />
produkter. AEC giver et brillant rødbrunt<br />
reaktionsprodukt, der er opløseligt i<br />
alkohol. AEC-fremkaldte præparater kræver<br />
derfor montering med hydrofile monteringsmidler.<br />
Præparater fremkaldt med AEC bør<br />
opbevares mørkt, da stærk lyspåvirkning kan<br />
få reaktionsproduktet til at blege (“fade”) i<br />
intensitet.<br />
DAB giver et brunt reaktionsprodukt, der er<br />
uopløseligt i alkohol og andre organiske opløsningsmidler.<br />
Sensitiviteten af de 2 protokoller<br />
er i flere arbejder blevet sammenlignet.<br />
De Jong et al (50) fandt, at de 2 protokoller<br />
var lige sensitive. Scopsi og Larsson (51)<br />
fandt derimod, at DAB var en smule mere<br />
sensitiv end AEC. En væsentlig fordel ved<br />
DAB er dog, at sensitiviteten med forholdsvis<br />
enkle midler kan forbedres betydeligt. Blandt<br />
mange forskellige protokoller kan specielt 3<br />
meget simple og meget reproducerbare <strong>teknik</strong>ker<br />
anbefales.<br />
Protokoller til forstærkede DAB reaktioner<br />
c. DAB/imidazol (0,1M) protokol:<br />
Imidazol 700 mg<br />
TBS, pH 7,4 100 ml<br />
pH justeres til 7,4 med 1N HCl<br />
Diaminobenzidin 50 ml<br />
30% H2O2<br />
35 µl<br />
Opløsningen filtreres før brug. Inkubationstid: 5-10<br />
min. Opløsningen kan genbruges flere gange inden<br />
for 60 min. 0,1M imidazol i TBS er holdbar 1 mdr.<br />
ved stuetemperatur.<br />
d. DAB-Nikkel protokol:<br />
Diaminobenzidin 50 mg<br />
Acetatbuffer 0,1M, pH 6,0 100 ml<br />
Nikkelsulfat 0,8 g<br />
30% H2O2<br />
35 µl<br />
DAB opløses først, dernæst nikkelsulfat.<br />
Opløsningen filtreres før brug. Inkubationstid: 10<br />
min. Opløsningen kan genbruges flere gange inden<br />
for 60 min.<br />
DAB/nikkel fremkaldning giver et intenst blåsort<br />
reaktionsprodukt, der er uopløseligt i<br />
alkohol og xylen. Den blåsorte farve gør, at<br />
DAB/nikkel protokollen med fordel kan anvendes<br />
i dobbeltfarvningsprotokoller. I den<br />
forbindelse er det dog vigtigt at bemærke, at<br />
reaktionsproduktet efter DAB/nikkel bleger<br />
meget hurtigt i præparater, der er monteret<br />
med hydrofile monteringsmidler som fx AquaTex<br />
og AquaMount.<br />
e. Kobbersulfat (0,5%) protokol:<br />
Kobbersulfat 0,5 g<br />
PBS, TBS eller fysiologisk saltvand 100 ml<br />
Efter fremkaldning med DAB eller DAB/imidazol<br />
protokol kan yderligere forstærkning<br />
opnås ved at inkubere 5-10 min. i 0,5% kobbersulfat.<br />
Det originale DAB reaktionsprodukt<br />
bliver herved mørkere og mere intens i farven.<br />
Specielt kombinationen af DAB/imidazol<br />
protokollen og kobbersulfat efterbehandling<br />
kan pga af sin enkelhed og forbedrede sensitivitet<br />
anbefales. Kobbersulfat kan genbruges<br />
flere dage.<br />
Kommercielle kits til HRP påvisning<br />
På det kommercielle marked findes mange<br />
udmærkede og brugervenlige 2-komponent<br />
og endog enkelte “Ready-to-use”<br />
1-komponent kits af både DAB og AEC.<br />
Blandt de kommercielle DAB kits skal fremhæves<br />
den fra KemEnTec (4170) og DakoCytomations<br />
DAB+ (K3468). Begge kits kan<br />
med fordel kombineres med efterbehandling i<br />
kobbersulfat.<br />
For AEC’s vedkommende synes det med kits<br />
muligt at opnå en vis sensitivitetsforbedring i<br />
forhold til en standard AEC protokol. DakoCytomation’s<br />
“Ready-to-use” AEC+ (K3469)<br />
giver således en sensitivitetsforbedring, der<br />
svarer til en fortyndingsfaktor på ca. 2 for de<br />
de primære antistoffer. Prisen på de fleste<br />
kits udelukker desværre muligheden for “immersions-inkubation”<br />
i farveskåle, inkubationen<br />
må i stedet foretages som en mere arbejdskrævende<br />
“dråbeinkubation” på hvert<br />
enkelt glas.<br />
NovaRed<br />
Firmaet Vector, der primært har specialiseret<br />
sig indenfor detektionssystemer og chromogen/substrat<br />
kits, lancerede i 1999 et nyt<br />
følsomt kit til HRP påvisning. Systemet hedder<br />
Vector NovaRed. NovaRed giver et rødbrunt<br />
reaktionsprodukt, lidt mørkere end<br />
AECs reaktionsprodukt. Snit fremkaldt med<br />
NovaRed kan dehydreres og monteres med<br />
hydrofobe monteringsmidler som PerTex,<br />
VectaMount eller lignende. Til gengæld er<br />
reaktionsproduktet ikke stabilt i det hydrofile<br />
monteringsmiddel, AquaTex.<br />
NovaRed matcher den kobbersulfat-forstærkede<br />
DAB/imidazol protokol, hvad<br />
angår følsomhed (4). NovaRed er derfor et<br />
glimrende tilbud til dem, der ønsker et<br />
HRP-chromogen i “AEC-farve” men med en<br />
følsomhed og monteringsegenskaber som de<br />
bedste DAB protokoller. I forhold til andre<br />
kommercielle kits er prisen rimelig. 1 ml arbejdsopløsning<br />
koster ca. 3 kr. DakoCytomations<br />
DAB+ (K3468) koster til sammenligning<br />
næsten det dobbelte!<br />
<strong>2.</strong>11.2 Alkalisk phosphatase<br />
Indenfor hæmatologien er alkalisk phosphatase<br />
(AP) et vigtigt alternativ til HRP som<br />
enzymlabel. Påvisning af AP-aktivitet kan<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 43<br />
opnås gennem flere forskellige og velfungerende<br />
histokemiske <strong>teknik</strong>ker. To principielt<br />
forskellige <strong>teknik</strong>ker anvendes i de fleste<br />
tilfælde.<br />
Den ene <strong>teknik</strong> er den såkaldte simultankoblingsreaktion,<br />
hvor AP katalyserer fraspaltningen<br />
af phosphat fra en naphtholphosphatesterforbindelse.<br />
Efter fraspaltning kobler<br />
naphtholforbindelsen til diazoniumforbindelser<br />
(kromogen), der er tilsat substratopløsningen.<br />
Koblingsproduktet er farvet og tungtopløseligt<br />
i vandige medier. Specielt 2 simultan-koblingsreaktioner,<br />
der hver for sig benytter<br />
sig af forskellige kromogen-substrat<br />
kombinationer, kan på grund af deres sensitivitet<br />
og reproducerbarhed anbefales. Det<br />
drejer sig om Fast Red TR/Naphthol-AS-MX<br />
Phosphat (“Fast Red TR”) og New Fuchsin/Naphthol-AS-BI<br />
Phosphat (“New Fuchsin”).<br />
Den anden <strong>teknik</strong> til påvisning af AP er den<br />
såkaldte Indoxyl-Tetrazolium <strong>teknik</strong>, hvor AP<br />
katalyserer fraspaltningen af phosphat fra en<br />
indoxylphosphatester. Den frie indolyl-forbindelse<br />
er herefter i stand til at reducere<br />
tetrazoliumsalte, der herved udfældes i vævet<br />
som farvede og tungtopløselige formazaner.<br />
Til denne type <strong>teknik</strong>ker hører Bromo-Chloro-Indoxyl-Phosphat/Nitro<br />
B Tetrazolium<br />
(BCIP-NBT) metoden (50) BCIP-NBT er<br />
en sensitiv metode, men på trods af dette<br />
ikke særlig udbredt inden for immunhistokemien.<br />
BCIP-NBT giver et intenst blåsort granulært<br />
reaktionsprodukt, der er stabilt i etanol<br />
og xylen. BCIP-NBT substratopløsningen<br />
udmærker sig ved at være mere stabil end<br />
Fast Red TR og New Fuchsin opløsningerne,<br />
hvilket gør det muligt at forlænge inkubationstiden<br />
betydeligt. I visse in situ hybridiserings-<strong>teknik</strong>ker<br />
anvendes således inkubationstider<br />
på 16 timer i BCIP-NBT, hvilket giver<br />
en betydelig forbedring af sensitiviteten. Den<br />
meget lange inkubationstid er kun mulig i<br />
kraft af dels den gode holdbarhed af<br />
BCIP-NBT og dels af det faktum, at AP enzymet<br />
ikke inaktiveres så hurtigt som HRP under<br />
enzymreaktionen.<br />
Protokoller til visualisering af alkalisk<br />
phosphatase (AP) aktivitet<br />
a. Fast Red TR protokol:<br />
Naphthol AS-MX Phosphate Sigma<br />
No. N5000 10 ml<br />
Tris buffer 0,1 M pH 8,2 50 ml<br />
Levamisol 1 M 50 µl<br />
Fast Red TR salt Sigma No. F2768 50 mg<br />
Naphthol AS-MX opløses i Tris buffer. Opløsning er<br />
holdbar 14 dage ved 4°C. Lige før brug tilsættes<br />
Levamisol og Fast Red TR salt. I LSAB-AP <strong>teknik</strong>ken<br />
nedsættes mængden af levamisol til 25µl (se<br />
afsn. <strong>2.</strong>5.1). Når Fast Red TR er gået i opløsning<br />
filtreres. Inkubationstid: 20 - 60 min. Ønskes et<br />
blåt reaktionsprodukt erstattes Fast Red TR med<br />
Fast Blue BB (Sigma F3378).<br />
Mogens Vyberg 2005<br />
b. New Fuchsin protokol:<br />
Stamopløsning A:<br />
Naphthol AS-BI Phosphat Sigma<br />
No. N2250 25 mg<br />
N,N-Dimethylformamid Merck No. 3034 300 µl<br />
Stamopløsning B:<br />
Natriumnitrit 4%, frisk fremstillet 250 µl<br />
New Fuchsin 5% i 2 M HCl, Merck No. 4041 100 µl<br />
Tris buffer 0,05M, pH 8,7 50 ml<br />
Levamisol 1 M 50 µl<br />
New Fuchsin og natriumnitrit blandes under omrystning<br />
i 60 sek. Blandingen foregår i stinkskab,<br />
da der kan udvikles nitrøse dampe. Herefter tilsættes<br />
Tris buffer og til sidst Levamisol. I LSAB-AP<br />
<strong>teknik</strong>ken nedsættes mængden af levamisol til 25µl<br />
(se afsn. <strong>2.</strong>5.1).<br />
Arbejdsopløsning<br />
De frisk fremstillede stamopløsning blandes grundigt<br />
(opl. B i opl. A). Den færdige arbejdsopløsning<br />
filtreres før brug. Inkubationstid: 20-60 min.<br />
Fast Red TR og New Fuchsin protokollerne<br />
giver klare røde reaktionsprodukter, der er<br />
uopløselige i vandige medier. Fast Red TR<br />
reaktionsproduktet er ikke stabilt i organiske<br />
opløsningsmidler, hvorfor montering med<br />
hydrofile monteringsmidler er påkrævet. New<br />
Fuchsin reaktionsproduktet er angivet til at<br />
være stabilt i etanol og xylen (50), hvilket<br />
gør montering med hydrofobe monteringsmidler<br />
mulig. Egne undersøgelser har dog<br />
vist, at selv efter en hurtig dehydrering i etanol<br />
synes reaktionen svagere (og lysere i<br />
farvenuancen) i hydrofobt monterede præparater<br />
end i hydrofilt monterede præparater.<br />
Montering med hydrofilt monteringsmiddel<br />
synes derfor at være det sikreste - også for<br />
New Fuchsin fremkaldte præparater.<br />
Fast Red TR opløsningen er mere simpel at<br />
fremstille end New Fuchsin. Samtidig giver<br />
Fast Red reaktionsproduktet en intens orangerød<br />
fluorescens (53), der i fluorescensmikroskopet<br />
giver mulighed for en væsentlig<br />
mere sensitiv detektion af reaktionsproduktet,<br />
end den traditionelle lysmikroskopiske<br />
undersøgelse kan. En væsentlig ulempe ved<br />
Fast Red TR er, at reaktionsproduktet i acetone<br />
og NBF-fikserede frysesnit er meget<br />
granulært og med en udpræget tendens til<br />
diffusion ud fra den primære lokalisation af<br />
AP. Med New Fuchsin ses ikke de samme<br />
problemer på frysesnit. Reaktionsproduktet<br />
er mere amorft og homogent uden synlig<br />
tendens til diffusion. Lysmikroskopisk er New<br />
Fuchsin angivet til at være en smule mere<br />
sensitivt end Fast Red TR (50). På trods af<br />
dette må det anbefales, bl.a. på grund af den<br />
simple protokol og fluorokrom egenskaberne,<br />
at anvende Fast Red TR til cytologisk materiale<br />
og paraffinsnit. Til gengæld bør New<br />
Fuchsin rutinemæssigt anvendes på frysesnit.<br />
Kommercielle kits til AP-påvisning<br />
Udbudet af kits til AP-påvisning er stort. Hvad<br />
angår sensitivitet er der gode muligheder for<br />
at finde produkter, der giver en forbedret
44 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
sensitivitet i forhold til standardprotokollerne<br />
for Fast Red og New Fuchsin. En mindre,<br />
sammenlignende undersøgelse af 4 kommercielle<br />
kits og de 2 standardprotokoller viste,<br />
at alle 4 kits var mere følsomme end standardprotokollerne<br />
(4). Specielt gode resultater<br />
blev opnået med DakoCytomation’s Fast<br />
Red kit (K0597), DakoCytomation’s New<br />
Fuchsin kit (K0596) samt “Vector-Red” og<br />
“Vector Blue” fra Vector Laboratories. Alle 4<br />
kits gav en sensitivitetsforbedring svarende<br />
til en fortyndingsfaktor på de primære antistoffer<br />
på minimum <strong>2.</strong><br />
<strong>2.</strong>12 Kernefarvning<br />
For at kunne iagttage den præcise lokalisation<br />
af reaktionsproduktet i forhold til vævs-<br />
og cellemorfologien afsluttes den immunhistokemiske<br />
farvemetode sædvanligvis med<br />
en kernefarvning. Valg af kernefarvning afhænger<br />
af det anvendte kromogen. Farvning i<br />
Mayers Hæmatoxylin eller lignende vandige<br />
Hæmatoxylinopløsninger fungerer fint sammen<br />
med de fleste kromogener (Fast Red,<br />
New Fuchsin, AEC og DAB). En farvetid i<br />
Mayers hæmatoxylin på 2 min. er det almindelige,<br />
men ved påvisning af kernelokaliserede<br />
antigener kan farvetiden med fordel nedsættes<br />
til 30 sek. Mayers hæmatoxylin tåler<br />
montering med både hydrofile monteringsmidler<br />
(AquaMount, AquaTex, Glycergel o.l.)<br />
og hydrofobe midler (PerTex, DPX o.l.).<br />
Ethylgrøn (Methylgrøn) eller Neutralrød (50)<br />
kan med fordel anvendes, hvis BCIP-NBT<br />
bruges som kromogen. Ethylgrøn har ligeledes<br />
været anvendt i kombination med DAB<br />
og DAB-Nikkel. Det forudsætter blot, at der<br />
anvendes hydrofobe monteringsmidler, da<br />
Ethylgrøn ikke er særlig stabil i de hydrofile.<br />
Anvendes Ethylgrøn skal man yderligere være<br />
opmærksom på, at farvbarheden af cellekerner<br />
nedsættes efter HIER forbehandling (på<br />
grund af DNA denaturering).<br />
Azur B kan med fordel anvendes som kernefarvning<br />
i stærkt pigmenterede melanocytiske<br />
læsioner (55), hvor det kan være svært at<br />
skelne melanins egenfarve fra kromogener<br />
som AEC og specielt DAB. Azur B giver - foruden<br />
den blå kernefarvning - en intens grønblå<br />
farvning af melanin i melanofager, hvorved<br />
pigmentet let adskilles fra kromogenet.<br />
<strong>2.</strong>13 Referencer<br />
1. Kohler G, Milstein C. (1975). Continuous cultures of<br />
fused cells producing antibody of pre-difined specificity.Nature<br />
256: 495.<br />
<strong>2.</strong> Gatter KC, Falini B, Mason DY. (1984). The use of<br />
monoclonal antibodies in histopathological diagnosis.<br />
Recent Advances in Histopathology. Churchill Livingstone<br />
side 35-67.<br />
3 Lyon H. (1985). Histokemi I og II. DSR Forlag Landbohøjskolen<br />
KBH.<br />
4 Egne ikke publiserede data.<br />
5 Rasmussen BB, Hjort KN, Mellerup I, Sether G, Christensen<br />
N. (1992). Vegetable oils instead of xylene in<br />
tissue processing.APMIS 100: 827.<br />
6 Prioleau J, Schnitt SJ. (1995). p53 antigen loss in<br />
stored paraffin slides.The New England Journal Of<br />
Medicine 332: 1521.<br />
7 Brigati DJ, Budgeon LR, Unger ER, Koebler D, Cuomo<br />
C, Kennedy T, Permodo JM. (1988). Immunocytochemistry<br />
is automated: Development of a robotic<br />
workstation based upon the capillary action principle.<br />
The Journal of Histotechnology 11:165.<br />
8 Li C-Y, Ziesmer SC, Villareal OL. (1987). Use of azide<br />
and hydrogen peroxide as an Iinhibitor for endogenous<br />
in the immunoperoxidase method.The Journal of<br />
Histochemistry and Cytochemistry 35: 1457.<br />
9 Miller RT, Groothuis CL. (1990). Improved avidinbiotin<br />
immunoperoxidase method for terminal deoxyribonucleotidyl<br />
transferase and immunophenotypic<br />
characterization of blood cells.American Journal of<br />
Clinical Pathology 93: 670.<br />
10 Yam LT, Janckila AJ, Epremian BE, Li C-Y. (1989).<br />
Diagnostic significance of levamisol-resistant alkaline<br />
phosphatase in cytochemistry and immunocytochemistry.<br />
American Journal of Clinical Pathology 91: 31.<br />
11 Thisted K. (1995). The use of levamisol in immunohistochemistry.<br />
Pathology Research and Practice 191:<br />
797.<br />
12 Yokoyama S, Kashima K, Inoue S, Daa T, Nakayama<br />
I Moriuchi A. (1993). Biotin-containing intranuclear<br />
inclusions in endometrial glands during gestation and<br />
puerperium. American Journal of Clinical Pathology<br />
99: 13..<br />
13 Huang S, Minassian H, More JD. (1976). Application<br />
of immunoflourescent staining in paraffin sections<br />
improved by trypsin digestion. Laboratory Investigation<br />
35: 383.<br />
14 Curran RC, Gregory J. (1977). The unmasking of<br />
antigens in paraffin sections of tissue by trypsin. Experientia<br />
33: 1400.<br />
15 Battifora H, Kopinski M. (1986). The influence of<br />
protease digestion and duration of fixation on the<br />
immunostaining of keratins. The Journal of Histochemistry<br />
and Cytochemistry 34: 1095.<br />
16 Fraenkel-Conrat H, Brandon BA, Olcott HS. (1947).<br />
The reaction of formaldehyde with proteins. IV. Participation<br />
of indole groups. Journal of Biological<br />
Chemistry 168: 99<br />
17 Fraenkel-Conrat H, Olcott HS. (1948). Reactions of<br />
formaldehyde with proteins. VI. Cross-linking of<br />
amino groups with phenol imidazol, or indole groups.<br />
Journal of Biological Chemistry 174: 827.<br />
18 Fraenkel-Conrat H, Olcott HS. (1948). The reaction of<br />
formaldehyde with proteins. V. Cross-linking between<br />
amino and primary amide or guanidyl groups. Journal<br />
of the American Chemical Society 70: 2673.<br />
19 Shi SR, Key ME, Kalra KL. (1991). Antigen retrieval<br />
in formalin-fixed, paraffin-embedded tissues: An enhancement<br />
method for immunohistochemical staining<br />
based on microwave oven heating of tissue sections.<br />
The Journal of Histochemistry and Cytochemistry 39:<br />
741.<br />
20 Cattoretti G, Pileri S, Parravicini C, Becker MHG,<br />
Poggi S, Bifulco C, Key G, D’Amato L, Sabattini E,<br />
Feudale E, Reynolds F, Gerdes J, Rilke F. (1993). Antigen<br />
unmasking on formalin-fixed, paraffinembedded<br />
tissue sections. Journal of Pathology 171:<br />
83.<br />
21 Werner M, Wasielewski RV, Komminoth P. (1996).<br />
Antigen retrieval, signal amplification and intensification<br />
in immunohistochemistry. Histochemistry and<br />
Cell Biology 105: 253.<br />
22 Gown AM, Wever ND, Battifora H. (1993). Microwavebased<br />
antigenic unmasking. A revolutionary new<br />
technique for rutine immunohistochemistry. Applied<br />
Immunohistochemistry 1: 256.<br />
23 Leong ASY, Milios J. (1993). An assessment of the<br />
efficacy of the microwave antigen-retrieval procedure<br />
on a range of tissue antigens. Applied Immunohistochemistry<br />
1: 267.<br />
24 Bankfalvi A, Navabi H, Bier B, Böcker W, Jasani B,<br />
Schmid KW. (1994). Wet autoclave pretreatment for<br />
antigen retrieval in diagnostic immunohistochemistry.<br />
Journal of Pathology 174: 223.<br />
25 Norton AJ, Jordan S, Yeomans P. (1994). Brief, hightemperature<br />
heat denaturation (pressure cooking).: A<br />
simpel and effective method of antigen retrieval for<br />
Mogens Vyberg 2005
Anvendt immunhistokemi 45<br />
rutinely processed tissues. Journal of Pathology 173:<br />
371.<br />
26 Shi SR, Gu J, Kalra KL, Chen T, Cote RJ, Taylor CR.<br />
(1995). Antigen retrieval technique: A novel approach<br />
to immunohistochemistry on rutinely processed tissue<br />
sections. Cell Vision 2: 6.<br />
27 Shi SR, Imam SA, Young L, Cote RJ, Taylor CR.<br />
(1995). Antigen retrieval immunohistochemistry under<br />
the influence of pH using monoclonal antibodies.<br />
The Journal of Histochemistry and Cytochemistry 43:<br />
193.<br />
28 Beckstead JH. (1994). Improved antigen retrieval in<br />
formalin-fixed, paraffin-embedded tissues. Applied<br />
Immunohistochemistry 2: 274.<br />
29 Morgan JM, Navabi H, Schmid KW, Jasani B. (1994).<br />
Possible role of tissue-bound calcium ions in citratmediated<br />
high-temperature antigen retrieval. Journal<br />
of Pathology 174: 301.<br />
30 Reynolds GM, Young FI, Young JA, Williams A, Rowlands<br />
DC. (1994). Microwave oven antigen retrieval<br />
applied to the immunostaining of cytopathology<br />
specimens. Cytopathology 5: 345.<br />
31 Hølund B, Gundersen P, Holm K (1995). Can Ki67<br />
detection be used in selection between normal cells<br />
and carcinoma in situ in smears? 9th World Congress.<br />
Cervical Pathology & Colposcopy. Abstract 32<strong>2.</strong><br />
32 Tacha DE, McKinney L. (1992). Casein reduces nonspecific<br />
background staining in immunolabeling techniques.<br />
The Journal of Histotechnology 15: 127.<br />
33 Linscott www.linscottsdirectory.co.uk.<br />
34 MSRS www.antibodies-probes.com.<br />
35 Battifora H. (1986). The multitumor (sausage) tissue<br />
block: Novel method for immunohistochemical antibody<br />
testing. Laboratory Investigation 55: 244.<br />
36 Kraaz W, Risberg B, Hussein A. (1988). Multiblock: an<br />
aid in diagnostic immunohistochemistry. The Journal<br />
of Clinical Pathology 41: 1337.<br />
37 Miller RT, Groothuis CL. (1991). Multitumor “sausage”<br />
blocks in immunohistochemistry. Simplified method of<br />
preparation, practical uses, and roles in quality assurance.<br />
American Journal of Clinical Pathology 96:<br />
228.<br />
38 True LD. (1991). Parallel array method of embedding<br />
multiple tissue samples in a single paraffin block. The<br />
Journal of Histotechnology 14: 101.<br />
39 Stross WP, Jones M, Mason DY. (1989). Automation<br />
of APAAP immunocytochemical technique. The Journal<br />
of Clinical Pathology 42: 106.<br />
40 Pfeiffer P, Grabau DA, Nielsen O, Clausen PP. (1996).<br />
Immunohistochemical bulk staining of slides using a<br />
rack peroxidase-labelled streptavidin-biotin technique.<br />
Applied Immunohistochemistry 4: 135.<br />
41 Chilosi M, Lestani M, Pedron S, Montagna L, Benedetti<br />
A, Pizzolo G, Menestrina F. (1994). A rapid immunostaining<br />
method for frozen sections. Biotechnic and<br />
Histochemistry 69: 235.<br />
42 Larsson LI (1988). Immunocytochemistry: Theory<br />
and practice CRC Press, Inc. Boca Raton, Florida.<br />
43 Battifora H. (1991). Assesment of antigen damage in<br />
immunohistochemistry. The vimentin internal control.<br />
American Journal of Clinical Pathology 96: 669.<br />
44 Guesdon JL, Terynck T, Avrameas S. (1979). The use<br />
of avidib-biotin interaction in immunoenzymatic techniques.<br />
The Journal of Histochemistry and Cytochemistry<br />
27: 1131.<br />
45 Hsu SM, Raine L, Fanger H. (1981). Use of avidinbiotin-peroxidase<br />
complex (ABC). in immunoperoxidase<br />
techniques: a comparison between ABC and<br />
unlabeled antibody (PAP). procedures. The Journal of<br />
Histochemistry and Cytochemistry 29: 577.<br />
46 Isabella MG, Rüdiger WV, (1995). The SA/rABC technique:<br />
A new ABC procedure for detection of antigens<br />
at increased sensitivity. The Journal of Histochemistry<br />
and Cytochemistry 43: 31.<br />
47 DakoCytomation.<br />
48 Bobrow MN, Harris TD, Shaughnessy KJ, Litt GJ.<br />
(1989). Catalyzed reporter deposition, a novel<br />
method of signal amplification. Journal of Immunological<br />
Methods 125: 279.<br />
49 Merz H, Malisius R, MannWeiler S, Zhou R, Hartmann<br />
W, Orscheschek K, Moubayed P, Feller AC. (1995).<br />
Immunomax: A maximized immunohistochemical<br />
Mogens Vyberg 2005<br />
method for the retrieval and enhancement of hidden<br />
antigens. Laboratory Investigation 73: 149.<br />
50 De Jong ASH, Van Vark MVK, Raap AK. (1985). Sensitivity<br />
of various visualization methods for peroxidase<br />
and alkaline phosphatase activity in immunoenzyme<br />
histochemistry. Histochemical Journal 17:<br />
1119.<br />
51 Scopsi L, Larsson LI (1986). Increased sensitivity in<br />
peroxidase immunocytochemistry. A comparative<br />
study of a number of peroxidase visualizing methods<br />
employing a model system. Histochemistry 84:221.<br />
52 Boenish T (1989). Handbook. Immunochemical<br />
staining methods: s.23.<br />
53 Speel EJM, Schutte B, Wiegant J, Ramaekers FCS,<br />
Hopman AHN. (1992). A novel fluorescence detection<br />
method for In Situ Hybridization, based on the alkaline<br />
phosphatase-Fast Red reaction. The Journal of<br />
Histochemistry and Cytochemistry 40: 1299.<br />
54 Adams JC. (1992). Biotin amplification of biotin and<br />
horseradish peroxidase signals in histochemical<br />
stains. The Journal of Histochemistry and Cytochemistry<br />
40: 1457.<br />
55 Sayadi H, Fitzgibbon JF, Swanson PE, Wick MR.<br />
(1995). Azure B as a counterstain in the immunohistological<br />
evaluation of heavily pigmented nevomelanocytic<br />
lesion. Applied Immunohistochemistry 3:<br />
268.<br />
56 Williams JH, Mepham BL, Wright DH. (1997). Tissue<br />
preparation for immunocytochemistry. The Journal of<br />
Clinical Pathology 50: 42<strong>2.</strong><br />
57 Arbner JM, Arbner DA, Jenkins KA, Battifora H.<br />
(1996). Effect of decalcification and fixation in paraffin-section<br />
immunohistochemistry. Applied Immunohistochemistry<br />
4: 241.<br />
58 Dash RC, Ballo MS, Layfield LJ. (1998). Decay of<br />
androgen receptor immunoreactivity in archived tissue<br />
by using monoclonal antibody F39.4.1. Applied<br />
Immunohistochemistry 6: 145.<br />
59 Jacobs TW, Prioleau JE, Stillman IE, Schnitt SJ.<br />
(1996). Loss of tumor marker-immunostaining intensity<br />
on stored paraffin slides of breast cancer. Journal<br />
of the National Cancer Institute 88: 1054.<br />
60 Bertheau P, Cazals-Hatem D, Meignin V, de Roquancourt<br />
A, Vérola O, Lesourd A, Séné C, Brocheriou C,<br />
Janin A. (1998). Variability of immunohistochemical<br />
reactivity on stored paraffin slides. Journal of Clinical<br />
Pathology 51: 370.<br />
61 Shin HJC, Kalapurakal SK, Lee JJ, Ro JY, Hong WK,<br />
Lee JS. (1997). Comparison of p53 immunoreactivity<br />
i fresh-cut versus stored slides with and without microwave<br />
heating. Modern Pathology 10: 224.<br />
62 Grabau DA, Nielsen O, Hansen S, Nielsen MM, Lænkholm<br />
A-V, Knoop A, Pfeiffer P. (1998). Influence of<br />
storage temperature and high-temperature antigen<br />
retrieval buffers on results of immunohistochemical<br />
staining in sec-tion stored for long periods. Applied<br />
Immunohistochemistry 6: 209.<br />
63 Miller RT, Kubier P. (1997). Blocking of endogenous<br />
avidin-binding activity in immunohistochemistry. The<br />
use of egg whites. Applied Immunohistochemistry 5:<br />
63.<br />
64 Vyberg M, Nielsen S. (1998). Dextran polymer conjugate<br />
two-step visualization system for immunohistochemistry.<br />
A comparison of EnVision+ with two threestep<br />
avidin-biotin techniques. Applied<br />
Immunohistochemistry 6: 3.<br />
65 Sabattini E, Bisgaard K, Ascani S, Poggi S, Piccioli M,<br />
Ceccarelli C, Pieri F, Fraternali-Orcioni G, Pileri SA.<br />
(1998). The EnVision+ system: A new immunohistochemical<br />
method for diagnostics and research. Critical<br />
comparison with APAAP, ChemMate, CSA, LABC, and<br />
SABC techniques. Journal of Clinical Pathology 51:<br />
506.<br />
66 Erber WN, Willis JI, Hoffman GJ. (1997). An enhanced<br />
immunocytochemical method for staining bone marrow<br />
trephine sections. Journal of Clinical Pathology<br />
50: 389.<br />
67 von Wasielewski R, Mengel M, Gignac S, Wilkens L,<br />
Werner M, Georgii A. (1997). Tyramine amplification<br />
technique in routine immunohistochemistry. The<br />
Journal of Histochemistry & Cytochemistry 45: 1455.<br />
68 Brassil KE (1997). Antigen retrieval in immunohistochemistry<br />
- a new method using a domestic micro-
46 <strong>Immunhistokemisk</strong> <strong>teknik</strong><br />
wave pressure cooker. Australian Journal of Medical<br />
Science 18: 84.<br />
69 Taylor CR, Shi S-R, Chen C, Young L, Yang C, Cote<br />
RJ. (1996). Comparative study of antigen retrieval<br />
heating methods: Microwave, microwave and pressure<br />
cooker, autoclave and steamer. Biotechnic & Histochemistry<br />
71: 263.<br />
70 Shi S-R, Cote RJ, Chaiwun B, Young LL, Shi Y, Hawes<br />
D, Chen T, Taylor CR. (1998). Standardization of immunohistochemistry<br />
based on antigen retrieval technique<br />
for routine formalin-fixed tissue sections. Applied<br />
Immunohistochemistry 6: 89.<br />
71 Morgan JM, Navabi H, Jasani B. (1997). Role of calcium<br />
chelation in high-temperature antigen retrieval<br />
at different pH values. Journal of Pathology 182: 233.<br />
72 Pileri SA, Roncador G, Ceccarelli C, Piccioli M,<br />
Briskomatis A, Sabattini E, Ascani S, Santini D,<br />
Piccaluga PP, Leone O, Damiani S, Ercolessi C, Sandri<br />
F, Pieri F, Leoncini L, Falini B. (1997). Antigen retrieval<br />
techniques in immunohistochemistry: Comparison<br />
of different methods. Journal of Pathology<br />
183: 116.<br />
73 Shi S-R, Cote RJ, Taylor CR. (1997). Antigen retrieval<br />
immunohistochemistry: Past, present and future. The<br />
Journal of Histochemistry & Cytochemistry 45: 327.<br />
74 Leong ASY, Milios J. (1996). Epitop retrieval with<br />
microwaves. A comparison of citrate buffer and EDTA<br />
with three commercial retrieval solutions Applied Immunohistochemistry<br />
4: 201.<br />
75 Vyberg M (2000) Personlig meddelelse.<br />
76 Taylor CR, Shi S-R, Cote RJ. (1996). Antigen retrieval<br />
for immunohistochemistry. Applied Immunohistochemistry<br />
4: 144.<br />
77 Koopal SA, Iglesias Coma M, Tiebosch ATMG,<br />
Suurmeijer AJH. (1998). Low-temperature heating<br />
overnight in Tris-HCl buffer pH 9 is a good alternative<br />
for antigen retrieval in formalin-fixed paraffinembedded<br />
tissue. Applied Immunohistochemistry 6:<br />
228.<br />
78 Shi S-R, Guo J, Cote RJ, Young LL, Hawes D, Shi Y,<br />
Thu S, Taylor CR. (1999). Sensitivity and detection<br />
efficiency of a novel two-step detectionssystem<br />
(PowerVision). for immunohistochemistry. Applied<br />
Immunohistochemistry & Molecular Morphology 7:<br />
244.<br />
79 Wester K, Wahlund E, Sundström C, Ranefall P,<br />
Bengtson E, Russell PJ, Ow KT, Malmström PU, Busch<br />
C (2000). Paraffin section storage and Immunohistochemistry.<br />
Applied Immunohistochemistry & Molecular<br />
Morphology 8: 61.<br />
80 Olapade-Olaopa EO, Ogunbiyi JO, MacKay EH,<br />
Muronda CA, Alonge TO, Danso AP, Shittu OB, Terry<br />
TR, Wong AJ, Habib FK. (2001). Further characterization<br />
of storage-related alterations in immunoreactivity<br />
of archival tissue sections. Applied Immunohistochemistry<br />
& Molecular Morphology 9: 261.<br />
81 Van der Broeck LJCM, Van der Vijver MJ. (2000).<br />
Assessement of problems in diagnostic and research<br />
immunohistochemistry associated with epitope instability<br />
in stored paraffin sections. Applied Immunohistochemistry<br />
& Molecular Morphology 8: 316.<br />
82 Edgerton ME, Roberts SA, Montone KT. (2000). Immunohistochemical<br />
performance of antibodies on previously<br />
frozen tissue. Applied Immunohistochemistry<br />
& Molecular Morphology 8: 244.<br />
83 Kämmerer U, Kapp M, Gassel AM, Richter T, Tank C,<br />
Dietl J, Ruck P. (2001). A new rapid immunohistochemical<br />
staining technique using the EnVision antibody<br />
complex. The Journal of Histochemistry & Cytochemistry<br />
49:623.<br />
84 Boenisch T. (1999). Diluent buffer ions and pH: Their<br />
influence on the performance of monoclonal antibodies<br />
in immunohistochemistry. Applied Immunohistochemistry<br />
& Molecular Morphology 7: 300.<br />
85 Boenisch T. (2001). Formalin-fixed and heat-retrieved<br />
tissue antigens: A comparison of their immunoreactivity<br />
in experimental antibody diluents. Applied Immunohistochemistry<br />
& Molecular Morphology 9: 176.<br />
86 Leong AS-Y, Lee ES, Yin H, Kear M, Haffajee Z, Pepperall<br />
D. (2002). Superheating antigen retrieval. Applied<br />
Immunohistochemistry & Molecular Morphology<br />
10: 263.<br />
87 Marzo AMD, Fedor HH, Gage WR, Rubin MA. (2002).<br />
Inadequate formalin fixation decreases reliability of<br />
p27Kip1 immunochemical staining: Probing optimal<br />
fixation time using high-density tissue microarrays.<br />
Human Pathology 33:756.<br />
88 Shi S-R, Cote RJ, Liu C, Yu MC, Castelao JE, Ross RK,<br />
Taylor CR. (2002). A modified reduced-temperature<br />
antigen retrieval protocol effective for use with a<br />
polyclonal antibody to Cyclooxygenase-2 (PG 27).<br />
Applied Immunohistochemistry & Molecular Morphology<br />
10: 368.<br />
89 Nielsen S (2002). Personlig meddelelse.<br />
90 Petrosyan K, Tamayo R, Joseph D. (2002). Sensitivity<br />
of a novel biotin-free detection reagent (PowerVision+).<br />
for immunohistochemistry. Journal of Histotechnology<br />
25:247.<br />
91 Skacel M, Skilton B, Pettay JD, Tubbs RR. (2002).<br />
Tissue microarrays: A powerful tool for highthroughput<br />
analysis of clinical specimens: A review of<br />
the method with validation data. Applied Immunohistochemistry<br />
& Molecular Morphology 10:1.<br />
92 Nielsen L, Jensen J. (2003). Endogen peroxidase? –<br />
Metastase?: KL1 på Sentinel Node frysesnit. Erfaringer<br />
fra Vejle Sygehus. Poster ved “Histologisk årsmøde”<br />
for bioanalytikere.<br />
<br />
Mogens Vyberg 2005